子宫颈癌是发展中国家最常见的恶性肿瘤之一,其发病存在一个较长、可逆的癌前病变期,宫颈癌早诊、早治已成为流行病学和临床研究的热点。近年来,宫颈癌的发病率又有上升趋势,且年轻患者所占比例逐渐增加[1]。高危型人乳头瘤病毒(human papillomavirus,HPV)持续感染是宫颈癌发病的主要原因已被明确,因此,临床上HPV基因检测对于早期发现宫颈癌高危人群是必不可少的手段。本文总结2007年01月至2010年12月在暨南大学附属第一医院妇科及体检中心等行宫颈HPV基因分型检测病例1380例,探讨其在宫颈癌筛查中的临床意义。
1 资料和方法
1.1 研究对象 2007年01月至2010年12月在暨南大学附属第一医院妇科病房、妇产科门诊、皮肤科、健康体检中心行HPV基因检测病例共1380例。病例来源于因宫颈疾病住院或其他疾病需手术的病人;常规行健康体检的妇女:年龄≥30岁或<30岁,细胞学诊断结果≥未明确诊断意义的不典型鳞状上皮细胞 (atypical squamous cells of undetetemined sigificance,ASCUS),或具高危因素者(如多个性伴侣、性生活过早;CINⅡ~Ⅲ病史;人类免疫缺陷病毒(human immunodeficiency virus,HIV)感染史;免疫功能低下;乙烯雌酚暴露史;卫生条件差、性保健知识缺乏等)。年龄18~73岁,平均(37.71±5.6)岁。所有研究对象均有性生活,智力正常,剔除二次复查的数据。
1.2 仪器与试剂 I2Prism7000 PCR检测仪、HybriMax医用核酸分子杂交仪(均购自AB公司,美国),PCR试剂盒(QIAGEN公司,美国),HPV基因微阵列分型检测试剂盒、HPV取样器(均购自广州市凯普生物科技有限公司)。
1.3 标本采集 由医生以窥器暴露宫颈,拭净宫口分泌物,若同时取TCT行细胞学检测者,先取细胞学标本。采用广州市凯普生物科技有限公司提供的专用HPV取样器, 插入子宫颈内口, 顺时针或逆时针转动5~7周, 慢慢取出取样器折断,连同取样器头一同放入含有保存液的小瓶中, 随后送实验室置4℃冰箱保存,1周内完成检测。按照宫颈癌“三阶梯”筛查流程,对细胞学和/或HPV结果异常者行阴道镜及宫颈活组织病理检查。
1.4 检测方法 HPV检测是以HybriMax 导流杂交技术为平台, 利用QIAGEN公司的QIAMini试剂盒抽提DNA和应用AB I2Prism7000 PCR扩增仪做定性扩增。严格按照试剂盒说明进行操作,其步骤包括样本DNA提取、PCR扩增、导流杂交、酶标显色和结果分析[2]。能同时对21种HPV基因型进行分型,包括 HPV-16、-18、-31、-33、-35、-39、-45、-51、-52、-53、-56、-58、-59、-66、-68和-CP8304等13种高危型及3种中国人群常见基因型,HPV-6、-11、-42、-43、-44等5种低危型基因型。
1.5 数据整理和统计分析 采用VFP软件建立数据库,两遍录入原始数据,进行核对。应用SPSS 16.0 行统计分析,计量资料采用以 ±S表示,组间阳性率比较采用行×列表资料χ2检验;当行×列表中理论频数<1或者20%以上的理论频数1≤T<5时,则采用Fisher确切概率法。检验水准均为双侧α=0.05,以P<0.05为差异有统计学意义。
2 结果
2.1 宫颈HPV感染情况 1380例筛查对象中HPV感染例数为444例,占32.17%(444/1380),其中高危型HPV感染377例,占27.32%(377/1380);低危型HPV感染67例,占4.86%(67/1380);高危型与低危型同时感染38例,占2.75%(38/1380)。
2.2 HPV不同基因型别感染情况 本次筛查中覆盖了21种HPV基因型别中的20种,其中HR-HPV基因型感染率依次为: HPV-16型(33.16%,125/377)、HPV-58型(21.22%,80/377)、HPV-52型(20.16% ,76/377)、HPV-53型(10.61%,40/377)、HPV-33型(9.55%,36/377)、HPV-18型(6.90%,26/377)、HPV-cp8304型(4.24%,16/377)、HPV-31型(3.71%,14/377)、HPV-51,-59和-66型(均为2.65%,10/377)、HPV-39型(2.12% ,8/377)、HPV-35和-68型(均为21.59%,6/377)、 HPV-56型(1.06% ,4/377)和HPV-45型(0.53% ,2/377)。LR--HPV基因型感染率依次为:HPV-11型(40.30%,27/67)、HPV-6型(38.81%,26/67)、HPV-44型(11.94%,8/67)和HPV-42型(3.00%,2/67)。HPV-43型为惟一未检出基因型。 HR-HPV感染病例中,单一型别感染率为79.31%(299/377),双重型别感染率为15.91%(60/377),三重型别感染率为3.18%(12/377),四重以上型别感染率为1.59%(6/377),最多感染型别为1例18岁少女,同时感染10种HPV型别。本组感染率最高的5种HR-HPV基因型别为HPV-16、-58、-52、-53和-33型,其感染率分别为33.16%(125/377)、21.22%(80/377)、20.16%(76/377)、10.61%(40/377)和9.55%(36/377)。
2.3 不同年龄组HR-HPV感染情况 不同年龄组HR-HPV感染结果见表1,两组比较差异有统计学意义(P<0.05),其中≤35岁组最常见的感染型别依次为:HPV-16、-52、-58、-53和-33;>35岁组依次为:HPV-16、-58、-52、-53和-33。不同年龄组双重以上型别感染率结果见表2,两组比较差异无统计学意义(P>0.05),其中≤35岁组多重感染型别依次为:HPV-16、-52、-33、-58和-53;>35岁组依次为:HPV-16、-52,-58,-33和-53。
2.4 不同级别宫颈病变中HPV感染情况 根据细胞学和/或HPV结果异常行阴道镜检查及宫颈活组织检查,共取病理371例,各级宫颈病变HPV感染结果见表3,各组比较差异有统计学意义(P<0.05)。HR-HPV感染率随着宫颈病变级别上升而逐渐增加(χ2=404.333,P =0.000)。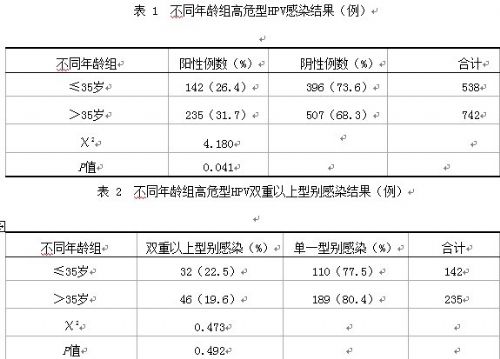
3 讨论
目前,宫颈细胞学检查结合HPV检测,根据检查结果进行阴道镜及宫颈病理活组织检查, 是生育年龄妇女宫颈癌筛查的主要方法,通过“三阶梯”诊断程序进行分层管理,制定宫颈癌个体化诊治方案。近年来,子宫颈癌的防治有了突破性进展,最重要的是确立了高危型人乳头瘤病毒持续感染是子宫颈癌发生的病因,已有的研究表明[3],大约82.4%的宫颈癌前病变与92%的宫颈浸润癌中存在HPV感染。HR-HPV检测是宫颈癌筛查的重要方法之一,当HPV感染细胞尚未引起细胞形态学改变时,即可检测为阳性,敏感度高,对于早期发现宫颈癌高危人群是必不可少的手段。《2010NCCN宫颈癌筛查临床实践指南》[4](National Comprehensive Cancer Network,NCCN Clinical Practice Guidelines in Oncology,Cervical Cancer Screening)新增对年龄≥30 岁受试者细胞学结果无异常,而HR-HPV呈阳性的处理办法。指南指出,HR-HPV阳性是行阴道镜检查的指征。而《2011NCCN宫颈癌筛查临床实践指南》则将HPV检测正式作为≥30岁妇女的宫颈癌筛查项目,作为宫颈细胞学检查的补充,同时将HPV检测列入阴道镜活检后对非典型腺细胞(atypical glandular cell,AGC )的处理。随着HR-HPV与宫颈癌关系的不断认识极大地促进了宫颈癌筛查新技术的开展,并有学者预测宫颈癌筛查模式将由形态学筛查转变为病原学筛查模式。宫颈细胞学检查联合HPV检测,可延长宫颈癌筛查间隔时间,提高筛查敏感度和特异度,降低医疗成本,增加患者依从性。而HPV检测结果对宫颈高度病变及宫颈癌发生风险的预测比宫颈细胞学和阴道镜检查结果敏感度更好、间隔时间更长,尤其适应于一些低资源地区[5]。
HPV检测方法包括细胞学法、斑点印迹法、荧光原位杂交法、原位杂交法、Southern杂交法、多聚合酶链反应(PCR)法、杂交捕获法以及表面等离子共振(surface plasma resonance,SPR)生物传感器分型检测[6]等,目前应用较多的是PCR法和杂交捕获法。第二代杂交捕获(hybrid capture,HC-Ⅱ)是迄今惟一获得美国食品与药品管理局(FDA)认证,并广泛用于临床的HPV检测手段,但其无法区分具体的HPV基因型, HR-HPV和LR-HPV不能同时检测,且不能判断多重感染。本实验采用改良导流杂交法(Improved HybriMax)是集PCR技术、核酸杂交技术、基因芯片技术和ELISA技术于一体的HPV基因分型检测的新方法,弥补了HC-Ⅱ的不足,能同时对21种HPV基因进行分型,且可判断多重感染。文献表明改良导流杂交法与HC-II法检测HPV高危基因型结果一致性好[7]。本研究结果显示随着宫颈病变级别进展,HPV感染率逐渐增加,与报道结果一致[8]。2010年一项包括欧洲、北美、南美、非洲、亚洲和大洋洲等全球范围的回顾性研究表明[9],宫颈癌患者最常见的HPV亚型为HPV-16,-18,-31,-33,-35,-45,-52和-58型,HPV-16,-18及-45型在年轻宫颈癌患者较其他年龄组患者中更为多见。 而在一项覆盖五大洲194项研究的Meta分析中[10]检测了1 016 719位细胞学正常的妇女宫颈HPV基因型,发现不同地区HPV感染率及感染高峰年龄均有差别,但最常见的十种基因型别均包括了HPV-16,-18,-31,-52和-58。本组研究人群中高危型HPV感染率为27.32%,最常见的五种高危HPV基因型别为HPV-16、-58、-52、-53和-33,不同年龄组HPV感染基因型及多重感染的基因型别中最常见的亦是此五种基因型,推测这可能是本地区妇女感染最常见的HPV基因型,HPV持续感染成为宫颈癌前病变甚至宫颈癌发生的主要原因。
HPV多重感染是否能促进子宫颈癌发生和进展一直是学者们关注的问题。有学者认为,HPV多重感染并不增加宫颈癌的发生,Kay等对南非宫颈癌和CINⅡ-Ⅲ的患者进行对比研究,发现CINⅡ-Ⅲ中多重感染为12.4%,宫颈癌中为16%,认为多重感染与宫颈病变的级别无关,多重感染并不增加宫颈癌的发生率[11]。NCCN指南中也指出,宫颈癌初筛使用HR-HPV检测,仅检测是否存在HR-HPV感染,而具体感染种类并不重要;同时不推荐对<21岁年轻女性进行HPV检测。同时Burd对文献进行了综述,认为生殖道HPV感染中存在不同类型的多重感染,可达39%,并且多重感染与病变的严重程度相关,并且指出约11.8%细胞学正常或ASCUS的女性和35.4%CINⅠ-Ⅱ的女性中可以见到HPV多重感染,并且至少有一种为高危型HPV[12]。由于不同亚型HPV其编码外壳蛋白的基因变异很大,各亚型之间基本上没有交叉保护性抗体,容易造成不同高危型HPV多重感染或多次感染。Lee等通过多因素分析发现单型别HPV感染使宫颈癌的患病风险增加19.9倍,而多重感染使该风险增加到31.8倍[13]。也有研究表明,对于2次以上检测HPV呈阳性时,只有检测出属于同一基因型才能确认是HPV持续感染。不同HR-HPV反复感染的CINⅡ/Ⅲ风险比为192,而相同HR-HPV持续感染的CINⅡ/Ⅲ 的风险比显著升高达813[14]。Spinillo等也对宫颈细胞学结果为ASCUS和LSIL行阴道镜检查的妇女进行HPV检测,结果发现HR-HPV多重感染与单一感染人群OR值为4.33 (95% CI=2.32-7.14) ,非HPV-16/-18型感染者OR值为2.76(95% CI=1.36-5.59),认为HPV多重感染是宫颈高度病变(≥CINⅢ)的一个重要危险因素[15]。本研究发现HPV双重以上型别感染率为20.69%,35岁以上妇女多重感染率较35岁以下妇女稍有下降,且基因型别有一定调整,估计部分HPV型别更难以被机体清除,从而成为导致宫颈高度病变及宫颈癌的主要病因。根据感染的HPV基因型别及有无多重感染可预测受检者发生宫颈癌的风险度,以决定其筛查后的处理方案。近年来年轻患者的宫颈癌发病率越来越高,故对于细胞学检查结果异常的年轻女性,可考虑进行HPV基因分型检测,依此可判断是相同型别HPV持续感染还是不同型别HPV重复感染,决定患者是否需进行阴道镜检查等进一步处理,尤其对于单纯HR-HPV感染患者更具临床指导意义。因此, HPV基因分型检测对判断该地区HPV流行状况的分析、疾病类型、治疗后的随访、HPV基因分型检测试剂的制定以及多价HPV基因疫苗的研制都有重要意义。对早期预防、早期发现和早期治疗宫颈癌有重要作用,如果能同时检测HPV病毒载量将能更好地对宫颈癌的处理方案进行合理评估。
 妇产科在线APP下载
妇产科在线APP下载