
2019年9月28日,正在西班牙巴塞罗拉进行的第19届ESMO(European Society for Medical Oncology,欧洲肿瘤内科学会)大会,Presidential symposium上公布了PRIMA(ENGOT-OV26 / GOG-3012)尼拉帕利在晚期卵巢癌一线维持治疗的最新临床结果并已同步发表于2019年9月28当日新英格兰医学杂志《The New England Journal Of Medicine》。研究结果显示,接受尼拉帕利治疗使总人群中疾病进展或死亡的风险降低了38%(PFS,HR 0.62;95%CI,0.50-0.75;p <0.001),同时在各预设的亚组分析中也获得了PFS延长。这一研究结果对晚期卵巢癌的一线维持治疗具有重要的指导意义。
就这一最新结果,本文特约浙江大学医学院附属妇产科医院谢幸教授进行解读,以飨读者。
专家简介

一、 应运而生——PRIMA研究满足晚期卵巢癌一线维持治疗需求
即使通过满意的肿瘤细胞减灭术联合铂类方案化疗达到CR或PR,晚期卵巢癌仍有70%的机率在2-3年内复发,给患者造成极大的心理负担和治疗上的困难。如何通过有效的一线维持治疗减少或延缓晚期卵巢癌的复发,一直是临床关注的热点之一。
GOG218等已有的研究表明,在伴有潜在风险的情况下,抗血管生成药物可以使晚期卵巢癌的PFS延长约2-6个月,这一结果还远远不能满足临床治疗的需求。
以“协同致死效应”为理论基础而研发的PARP抑制剂,最有可能为晚期卵巢癌维持治疗带来突破性进展。在复发性铂敏感卵巢癌维持治疗方面,PARP抑制剂(包括奥拉帕利、尼拉帕利等)的疗效和安全性已经被多项研究证实,并获得了FDA、EMA等批准上市。其中NOVA研究首次在入组人群中包含了gBRCA突变人群、HRD阳性[非gBRCA(non-gBRCA)]人群、以及non-gBRCA突变总人群(包含HRD阳性人群)三个队列,并在三组人群中均取得了PFS延长的结果,从而使尼拉帕利成为第一个获批用于铂敏感复发卵巢癌患者的维持治疗、而无论BRCA是否突变的PARP抑制剂。
在新诊断铂敏感晚期卵巢癌维持治疗方面,SOLO-1研究已经首开先例并获得了PFS显著延长的结果,使得奥拉帕利于2018年成为首个被FDA批准用于BRCA突变患者一线维持治疗的PARP抑制剂类药物。但SOLO-1研究仅入组了在人群占比约为20%左右的BRCAmut人群,其结果并不适用于其余多数的患者。正是在这样的背景下,PRIMA研究的设计和结果更加具有重要的临床价值。
二、 贴近临床——PRIMA研究设计符合晚期卵巢癌临床治疗实践
PRIMA研究(ENGOT-OV26/GOG-3012)是一项随机、双盲、安慰剂对照的III期临床研究,旨在检验新诊断的晚期卵巢癌患者(包括复发风险较高的患者)接受一线铂类化疗后,尼拉帕利治疗的疗效和安全性。对铂类有应答的患者以2:1比例随机分配至尼拉帕利或安慰剂组,通过PFS(无进展生存期)评估尼拉帕利作为维持治疗的有效性。本研究包括了尼拉帕利的个体化使用方案:基线体重<77公斤或血小板计数<150 K/μL的患者接受起始剂量200mg/天治疗,其他患者接受300mg/天治疗。
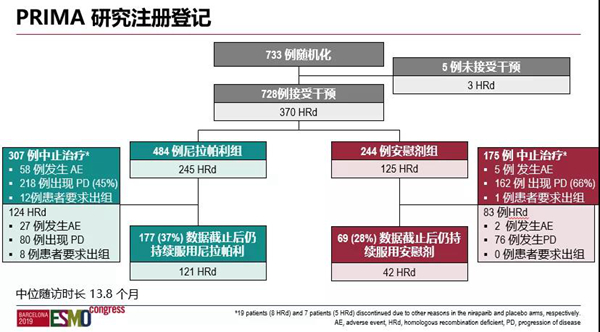
PRIMA研究的方案设计主要特点体现在以下方面:
(一)PRIMA研究:不论BRCA突变/HRD状态单药使用PARP抑制剂进行所有卵巢癌一线维持治疗的临床研究。
PRIMA研究是在标准含铂化疗达到PR/CR的基础上,对所有入组的晚期卵巢癌患者进行单药维持治疗。共有733例患者进入随机化,经myChoice检测,373例(51%)患者存在HRD,其中223例(31%)为BRCAmut,150例(20%)非BRCAmut,其余为HRDneg/Unknown患者。
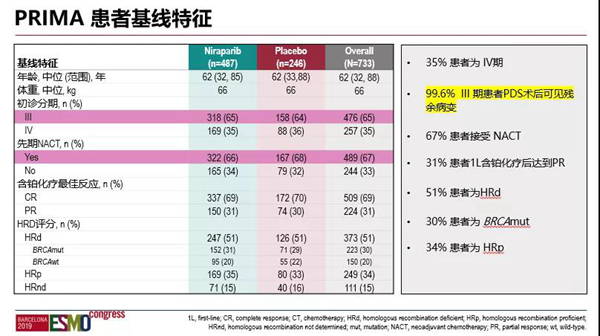
(二)PRMIA研究入组旨在解决晚期卵巢癌1线治疗中未满足的临床需求
除了上述的包括各种BRCA突变/HRD状态患者之外,PRIMA的入组人群还具备以下特点:
IV期患者占35.0%
III期卵巢癌PDS后病灶残留的患者比例为99.6%
接受新辅助化疗的人群占67%
一线铂方案化疗后部分缓解的患者占比30.5%
换言之,PRIMA研究入组具有高危复发风险的晚期卵巢病人,这使得PRIMA研究更加具有挑战性。
三、 疗效卓越——PRIMA研究在ITT人群及各分层人群中均取得PFS延长结果
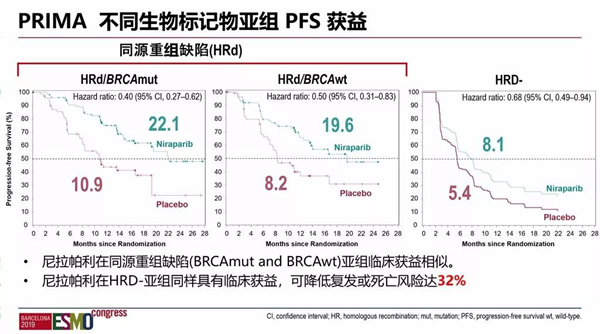
在疗效方面,PRIMA研究结果令人振奋:接受尼拉帕利治疗使ITT人群中疾病进展或死亡的风险降低了38%(PFS,HR 0.62;95%CI,0.50-0.75;p <0.001)。在HRD/BRCA状态不同的三个亚组中也取得了阳性结果:1)携带BRCA突变的肿瘤患者对PARP抑制剂的治疗敏感性最高,也是预后较好的患者人群。尼拉帕利使BRCAmut患者的中位PFS显著延长,疾病进展或死亡风险降低60%,HR 0.40(95%CI,0.27–0.62)p<0.001。2)同源重组缺陷(HRD)阳性BRCA野生型肿瘤患者的中位PFS同样显著延长,疾病进展或死亡风险降低50%,HR 0.50(95%CI,0.30-0.83),p = 0.006。以上两组人群(HRD阳性)的疾病进展或死亡风险降低57%,HR 0.43 (95% CI, 0.31–0.59) p <0.001。3)对于预后最差的HRD阴性患者本研究同样取得了阳性结果,尼拉帕利使疾病进展或死亡风险降低32%,HR0.68(95%CI,0.49–0.94),p = 0.020。特别值得一提的是,这是PARP抑制剂目前唯一在HRD阴性患者中显示阳性结果的临床试验。
在总生存期(OS)的期中分析中,根据目前已有的成熟数据,相对于安慰剂而言,尼拉帕利也显示出OS改善的趋势。预先计划的OS期中分析上,尼拉帕利对所有试验人群显示出了总生存获益(HR = 0.70;95%CI,0.44-1.11)。在HRD阳性的亚组中,91%接受尼拉帕利治疗的患者在满24个月时依然生存,而安慰剂组为85%(HR = 0.61; 95%CI,0.27-1.40)。OS期中分析还显示,在HRD阴性的亚组中,81%接受尼拉帕利治疗的患者在满24个月时依然生存,而接受安慰剂的患者则为59%(HR = 0.51;95%CI,0.27-0.97)。
在安全性方面,PRIMA研究与尼拉帕利既往的研究相似,安全可控,没有发现新的安全性信号。此外,尼拉帕利每天只需口服一次,且不受服药时间、食物等因素的影响,独特的代谢途径(羧酸酯酶)较少的的药物相互作用,这对于提高维持治疗的便利性和长期使用依从性是非常有利的。
作为卵巢癌领域的重镑研究,PRIMA研究结果已经于2019年9月28日在《The New England Journal Of Medicine》正式发表,并得到了广泛的关注,必将对晚期卵巢癌一线维持的治疗策略带来深远的影响。从临床实践来看,同源重组缺陷(HRD)的检测,国内尚无标准的检测方式,国际上FDA认可的HRD方法检测费用及检测方法复杂,难以临床普遍筛查。而对于初始卵巢癌患者,尼拉帕利是唯一已有数据证实无论HRD状态均可延长PFS的PARP抑制剂。期待未来有更进一步的研究为卵巢癌患者带来更多临床获益。
 妇产科在线APP下载
妇产科在线APP下载












