“我们都期待着一个健康宝宝的诞生!”3月24日,首都医科大学附属北京妇产医院内分泌科阮祥燕教授团队成功完成“中国首例”卵巢组织冻存移植后成功自然妊娠,孕周已满15周。这是继2016年该团队成功完成中国第一例卵巢冻存组织移植术后的又一壮举。
该患者在2016年被诊断为骨髓异常增生综合征,唯一能根治的方法就是造血干细胞移植,而骨髓移植前的超大剂量化疗对卵巢功能的损伤是极其严重的,几乎导致100%卵巢功能早衰,这不仅使患者永远丧失做母亲的机会,同时因为早绝经导致的各种更年期症状会提前10年、20年出现,早绝经引起的各种慢性病明显提前,早死的风险也明显增高。为了保存生育力及卵巢功能。在医院多科室联合下,阮祥燕教授生育力保护团队为其紧急实施了腹腔镜下微创卵巢组织取材手术,并将取出的卵巢组织成功冻存。
2018年,患者原发疾病完全缓解,但体内的卵巢功能早已衰竭。经过多学科讨论及国际专家会诊,实施了冻融卵巢组织自体再移植,3个月后患者恢复月经及卵巢内分泌功能,定期随访,有规律排卵。2020年12月30日,患者检查确定自然妊娠。2021年1月20日,超声显示“宫内可见妊娠囊,内见胎芽,胎心搏动可见”。
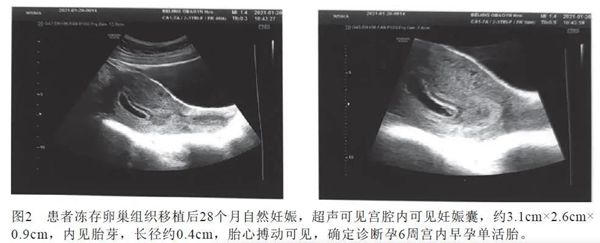
▲ 图片来源:中国临床医生杂志.
国际报道冻融卵巢组织在移植后1年内的存活率仅为63%,且多数患者在移植1年内妊娠,鲜有移植2年后妊娠的报道。卵巢组织维持活性的时间取决于组织中的卵泡数量。研究显示,超过75%的卵泡死亡发生于移植早期,与卵巢组织冻融与移植技术息息相关。本研究患者29岁,卵巢皮质中卵泡密度并不高,但在移植后3个月卵巢功能恢复,且维持规律排卵至2年后自然妊娠,证实北京妇产医院生殖中心冻存卵巢组织移植后卵泡丢失率低、存活率高,医院卵巢组织冻存与移植技术达国际先进水平。
卵巢组织冻存:新型生育力保护方法
2020年中国新发肿瘤患者450多万,各种良恶性肿瘤侵犯着女性健康,高达78.3%的年轻癌症患者有生育需求。但疾病本身和放疗、化疗等癌症治疗会对卵巢造成严重的不可逆性损伤,使女性在癌症治疗后可能永远失去做母亲的机会。因此,癌症患者的生育力保护社会需求极大而且更为迫切。
目前,对女性生育力保护与保存已成为世界医学领域广泛关注和重视的焦点,其中,最备受关注的就是卵巢组织冻存移植技术,这是一种新兴的生育力保护方法,也就是在患者进行放化疗前,通过腹腔镜微创手术先取出部分卵巢组织在体外冷冻、冻存起来,待患者原发疾病临床缓解后再将组织移植回体内的一种生育力保护技术。世界上通过该技术诞生的孩子已经有200多例,相关的大量研究也正在开展中。2012年,在国家外专局、市外专局、市科委、市卫生健康委、市医管中心等相关单位的支持下,北京妇产医院与德国图宾根大学、波恩大学、海德堡大学以及德国绝经学会等建立了多渠道的合作与交流,同年,医院建立了中国首个人卵巢组织冻存库。
迄今为止,北京妇产医院卵巢组织冻存库已为300多例的儿童及年轻患者进行了卵巢组织冻存,并成功进行了10例冻融卵巢组织移植,术后卵巢功能全部恢复正常,移植成功率100%,达到了国际领先水平。目前,在北京妇产医院卵巢组织冻存库进行冻存卵巢组织的患者年龄最小的只有1岁3个月。
1.卵巢组织冻存(OTC)的适用对象
OTC年龄限制为35岁,根据个人意愿和卵巢储备情况可适当放宽年限。有数据表明,OTC时年龄为35岁及以下的女性,冻融移植后妊娠率为33%,而大于35岁女性的妊娠率为18%。
OTC的筛选标准:
①无足够时间进行卵母细胞冻存或胚胎冷冻,需马上进行放疗、化疗或骨髓移植的肿瘤患者。患者必须排除卵巢恶性肿瘤或卵巢转移,转移风险高者应慎重考虑,患者应能够耐受腹腔镜或开腹取卵巢活检手术;
②免疫治疗失败的自身免疫病患者(系统性红斑狼疮、类风湿关节炎);
③需进行骨髓移植血液系统疾病的患者(重型地中海贫血症、再生障碍性贫血、镰刀状细胞贫血症);
④家族或基因检测携带POF高风险基因的患者;
⑤因社会、经济或年龄因素推迟生育者。
2.卵巢组织的移植
冻融卵巢组织移植回体内后超过95%的患者可以恢复生殖内分泌功能,在4个月左右恢复生理周期,卵巢功能平均持续时间约为5年。许多研究仍在追踪卵巢组织移植后女性卵巢的功能变化,因此最长的卵巢功能持续时间尚有待确定。移植后卵巢的寿命取决于卵巢组织冻存者的年龄、卵巢组织内卵泡的密度、分布、卵巢组织的大小、冷冻方法及移植位置。
3.卵巢组织移植的潜在风险
肿瘤患者的卵巢组织冻存时可能含有肿瘤细胞,移植后存在着肿瘤细胞在患者体内再次入侵、传播的风险。根据肿瘤细胞转移至卵巢组织风险的不同将肿瘤分为低风险型(乳腺癌Ⅰ~Ⅱ期、子宫颈鳞癌、霍奇金淋巴瘤、肾母细胞瘤等)、中风险型(乳腺癌Ⅳ期、结肠癌、子宫颈腺癌、非霍奇金淋巴瘤等)和高风险型(白血病、神经母细胞瘤、伯基特淋巴瘤)。有研究预测卵巢组织冻存-移植后肿瘤细胞再传播的概率约为1%,尤其是白血病转移风险最高。
在卵巢组织移植前,通过分子生物学技术、荧光原位杂交、免疫组织化学、免疫缺陷小鼠移植及其他方法严格监测移植组织被是否被肿瘤细胞污染,可降低卵巢组织移植后肿瘤细胞的再引入风险,但并不能完全排除再引入肿瘤细胞的风险。因此有研究者建议高转移风险患者可进行原始卵泡体外培养成熟后借助IVF技术妊娠或在肿瘤细胞的豁免期进行OTC。
4.卵巢组织冻存技术的优势
(1)避免了大剂量、长时间的前期激素刺激,只要患者可以耐受手术,立即可以实施,节约时间,不会延误癌症的治疗。
(2)卵巢组织中的卵泡储备量大,一片组织中的卵泡数可成百甚至上千。
(3)在复苏、移植成功后,可恢复的不仅是生育能力,卵巢的内分泌功能也能得到恢复。
(4)是青春期前患者和急需癌症治疗的患者唯一的生育力保护选择。
卵巢组织冷冻为年轻肿瘤患者生育力的保存带来了新希望,不仅可以恢复患者的生育能力,提高肿瘤患者治愈后的生活质量,也可以作为健康女性推迟绝经期的一种治疗手段。目前,OTCT技术无统一的实施方案,不同的实验室或生殖中心均有自己的实验程序,成功率为23%~41%,因此需制定全球性统一的OTCT规范,以更好地评价和实现该技术。
再次祝贺中国首例卵巢组织冻存移植患者自然妊娠成功!
参考来源:央视新闻、中华生殖与避孕杂志、中国临床医生杂志.
 妇产科在线APP下载
妇产科在线APP下载












