荧光原位杂交(fluorescence in situ hybridization,FISH)技术起源于20世纪60年代末和70年代初,其原理是基于碱基互补原则,采用荧光素标记的探针与被检样本中的DNA或RNA杂交后,在荧光显微镜下检测荧光信号来显示特定核苷酸序列的存在,定位及数目,可用于组织切片、细胞涂片及染色体制片等组织标本[1]。研究证实人染色体端粒酶基因(human telomerase gene,hTERC)与宫颈癌的发生和进展有着密切的关系,近两年已有多项研究应用FISH技术检测宫颈脱落细胞中hTERC基因表达,发现hTERC基因扩增随着宫颈病变分级呈逐渐上升趋势[2-4] 。本研究应用FISH技术检测宫颈石蜡标本中的hTERC基因表达情况,旨在探讨其临床意义。
1 材料和方法
1.1 临床资料 收集2008年10月至2010年3月暨南大学附属第一医院妇科102例宫颈活检或切除宫颈石蜡标本,包括对照组10例(活检为正常宫颈上皮),研究组92例(CINⅠ级20例,CINⅠ-Ⅱ级28例,CINⅡ级20例,CINⅢ级14例,宫颈癌10例,其中鳞癌8例,鳞腺癌2例,均为Ⅰa-Ⅰb期),对照组平均年龄(35.7±6.8)岁,CIN平均年龄(36.2±9.0)岁,宫颈癌平均年龄(41.1±7.1)岁。所有受检者接受治疗前进行宫颈薄层液基细胞学检查(Thinprep cytologic test,TCT)及HPV-DNA(human papilloma viral,HPV)分型检测,阴道镜下取活检。宫颈上皮内瘤变(cervical intraepithelial neoplasia,CIN)和宫颈癌患者在我院由固定医生给予治疗。CINⅠ-Ⅱ级以上病变予宫颈电热圈环切术(loop electrosurgical excision procedure,LEEP ) 或冷刀锥切(cold-knife conization ,CKC),切缘均为阴性;宫颈癌予根治性切除为主的综合治疗,术后6-12个月复查,行HPV-DNA检测,研究组中有72例完成随访。
1.2 方法
1.2.1 标本采集 将宫颈活检或手术切除宫颈标本进行石蜡包埋,HE染色后显微镜观察病变程度并经两位病理医生复核作出病理诊断。取其典型病灶处石蜡白片连续切片3-5张,厚度为2-4um,涂胶片贴连。
1.2.2 FISH杂交前预处理 二甲苯脱腊2次,梯度乙醇复水;30%[W/V]酸性亚硫酸钠疏解细胞外基质蛋白成分;蛋白酶K工作液消化组织切片;梯度乙醇脱水;待玻片自然干燥后加热至56℃。
1.2.3 FISH检测hTERC基因扩增方法 由北京金菩嘉公司提供hTERC/CSP3 DNA双色探针(染色体位点特异性探针/着丝粒探针),CSP3作为对照探针。主要操作流程:①钻石笔标记杂交区域后置入73℃70%甲酰胺/2×SSC变性液中5mim,-20℃下梯度乙醇脱水,之后45-50℃烤片机上烘烤。②室温下配制探针混合物(杂交缓冲液:探针:去离子水=7:2:1)离心后混匀。加探针混合物10ul于玻片杂交区,盖玻片,用封片胶封片,42℃杂交过夜。③次日洗涤玻片:将玻片依次置于3瓶46℃甲酰胺洗涤液中各10mim, 2×SSC溶液浸泡10mim后2×SSC/0.1%NP-40溶液中5mim,再浸入70%乙醇3mim后待自然干燥。④将15ulDAPI复染剂滴加于杂交区,盖玻片暗处放置后荧光显微镜下阅片。
1.3 统计学方法 用SPSS13.0软件包进行统计学分析,组间阳性率比较采用计数资料χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 对照组与研究组TCT结果 所有病例活检前均行TCT检查,结果按照2001年TBS系统( the Bethesda system)进行细胞病理学分类。宫颈鳞状上皮细胞的诊断包括:①未见上皮内病变或恶性病变 (No intraepithelial lesion or Malignant, NILM),包括正常宫颈细胞及炎性改变、反应性改变等良性病变;②鳞状上皮细胞异常:非典型鳞状上皮细胞(Atypical squamous Cells, ASC),又分为意义不明的非典型鳞状上皮细胞(Atypical squamous Cells ofUndetermined Signification, ASC-US)、不能排除高度鳞状上皮内病变的非典型鳞状上皮细胞(Atypical squamous Cells-Cannot exclude HSICL, ASC-H);③鳞状上皮内低度病变(Low-grade IntraepithelialLesinon, LSIL );④鳞状上皮内高度病变(High-grade Intraepitheliai Lesion,HSIL);⑤鳞状细胞癌(SCC)。腺上皮分析包括宫颈细胞和宫内膜细胞癌,分为非典型腺细胞(AtypicalGlandular cel,l AGC )、可疑腺癌、原位腺癌、腺癌(AC)。表1显示对照组与研究组TCT检查结果,10例正常宫颈病例中有4例为ASC-US,占40%(4/10);在CIN和宫颈癌组中NILM占22.8%(21/92);CINⅡ以上病变及宫颈癌中有27例ASC-US,占37.5%(27/72)。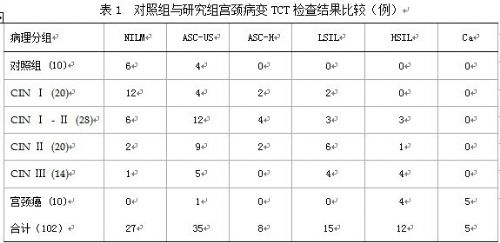
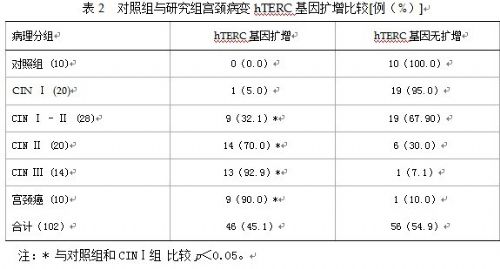
2.2 对照组与研究组hTERC基因扩增结果 FISH技术检测宫颈石蜡切片hTERC基因扩增阳性细胞正常阈值的建立及结果判定标准参照宫颈脱落细胞检测方法[5],以异常细胞数/计数细胞总数≥5为hTERC基因扩增阳性。表2显示对照组和研究组中CINⅠ组与CINⅠ-Ⅱ、Ⅱ、Ⅲ级及宫颈癌组hTERC基因扩增比较有统计学意义(p<0.05),CINⅡ以上病变hTERC基因扩增明显高于CINⅠ及以下病变,随着病变程度递增,hTERC基因的阳性表达率增加。
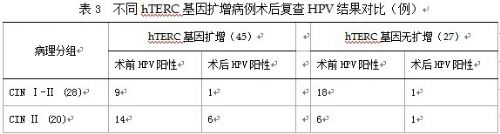
2.3 手术前后HPV-DNA检测结果 病理结果在CINⅠ-Ⅱ级以上病变予相应治疗,术后6-12个月复查,共有72例患者行HPV-DNA分型检测,完成随访。表3示手术治疗72例病例中术前HR-HPV感染率达98.6%(71/72),高于文献报导[6],其中45例hTERC基因扩增者术后13例再次出现高危型HPV(high-risk human papilloma viral,HR-HPV)阳性,占28.9%(13/45,其中CINⅠ-Ⅱ1/9,CINⅡ6/14,CINⅢ4/13,宫颈癌2/9),同一亚型占46.2%(6/13),其它亚型占53.8%(7/13)。27例hTERC基因无扩增病例中术后仅有2例出现HR-HPV阳性,占7.4%(2/27),其中1例合并尖锐湿疣,另1例为再生障碍性贫血患者。两组比较具有统计学意义(p<0.05)。
3 讨论
子宫颈癌的发生发展是一个连续的过程,对宫颈上皮内瘤变作出早期、准确的诊断并给予恰当的治疗可以降低宫颈浸润癌的发生,改善妇女生殖健康。目前宫颈癌筛查采用“三阶梯”方案虽大大降低了宫颈癌的发病率,但是细胞学检查可因诊断者对TBS系统的理解不同而存在较大的主观性及差异,其敏感性和重复性较低,常导致ASCUS的诊断分流存在一定争议。HPV检测具有较高的敏感性,但HPV感染后只有少部分发展为宫颈癌前病变及浸润癌。病理学检查是宫颈病变的最终诊断,但也会因病理医生诊断水平不一而有所偏倚。在本研究中,从病理结果追溯其细胞学情况,CIN及宫颈癌病变中有22.8%细胞学结果阴性,而在细胞学为ASCUS的病例中病理结果级别参差不齐,提示细胞学检查具有一定的漏诊和误诊率。近年来对端粒酶与肿瘤发生的关系研究较多,发现宫颈上皮细胞由非典型性异常向宫颈癌转变过程中几乎都伴有人类染色体端粒酶基因(hTERC)的扩增[5],Heselmeyer 等还对进行hTERC基因检测的患者随诊3年,发现hTERC基因扩增的CINⅠ-Ⅱ患者进展到CIN Ⅲ者多于基因阴性者,因此认为hTERC基因检测可作为宫颈病变进展的一个预测指标[7]。2006年至2009年国家卫生部医药卫生科技发展研究中心在全国83家医院进行了多中心临床研究,应用FISH技术对9858例宫颈脱落细胞标本进行hTERC基因检测,发现其筛查高级别宫颈病变(CINⅡ、Ⅲ)的敏感度和特异度分别为77.52%和71.82%,阳性预测值和阴性预测值分别为66.42%和81.63%[8] 。目前国内外多数研究是采用宫颈脱落细胞标本进行检测,但脱落细胞并无组织结构,其生物特性与活体细胞不全相同,对脱落细胞进行检测仍有可能造成漏诊。而且hTERC基因检测设备和试剂昂贵,如果对细胞学结果异常的病例进行基因检测则的筛查会造成较大浪费。Andersson等[9]曾对12例早期宫颈腺癌石蜡包埋的宫颈组织进行hTERC基因检测,发现全部病例均存在此基因的扩增。本研究应用FISH技术对宫颈活检后石蜡切片进行hTERC基因检测,无须重复取材,而且对于灶性病变可以选择病变典型处取材,其组织标本来源与活体细胞的一致性好。随着病变级别增高,hTERC基因阳性表达率增加,该结果与病理学诊断符合率高,具有更高的敏感性和特异性。现阶段国内不少医生由于对宫颈癌的发生发展及其癌前病变的认识不足,对CIN存在过度治疗的问题,给不少妇女造成不必要的宫颈机能丧失等并发症[10]。本研究表明hTERC基因有扩增者术后重复感染HR-HPV的可能性比hTERC基因无扩增者高。因此,对宫颈病理学检查异常的标本进行hTERC基因检测可以协助宫颈CIN的诊断分流,指导临床正确处理和术后随诊判断预后具有较好的临床意义。
 妇产科在线APP下载
妇产科在线APP下载