作者:中国抗癌协会肿瘤内分泌专业委员会 中国抗癌协会妇科肿瘤专业委员会
通讯作者:周琦,重庆大学附属肿瘤医院,重庆 400030,电子信箱:qizhou9128@163.com;吴小华,复旦大学附属肿瘤医院,上海 200032,电子信箱:docwuxh@126.com
执笔专家:邹冬玲(重庆大学附属肿瘤医院)
主审专家:周琦(重庆大学附属肿瘤医院);吴小华(复旦大学附属肿瘤医院)
参编专家(以姓氏笔画为序):王丹波(中国医科大学肿瘤医院/辽宁省肿瘤医院);王莉(河南省肿瘤医院);朱笕青(中国科学院大学附属肿瘤医院/浙江省肿瘤医院);向阳(中国医学科学院北京协和医院);刘乃富(山东省肿瘤医院);刘继红(中山大学附属肿瘤医院);李长忠(山东省立医院);李秀琴(中国医科大学附属盛京医院);李政(云南省肿瘤医院);李凌(江西省妇幼保健院);吴令英(中国医学科学院肿瘤医院);张师前(山东大学齐鲁医院);林仲秋(中山大学孙逸仙纪念医院);易琳(重庆大学附属肿瘤医院);娄阁(哈尔滨医科大学肿瘤医院);夏百荣(安徽省肿瘤医院);黄裕(重庆大学附属肿瘤医院);蔡红兵(武汉大学中南医院)
BRCA1/2基因是抑癌基因,通过与其他肿瘤抑制因子和调节细胞分裂蛋白等相互作用,参与DNA损伤修复和转录调控,在维持细胞遗传信息的稳定性方面发挥至关重要的作用,并通过调控其他基因的活性,在胚胎发育中起着重要作用[1-2]。
BRCA1/2基因检测是基因健康服务的新兴技术之一,已广泛应用于妇科恶性肿瘤尤其是卵巢癌的精准诊疗。然而基因检测作为新生事物,存有不少的弊端与漏洞。首先,受制于技术与认知的局限,一部分基因突变与疾病的确切关系还无法完全验证。5%的BRCA突变基因为未知变异,最后结论不确定。除此之外,对基因检测准确性的疑问主要来自实验操作与样本的处理方法,各实验室采集的样本类型、收集方法、样品处理、分析方法、比对解读以及结果报告等各有不同,致使结论存在差异[3]。因此,BRCA1/2基因检测的质量评价面临标准(包括标准序列及标准数据库等)缺失的挑战,是制约BRCA突变基因检测发展的关键。
促进、建立和健全BRCA突变基因检测的行业标准化体系,规范基因健康服务的各个环节,保障检测结果的质量,用高标准引领生命健康行业高质量发展,显得尤为紧迫。国家标准化管理委员会已于2018年将基因健康服务业标准化试点纳入项目计划,旨在加以引导和规范。
基因数据分析和解读,是掣肘基因测序发展的关键。目前,BRCA1/2基因检测虽已较为广泛应用,但不同检测机构的报告形式与内涵参差不齐。为统一报告形式,解决行业弊端,补充完善临床所需必备内容,提供足够解读信息以满足临床需求,中国抗癌协会肿瘤内分泌专业委员会联合中国抗癌协会妇科肿瘤专业委员会组织专家,结合国内部分主流基因检测公司及机构的报告模板,在集思广益的基础上形成本专家指导意见。
1 BRCA1/2基因检测报告单
受检者基本信息见表1。
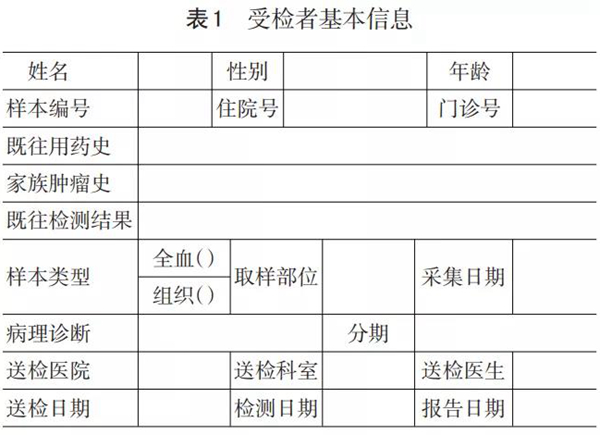
2 检测结果
2.1 胚系突变 检测结果见表2。根据《BRCA1/2数据解读中国专家共识(2021年版)》[4],将BRCA突变的分类命名分为以下5类。(1)致病性:表示该突变在现有临床意义和功能研究中被证实与疾病发生相关,其致病机制明确,或者遗传统计学意义显著,或者有相关功能验证。(2)可能致病性:表示该突变在现有研究数据中显示可能是致病的,但需进一步的临床意义和功能研究证明。(3)意义未明:表示该突变在现有的科学研究中尚不明确其与相关疾病发生风险的关系。(4)可能良性:表示该突变在现有研究数据中表明可能是不致病的,但需进一步的临床意义和功能研究确认。(5)良性:表示该突变在现有的临床意义和功能研究中表明其不会导致疾病的发生,与疾病表型无相关性。随着技术研究的深入,可能出现新的证据支持非致病性突变转变为致病性突变的情况,如有需要,需重新签发报告。

2.2 体细胞突变 检测结果见表3。根据诊断、治疗和预后的证据级别,将体细胞突变分为以下4个等级。
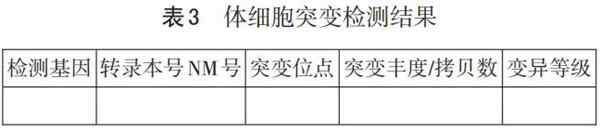
2.2.1 Ⅰ级 临床意义明确的突变。支持证据等级为:①Level A:FDA/NMPA批准于某种特定肿瘤治疗有响应或耐药,或来自专业指南中对某特定肿瘤作为治疗、诊断或预后的生物标志;②Level B:取得该领域专家共识,良好的动力学研究预测对治疗有响应或耐药,或对某疾病的诊断、预后意义。
2.2.2 Ⅱ级 具有潜在临床意义的突变。支持证据等级为:Level C:FDA/NMPA或专业协会批准对不同肿瘤类型治疗响应或耐药,或已作为临床试验的筛选入组标准,或基于多项小型研究具有诊断或预后意义。Level D:研究结果表明对其他肿瘤诊断、治疗或预后意义,临床前研究显示可能具有治疗意义,对于生物标志物本身或与其他生物标志物一起,基于一些小型研究或未达成共识的多个案例报道可能有助于疾病诊断或预后意义。
2.2.3 Ⅲ级 临床意义未明的突变。
2.2.4 Ⅳ级 良性或可能良性的突变。本报告的突变命名和解读参考相关人类基因组变异协会(HGVS)、美国病理学(AMP)、美国医学遗传学和基因组学学会(ACMG)、美国临床肿瘤学会(ASCO)和美国病理学家学会(CAP)[5-7]。
3 其他良性或意义未明突变
3.1 胚系突变 检测结果见表4。
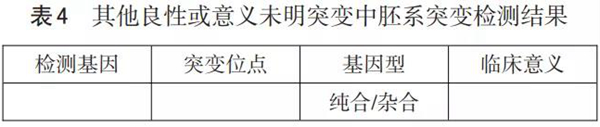
3.2 体细胞系突变 检测结果见表5。
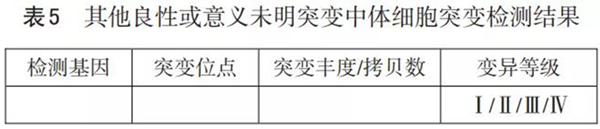
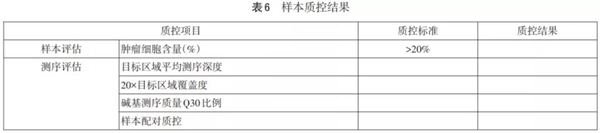
4 样本质控
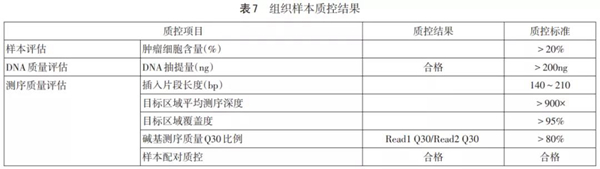
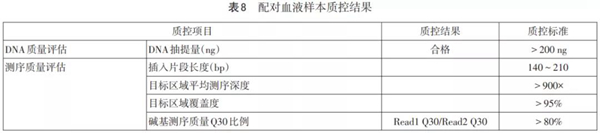
样本质控结果见表6。根据实际情况,又分为组织样本和配对血液样本2个质控。结果见表7~8。
5 临床用药详细解析
此部分内容根据最新高级别循证医学证据而持续更新。
6 关于本检测
6.1 本检测说明 本报告通过检测肿瘤组织或配对血液样本的BRCA基因全部外显子及其邻近±20 bp内含子区域,并对检测结果进行详细解读,为肿瘤患者的临床诊断治疗提供辅助参考[8-9]。本报告主要检测肿瘤相关基因的变异情况,对变异的解读参考相关指南和规范。报告给出的这些变异信息(和无变异信息)可为临床医生的决策提供参考,受检者请在临床医生的指导下阅读本报告。本报告中的基因变异和药物排名不分先后顺序。本报告中,任何一个标志物变异和潜在有效或无效药物均不按照先后顺序排名。本报告不对任何患者承诺或保证会在某一药物治疗中有效,也不承诺在某一药物治疗中无效。
6.2 检测方法与局限性[10] 技术检测可同时检测目标基因的单核苷酸变异(SNV)、小片段插入/缺失(InDel)、胚系拷贝数变异(CNV),仅采用高通量测序方法检测胚系CNV时具有一定的技术局限性。本产品可检测出一定突变丰度以上的体系变异,产品的检测性能与样本质量密切相关,样本质控等级以及某些变异特征会降低检测敏感度。
肿瘤具有异质性,不同肿瘤细胞之间的基因突变谱不同,相同肿瘤细胞不同区域之间的基因突变谱也可能不同,肿瘤发展或治疗过程中同样可能出现原发部位与继发部位肿瘤基因突变谱的差异。本报告中的检测结果仅反映本次送检样本的情况。
检测技术是否包含大片段重排(LGR)的说明,在亚洲人群中,LGR在所有BRCA1/2基因突变中占比在7%以下;一项包含555例中国南方城市乳腺癌/卵巢癌患者的研究表明,LGR占所有BRCA1/2基因突变的5.8%,BRCA1基因LGR的比例(6.9%)高于BRCA2基因(5%)。
本报告仅对送检样本负责,报告结果仅供参考,不代表临床决策意见,不作为临床诊断的依据。临床决策和诊断需要临床医生根据检测者各项检测结果进行综合评判。
实验操作者: 日期:
报告审核者: 日期:
利益冲突:专家组所有成员均声明不存在利益冲突。
参考文献
[1]Lord CJ,Ashworth A.PARP inhibitors:synthetic lethality in the clinic[J].Science,2017,355(6330):1152-1158.
[2]Mighton C,Charames GS,Wang M,et al.Correction:variant classification changes over time in BRCA1 and BRCA2[J].Genet Med,2019,21(10):2406-2407.
[3]《临床分子病理实验室二代基因测序检测专家共识》编写组.临床分子病理实验室二代基因测序检测专家共识[J].中华病理学杂志,2017,46(3):145-148.
[4] 中华医学会病理学分会,国家病理质控中心.BRCA1/2数据解读中国专家共识(2021版)[J].中华病理学杂志,2021,50(6):565-571.
[5] Richards S,Aziz N,Bale S,et al.Standards and guidelines for the interpretation of sequence variants:a joint consensus recommendation of the American College of Medical Genetics and Genomics and the Association for Molecular Pathology[J].Genet Med,2015,17(5):405-424.
[6] Richards CS,Bale S,Bellissimo DB,et al.ACMG recommendations for standards for interpretation and reporting of sequence variations:revisions 2007[J].Genet Med,2008,10(4):294-300.
[7] Li MM,Datto M,Duncavage EJ,et al.Standards and guidelines for the interpretation and reporting of sequence variants in cancer:a joint consensus recommendation of the Association for Molecular Pathology,American Society of Clinical Oncology,and College of American Pathologists[J].J Mol Diagn,2017,19(1):4-23.
[8] National Comprehensive Cancer Network.Ovarian cancer including fallopian tube cancer and primary peritoneal cancer.Version 1.2021[EB/OL].[2021-02-26].
[9] 中华医学会妇科肿瘤学分会.卵巢癌PARP抑制剂临床应用指南[J].中国医学前沿杂志(电子版),2020,12(5):29-37.
[10] 《基于下一代测序技术的BRCA1/2基因检测指南(2019版)》编写组,中华医学会病理学分会.基于下一代测序技术的BRCA1/2基因检测指南(2019版)[J].中华病理学杂志,2019,48(9):670-677.
 妇产科在线APP下载
妇产科在线APP下载












