PARP抑制剂是针对聚腺苷二磷酸核糖聚合酶的靶向治疗,有助于延长患者生存期。本例患者为卵巢高级别浆液性腺癌,初始治疗时仅接受手术治疗而未化疗,时隔1年就发现复发,给予TC方案化疗+PARP抑制剂维持治疗,基因检测为BRCA阴性。2年后又复发,给予二次减瘤术,并已接受TC方案化疗2程,那么下一步治疗该怎么办呢?PARP抑制剂还能再用吗?

张彦娜 教授
张彦娜,中山大学肿瘤防治中心主任医师、博士后导师,1986年7月毕业于中山医科大学。30余年来,致力于医学教育、医疗及临床科研工作。目前已毕业研究生数十人;连续多年获岭南名医称号。先后发表SCI等专业论著70余篇。目前在研国自然基金两项;在研研究者发起的临床研究一项。作为第二完成人获得2018年度广东医学科学技术一等奖——宫颈癌发生发展的分子机制及预防和治疗的相关研究。
病例介绍
一.基本信息
患者刘某,41岁,G3P3A0,因“卵巢癌术后1年,腹胀2月余”于2018-09-21到中山大学附属肿瘤医院就诊。平素月经规律,初次月经15岁,周期35天,经期7天。
2017-08
因“盆腔包块”行“经腹全宫+双附件切除术”,
术后病理:卵巢高级别浆液性腺癌(分期具体不详)。
术后拒绝化疗。
2018-09-18
复查经阴道超声:盆腔可见多个软组织肿块,考虑卵巢癌复发(具体不详)。
二.妇科检查
外阴:发育正常,已婚式。
阴道:粘膜光滑、通畅,残端可见一结节状肿物,大小约3*2*2 cm,质脆。
盆腔:可触及一大小约9*8*8 cm的肿物,活动度差,与周围分界不清。
肛查:盆腔肿物压迫直肠,直肠粘膜光滑,指套退出无血污。
三.辅助检查
2018-9-21
CA125:317.4 U/ml,HE4:287 pmol/L,CA153:45.66 U/ml,CA724:70.95 U/ml,NSE:28.94 ng/ml。其余常规、生化、止凝血、ECG均无明显异常。
2018-9-25
我院PET-CT提示:卵巢癌术后,阴道残端病灶代谢活跃,考虑复发;右内乳区及横膈上数个淋巴结代谢活跃,考虑转移; 腹盆腔腹膜(包括大网膜、肝脾包膜、肠系膜等)多发病灶代谢活跃,考虑转移,部分病灶累及邻近肝组织/肠管/胃壁;肝脾包膜下积液,盆腔少量积液。
四. 一线化疗
补充化疗:
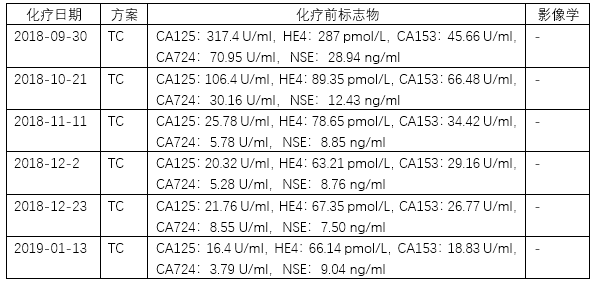
(点击图片可放大查看)
2019-01-22复查PET-CT提示:
1、复发性卵巢癌化疗后:阴道残端代谢未见异常,横膈上多个小淋巴结代谢未见异常,结合病史,考虑治疗后改变;腹盆腔腹膜稍增厚,见多发条索、小结节影,部分代谢略活跃,疑治疗后改变,残留待排;肝包膜下积液;与 2018-09-25 PET/CT 比较,较前明显好转。
2、双上颈及双腋窝多个小淋巴结代谢略活跃,疑炎性病变。
3、胆囊小结石。
4、全身骨髓代谢略活跃,疑反应性改变。
五.维持治疗
基因检测:未检出已知致病或疑似致病突变。

于2019-02-26起口服奥拉帕利300 mg Bid维持治疗:
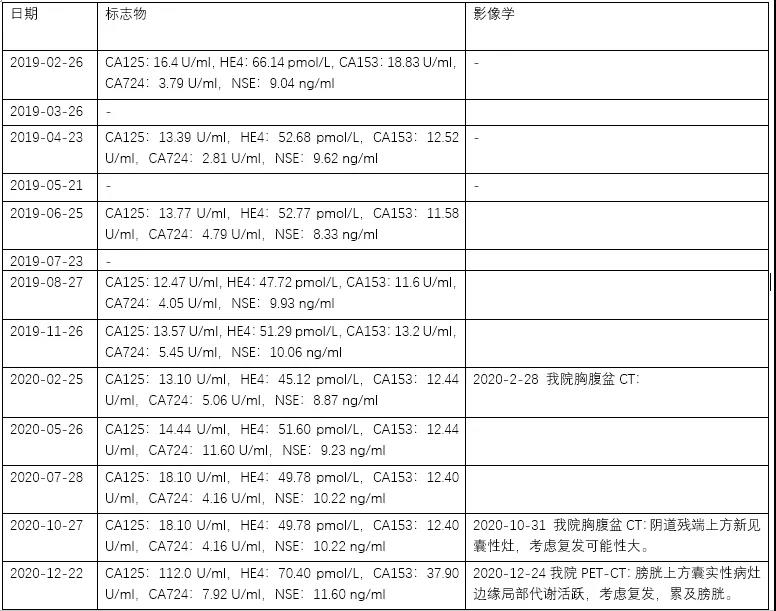
(点击图片可放大查看)
随访CT:
2020-02-28 复查胸腹盆CT影像诊断:
复发性卵巢癌化疗后,阴道残端未见异常。右肺中叶、左肺上叶少许纤维灶。腹部未见异常。
2020-10-31 复查胸腹盆CT影像诊断:
复发性卵巢癌化疗后,对比2020-02-28CT影像,可见:
阴道残端上方新见囊性灶,考虑复发可能大。双侧髂血管旁数个小淋巴结。右肺中叶、左肺上叶少许纤维灶。胆囊小结石。
2020-12-24复查PET-CT提示:
1、复发性卵巢癌术后化疗后:膀胱上方囊实性病灶边缘局部代谢活跃,考虑复发,累及膀胱、盆腔少量积液;
2、筛窦炎症;
3、双颈 I~III 区多个小淋巴结代谢略活跃,考虑炎症;
4、右上肺及右中肺纤维增殖灶。5、胆囊结石。

六.二次减瘤术
2020-12-30 全麻下行盆腔巨大肿物切除+阴道部分切除+盆腔粘连松解+膀胱全切+回肠导管+双侧输尿管粘连松解+小肠部分切除术。
(一)腹部探查情况
腹水:有颜色:血性,性状浑浊,200ml。
横膈、肝、胆、胰、脾、肾(L,R)、胃、结肠、小肠、直肠、腹膜未见明显异常,大网膜术后缺如。
(二)淋巴结探查情况
腹主动动脉旁:无肿大
盆腔:无肿大
其他:无
(三)盆腔探查情况
子宫:术后缺如
盆底可见一囊性肿物 5*6 cm大小,表面灰白,尚光滑,紧贴膀胱后壁及直肠前壁。
术后病理诊断:
冰冻后石蜡(盆腔肿瘤囊壁)镜下:增生的纤维组织中见少许核稍大的细胞小巢状排列,细胞退变明显,伴炎症细胞浸润,结合病史及免疫组化结果,符合腺癌,伴治疗后改变。
1.(阴道残端)未见癌。
2.(盆腔肿物)镜下:平滑肌及纤维组织中见腺癌浸润,结合病史及免疫组化结果,符合高级别浆液性癌;膀胱粘膜慢性炎。
3. (部分小肠1)镜下:肠壁浆膜层见腺癌浸润,结合病史,符合高级别浆液性癌。
4.(部分小肠2)镜下:肠壁浆膜层出血、水肿,伴多量中性粒细胞细胞浸润;未见癌。
免疫组化:
CK(AE1/AE3)(+),CK7(+),p53(-,突变型),Pax-8(+),WT1(+)。
二线化疗:

(点击图片可放大查看)
病例小结
本例患者2017-08因“盆腔包块”行“经腹全宫+双附件切除术”,术后病理为卵巢高级别浆液性腺癌,未行化疗。2018-09-18复查经阴道超声显示盆腔可见多个软组织肿块,考虑卵巢癌复发(具体不详)。
2018-09-21因“卵巢癌术后1年,腹胀2月余”来我院就诊。查CA125:317.4 U/ml,HE4:287 pmol/L,CA153:45.66 U/ml,CA724:70.95 U/ml,NSE:28.94 ng/ml。其余血常规、生化、止凝血、ECG均无明显异常。2018-09-25 PET-CT提示阴道残端病灶代谢活跃,考虑复发;右内乳区及横膈上数个淋巴结代谢活跃,考虑转移; 腹盆腔腹膜(包括大网膜、肝脾包膜、肠系膜等)多发病灶代谢活跃,考虑转移,部分病灶累及邻近肝组织/肠管/胃壁;肝脾包膜下积液,盆腔少量积液。
2018-09-30至2019-01-13给予TC方案补充化疗6程。第6次化疗前检查CA125:16.4 U/ml,HE4:66.14 pmol/L,CA153:18.83 U/ml,CA724:3.79 U/ml,NSE:9.04 ng/ml。
2019-01-22复查PET-CT提示:
1、复发性卵巢癌化疗后:阴道残端代谢未见异常,横膈上多个小淋巴结代谢未见异常,结合病史,考虑治疗后改变;腹盆腔腹膜稍增厚见多发条索、小结节影部分代谢略活跃,疑治疗后改变,残留待排;肝包膜下积液;与 2018-09-25 PET/CT比较,较前明显好转。
2、双上颈及双腋窝多个小淋巴结代谢略活跃,疑炎性病变。
3、胆囊小结石。
4、全身骨髓代谢略活跃,疑反应性改变。患者基因检测未检出已知致病或疑似致病突变。
为了延缓复发,于2019-02-26起口服奥拉帕利300 mg Bid维持治疗。
2020-12-24 PET-CT显示膀胱上方囊实性病灶边缘局部代谢活跃,考虑复发,累及膀胱。由于PFS接近2年,诊断为铂敏感复发卵巢癌,且病灶较局限,具有达到R0切除的潜力,符合二次减瘤术指征。于2020-12-30全麻下行盆腔巨大肿物切除+阴道部分切除+盆腔粘连松解+膀胱全切+回肠导管+双侧输尿管粘连松解+小肠部分切除术手术,手术达到R0。2021-01-11至2021-02-01,TC方案化疗两程,现等待下一步治疗。
余志英教授点评

余志英 教授
余志英教授、主任医师、硕士研究生导师、博士后合作导师,深圳大学第一附属医院(深圳市第二人民医院)妇科主任、教研室主任。
中华医学继续教育委员会妇产科专业委员会委员,中国老年保健协会老龄化社会支持专业委员会委员,广东省医学会妇产科学分会委员,广东省医学会计划生育学分会第五届委员会委员,广东省医师协会妇产科医师分会委员,广东省抗癌协会妇科肿瘤专业委员会委员,广东省健康管理学会妇产科专业委员会常务委员,深圳市医师协会妇科肿瘤专业委员会第一届委员会副主任委员,深圳市抗癌协会妇科肿瘤专业委员会副主任委员,深圳市医学会妇产科专业委员会妇科肿瘤学组副组长。
从事妇产科临床及科研教学工作三十年,曾赴德国访问学习,对妇产科常见病、多发病、疑难病的诊治有丰富的经验。主要研究方向:妇科恶性肿瘤的发病机制及防治,擅长妇科微创手术。现担任深圳大学、汕头大学、安徽医科大学教授、研究生导师,近年来先后参与及主持了国家、省、市科研项目10余项,发表论文三十余篇,其中SCI 9篇,获得全国妇幼健康科学技术成果奖一等奖。
卵巢癌是指发生在卵巢的恶性肿瘤性疾病,原发于输卵管和腹膜的恶性肿瘤临床特征和治疗模式与卵巢癌相似。卵巢癌可发生于任何年龄,其组织学类型多样,上皮性肿瘤最为常见,约占90%以上。而在上皮性卵巢癌中,又以 高级别浆液性卵巢癌最为常见,约占70%。
高级别浆液性卵巢癌是一种显示浆液性分化的高级别上皮性肿瘤,病理分化比较差,更容易发生侵袭和转移,超过95%患者就诊时已有卵巢外疾病。其治疗原则为以手术为主,辅助化疗,强调综合治疗,5年中位生存率介于15%~55%之间,分期和肿瘤减灭程度是主要预后因素。
对于新诊断患者,推荐由妇科肿瘤医生实行全面的分期手术或者肿瘤细胞减灭术,手术的目的,不仅是彻底切除肿瘤,而且要确认有无远处的微小病变,以界定分期,因为远处病变的存在就不再是早期。卵巢癌盆腔或腹主动脉旁淋巴结转移,并不少见。FIGO分期早期的卵巢癌淋巴结转移率13%-38%,1976年开始,FIGO主张卵巢癌手术病理分期,其在临床诊断、治疗和预后判断中起着极其重要的作用。因此,淋巴结切除术一直被认为是关键的分期步骤。具体术式包括子宫切除术、双侧输卵管卵巢切除术、大网膜切除术、细胞学、腹膜活检以及盆腔和腹主动脉旁淋巴结切除术。
关于早期卵巢癌淋巴结切除范围,ESGO(欧洲妇科肿瘤学会,2013)指南建议,双侧盆腔和腹主动脉旁淋巴结切除达到左肾静脉水平(I期膨胀型黏液性癌除外)(B级)。而2020年第一版NCCN卵巢癌指南共识,双侧盆腔和腹主动脉旁淋巴结切除至少达到肠系膜下动脉水平,最好达到肾血管水平。
总之,临床早期卵巢癌患者,淋巴结的分期手术,对指导后续治疗以及减少复发转移是有帮助的。
对于术后辅助化疗,欧洲的ICON1临床试验经过长期观察证实了辅助化疗对早期卵巢癌患者的无复发生存率和总生存率有长期疗效。研究共纳入早期上皮性卵巢癌477例,随访10年,总生存率改善了9%,无复发生存率改善了10%,特别是高危患者的总生存率改善了17%,无复发生存率改善了22%,但不除外辅助化疗对中、低危患者具有较小益处。
2019年NCCN指南第四版中讲到,大多数上皮性卵巢癌、输卵管癌和原发性腹膜癌患者术后需接受全身化疗。全面分期手术后低级别(G1)的ⅠA 期 或ⅠB 期的患者,可行临床观察,单纯手术治疗的存活率>90%,IA、IB期/G2的患者可选择观察随访或化疗。其余患者均应行辅助化疗,化疗方案为以铂类为基础的化疗。妇科肿瘤组(GOG)-157研究发现,3个疗程卡铂+紫杉醇化疗的效果与 6个疗程相同;但分层分析发现,对于高级别浆液性癌患者,6个疗程效果可能更佳(FIGO,2018)。
本例患者初次就诊仅进行了“经腹全宫+双附件切除”,未进行全面的分期手术,可能残留微小病变或远端病变。此外,在病理结果为高级别浆液性腺癌的情况下,也未给予规范的化疗,是患者术后时隔一年就复发的可能原因。而卵巢癌一旦复发,就意味着更容易发生耐药,含铂化疗的疗效逐渐下降,导致预后不佳。本例患者复发后,给予了规范的紫杉醇+卡铂(TC)方案6个疗程,并且给予了奥拉帕利维持治疗,22个月后再次复发,相比首次复发间隔延长了一倍。但若患者初次治疗更加规范,相信复发间隔会进一步延长,为患者带来更长久的生存获益。
因此,卵巢癌的初始治疗仍应以规范的手术为主,化疗为辅,结合新兴的靶向药物如PARP抑制剂的维持治疗,来延缓复发,延长生存。
潘跃银教授点评

潘跃银 教授
潘跃银教授,中国科学技术大学附一院主任医师,教授,博士生导师,博士后指导老师,江淮名医。
115产业团队带头人,肿瘤教研室主任,安徽省肿瘤医院副院长,药物临床研究机构执行主任,安徽省肿瘤质量控制中心副主任,任中国临床肿瘤协会(CSCO)理事,CSCO转化医学专委会副主任委员,CSCO心脏安全专委会副主任委员,CSCO肺癌专家委员会常委,CSCO乳腺癌专家委员会常委,中国医师学会肿瘤分会全国委员,中国医师学会肿瘤多学科专委会常委,国家癌症中心乳腺癌专家委员会成员,安徽临床肿瘤学会理事长,安徽省抗癌协会副理事长,中国临床肿瘤协会(CSCO)免疫专家委员会委员等,安徽省医学会乳腺病分会侯任主任委员,安徽省抗癌协会乳腺癌专委会主任委员等,获安徽省科技进步一等奖,以第一或通讯作者发表SCI50余篇,包括Nature cell biology、 ACS NANO、JTO、CCR等。
卵巢癌是病死率最高的妇科恶性肿瘤,70%的卵巢癌患者就诊时已是临床晚期。卵巢癌首选治疗模式为肿瘤细胞减灭术联合以铂类为基础的化疗。虽然大多数患者经过初始治疗可获得临床缓解,但仍有70%的患者在3年内复发,5年生存率不足50%。近年来,PARP抑制剂的问世为卵巢癌的治疗带来了重大变革,一系列高级别循证医学证据表明在初始治疗或铂敏感复发治疗获得完全缓解(CR)和部分缓解(PR)后应用PARP抑制剂可显著延长卵巢癌患者的无进展生存(PFS)时间,维持治疗已成为卵巢癌治疗的新模式。
奥拉帕利是“first-in-class”PARP抑制剂,基于“合成致死”原理,通过阻断携带同源重组缺陷(HRR)的肿瘤细胞的DNA损伤修复反应,在杀伤肿瘤细胞的同时,让健康细胞免受伤害,是全球首个获批用于卵巢癌维持治疗的PARP抑制剂。
SOLO 1研究是一项随机、双盲、安慰剂对照、多中心的Ⅲ期临床研究,用于评估与安慰剂相比,奥拉帕利(300mg bid))作为一线单药维持治疗在新诊断BRCA1/2m突变的高级别浆液性或子宫内膜样卵巢癌患者中的疗效和安全性。
其在2018年ESMO大会上公布的数据显示,奥拉帕利能够显著改善患者的PFS,降低疾病进展或死亡风险达70%(HR=0.3,95%可信区间为0.23~0.41,P<0.0001),研究数据具有临床相关性和统计学意义。次要终点PFS2中,奥拉帕利组同样有显著性获益。该结果证实奥拉帕利在显著延长一线PFS的同时,不会影响患者后续治疗中的获益。由此,2018年12月,奥拉帕利凭借SOLO1研究成为首个获批用于卵巢癌一线维持治疗的PARP抑制剂。


2020年ESMO大会上,SOLO 1研究5年随访结果公布,研究结果显示中位随访5年后,奥拉帕利的中位PFS值长达56个月,而安慰剂组仅为13.8个月,维持治疗组将PFS延长了42.2个月,奥拉帕利相比于安慰剂可以降低67%的疾病进展或死亡风险(HR 0.33)。奥拉帕利组48%的患者5年无疾病进展,而安慰剂组仅为21%,这说明奥拉帕利一线维持治疗可使近一半的BRCAm患者长期获益,这部分患者可能已经实现了临床“治愈”。
需要注意的是,虽然SOLO 1研究的随访时间是5年,但奥拉帕利组的中位治疗时间仅为24.6个月,这说明奥拉帕利的PFS获益在2年治疗结束后依然可以长期持续。超过半数基线时化疗为CR随后接受奥拉帕利2年维持治疗的患者,5年后疾病依然未复发。研究同时显示,奥拉帕利组的中位PFS2和中位TSST还未达到终点,而安慰剂组分别为42.1个月及40.7个月。这说明奥拉帕利维持治疗的获益可以持续,并未受到后续化疗的影响。
SOLO 1研究已证实,奥拉帕利在BRCAm卵巢癌中取得前所未有的PFS获益。然而,临床中仅有17%~25%的卵巢癌携带BRCA1/2基因突变。PAOLA-1研究正是为了在一线接受含贝伐珠单抗标准治疗的晚期卵巢癌患者中(无论BRCA突变状态如何)评估PARP抑制剂疗效和安全性的Ⅲ期研究。2019年ESMO大会报道的首次数据显示,奥拉帕利+贝伐珠单抗组对比单药贝伐珠单抗可显著改善患者PFS(22.1 vs 16.6个月,HR=0.59;95%CI:0.49~0.72;P<0.0001),其中HRD阳性患者获益显著,中位PFS达到37.2个月,较贝伐单抗单药组延长近20个月。而在PAOLA-1研究中,入组的HRD阳性患者占研究总人群的50%,奥拉帕利的获益人群从 BRCA突变患者扩大到HRD阳性人群,并维持了良好的安全性。
另一项针对既往接受过二线及以上含铂方案治疗的non-gBRCAm PSR卵巢癌患者采用奥拉帕利单药维持治疗的单臂、Ⅲb期临床研OPINION研究,中期数据分析显示:奥拉帕利可延长non-gBRCAm患者的PFS和TFST,mPFS为9.2个月,6个月PFS比例65.6%,12个月PFS比例37.0%,中位TFST13.4个月;奥拉帕利在各亚组中均有效,无论HRD/BRCA突变状态,HRD阳性(含sBRCAm) 亚组mPFS 10.9个月,HRD阳性(不含sBRCAm)亚组mPFS 9.7个月,sBRCAm亚组mPFS 14.5个月,HRD阴性亚组mPFS 7.3个月。研究结果进一步完善并夯实了奥拉帕利在BRCA突变阴性PSR卵巢癌患者中的显著临床获益。
本例患者不具有BRCA突变,一线化疗后接受奥拉帕利维持治疗PFS达22个月,相较自然病史一线PFS(18.2个月)显著延长且无铂间期超过6~12个月,为铂敏感复发(PSR)。对于PSR患者,PARP抑制剂维持治疗已成为标准治疗,不论BRCA是否突变。尽管本例患者一线化疗后已经使用过PARP抑制剂,但依据SOLO 1研究,奥拉帕利维持治疗不影响后续治疗获益,并且获益能够持续,结合OPINION研究结果,患者完成二线化疗后,或可继续使用奥拉帕利进行维持治疗。
 妇产科在线APP下载
妇产科在线APP下载












