子宫内膜癌是女性生殖道三大常见恶性肿瘤之一。晚期子宫内膜癌患者常常发生复发转移,治疗困难,5年生存率仅20%左右,预后很差。近年来研究表明,以PD-1抑制剂为代表的免疫疗法用于晚期子宫内膜癌患者显示出了良好的治疗效果。该例晚期子宫内膜癌患者在根治术及放化疗后复发进展,出现全身多发淋巴结转移,应用PD-1抑制剂替雷利珠单抗治疗,病情达到完全缓解,显示出替雷利珠单抗治疗晚期和复发性子宫内膜癌患者的良好疗效。

王冬 主任医师
重庆大学附属肿瘤医院妇科肿瘤中心教研室主任,硕士生导师
中国抗癌协会妇科肿瘤专业委员会常务委员,中国优生科学协会肿瘤生殖学分会常务委员,CSCO妇科肿瘤专家委员会委员,国家癌症中心宫颈癌质控专家委会委员,重庆抗癌协会妇科肿瘤专业委员会常务委员,重庆市医学会妇产科专委会副主任委员,重庆医学会妇产科专委会妇科肿瘤学组组长,重庆市肿瘤质量控制中心专家委员会委员,2010年度全国医药卫生系统先进个人。
病例诊疗经过
一、病例介绍
1、基本情况
患者,女,56岁,G3P1,体重指数(BMI)25.2 kg/m2
主诉:不规则阴道流血半年,2018.12就诊本院
其他病史:无异常
2、妇科检查
宫颈常大,光滑;双侧宫旁弹性好;子宫前位,饱满,活动,无压痛;双附件区未扪及明显肿物。
3、病理会诊
第一次诊刮病理会诊:(宫腔)符合子宫内膜样癌,局部见透明细胞癌成份;ER(+)40%~50%,PR(+)40%,Vimentin部分(+),Ki-67(+)30%~40%,p53(-),p16(+),CEA(-),CK7部分(+),CA125(+),WT-1(-),CK20(-),HNF1β(+),NapsinA(+),p504S部分(+)。
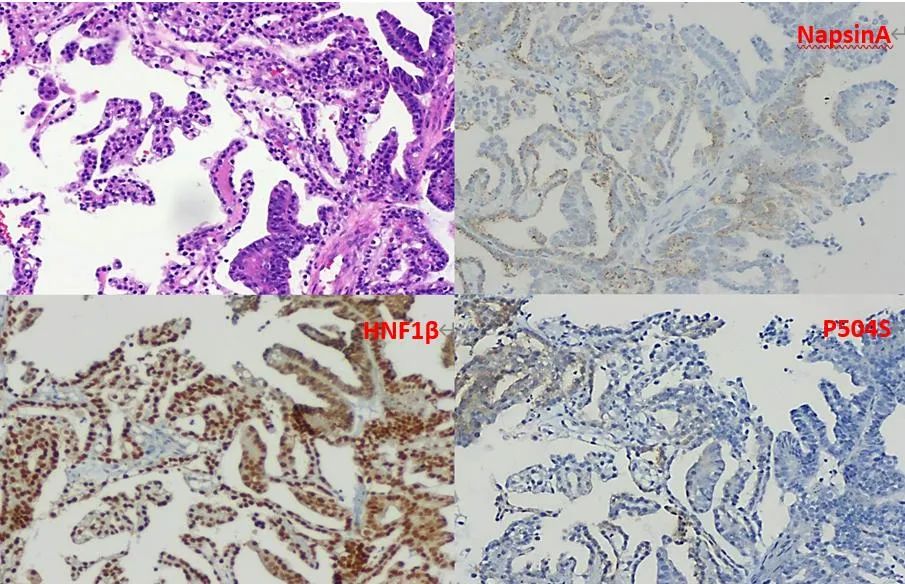
4、入院后检查
(1)实验室检查
CA125:36.8 U/ml;CA199:102.9 U/ml;血糖正常。
(2)超声检查
双下肢深静脉未见静脉血栓、全身浅表淋巴结未见肿大、双乳检查未见异常。
(3)盆腔及腹部MRI检查
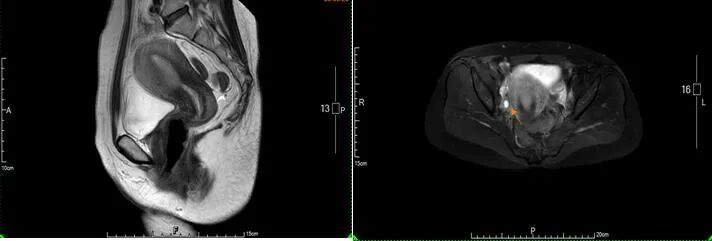
①子宫内膜增厚,侵及肌壁深度<1/2,考虑子宫内膜癌;②宫颈粘膜稍增厚;③右侧附件区囊性结节,性质待定;④双侧髂血管旁肿大淋巴结,直径<10 mm;⑤盆腔少量积液。
(4)PET-CT检查
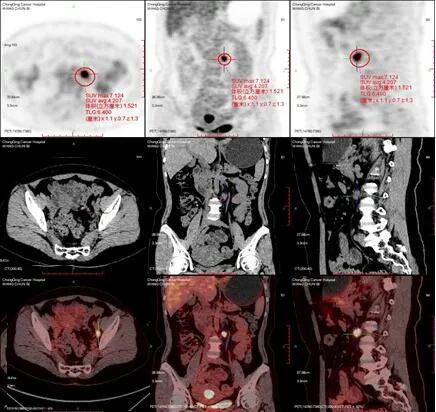
主要阳性发现:
①子宫内膜区团片状代谢增高,符合子宫内膜癌表现;②双侧髂血管旁、腹主动脉旁代谢增高淋巴结,考虑肿瘤转移;③双附件增大伴代谢不均,宫颈及阴道代谢稍显不均,考虑生理性改变可能; ④右肺中下叶及左肺上叶舌段少许慢性炎症,双肺下叶胸膜下少许局限性气肿。
(5)宫颈管刮术:未见肿瘤细胞
(6)宫颈刷片(TCT):无上皮内病变或恶性病变细胞(NILM)
初步诊断
子宫内膜样癌III期
二、初始治疗(手术+放化疗)
1、手术(2018.12)
行淋巴结标记+手术机器人辅助下盆腔淋巴结/腹主动脉旁淋巴结清扫+大网膜切除+筋膜外全子宫双附件切除(免举宫器)。
术中见腹腔内无腹水,肝脾膈顶未见异常;子宫饱满,双附件无明显肉眼异常;右侧髂外淋巴结1.5 cm*1.0 cm,质中,见荧光;左侧闭孔淋巴结2.5 cm*1.5 cm,腹主动脉右旁见1.5 cm*1.0 cm淋巴结;余腹主动脉旁及盆腔淋巴结未见肿大,未见荧光阳性。
2、术后病理
(1)全子宫双附件切除标本:(宫腔)低分化子宫内膜样癌(FIGO3级),伴部分透明改变,肿瘤大小4 cm*3.5 cm*1.5 cm,浸润至浆膜层,累及颈管内口内膜;未见神经侵犯;双宫旁及阴道切缘净;左侧卵巢见小灶癌累及,最大径约1 mm。
(2)(大网膜)脂肪中未见癌累及。
(3)(区域淋巴结)见癌转移(4/26):左髂总淋巴结0/3,右髂总淋巴结0/2,左盆腔淋巴结2/6,右盆腔淋巴结2/9,腹主动脉旁淋巴结0/6。
(4)(腹腔冲洗液):未见癌细胞。
(5)免疫组化:<19-19176-47宫腔肿块>HNF1β(-),NapsinA(-),p504S(-),Vimentin(-),P53(少量细胞+),β-catenin(+),GATA3(-)。耐药基因:TOPOⅡ耐药基因蛋白(+)25%~50%,MDR-1耐药基因蛋白(+),LRP耐药基因蛋白(+),GST-π耐药基因蛋白(+),P53(少量细胞+),ki-67约70%(+);错配修复蛋白-dMMR:MLH1(核-),MSH2(核+),MSH6(核+),PMS2(核-)。

病理诊断:子宫内膜混合性癌(子宫内膜样癌FIGO3级约95%,透明细胞癌约5%)
3、基因检测
MSI:微卫星高度不稳定(MSI-H);TMB结果:35.52 Muts/Mb。
4、术后诊断
子宫内膜混合性癌IIIC1期(MSI-H型)
5、术后辅助治疗(2019.01-2019.05)
(1)术后盆腔外照射
(2)TC方案化疗:紫杉醇175 mg/m2+卡铂AUC 5,iv,6疗程。
(3)放疗:TOMO,范围包括阴道残端、部分阴道+阴道旁、原双宫旁、淋巴引流区,剂量PTV 45 Gy/25F。
6、治疗结束时(2019.06)
全腹盆腔MRI检查:未见异常。
CA125:正常。
7、疗效评估
2019年治疗结束疗效评价:完全缓解(CR)
三、复发诊断
2020.03定期随访,检查结果如下。
1、CA125:18.9 U/ml
2、CT检查:(1)腹膜后主动脉旁多发肿大淋巴结,最大淋巴结短径为15.2 mm,考虑肿瘤转移;(2)右肺上叶及左肺下叶磨玻璃结节,左肺下叶结节较前为新增,炎性?(3)右肺下叶后基底段小结节,较前无变化。
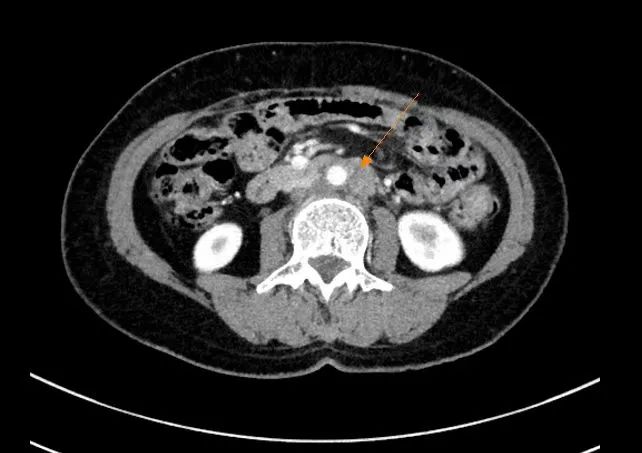
3、PET-CT检查:(1)子宫内膜癌术后改变;(2)左侧锁骨上区、右侧膈脚后、腹主动脉旁淋巴结代谢增高,考虑肿瘤转移;(3)双侧颈部多发淋巴结反应性增生;(4)右肺上叶类圆形磨玻璃结节,考虑炎性病变可能。
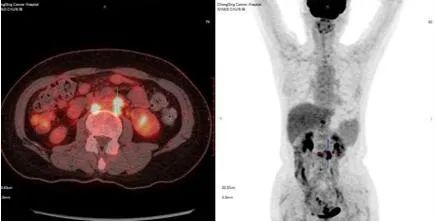
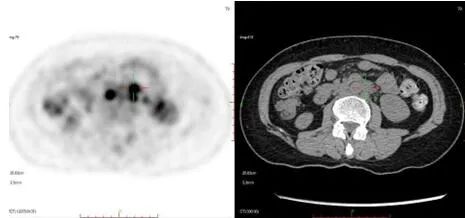
4、ECOG评分:1分。
5、诊断:子宫内膜混合性癌IIIC1期术后复发
四、复发后治疗
1、入组临床试验(BGB-A317-209)
经筛选,符合入组条件,参加“一项在既往经治的局部晚期不可切除或者转移性MSI-H或者dMMR实体肿瘤患者中评估抗PD-1单克隆抗体(BGB-A317)单药的有效性和安全性临床研究”,患者参加临床试验。
2、治疗过程
2020.04入组BGB-A317-209研究。
2020.04.27开始替雷利珠单抗(Tislelizumab)注射液200 mg治疗,每3周一次,末次治疗2022.04.29,共计治疗36次。
主要副反应:药物性肝损害(轻度)。
3、疗效随访
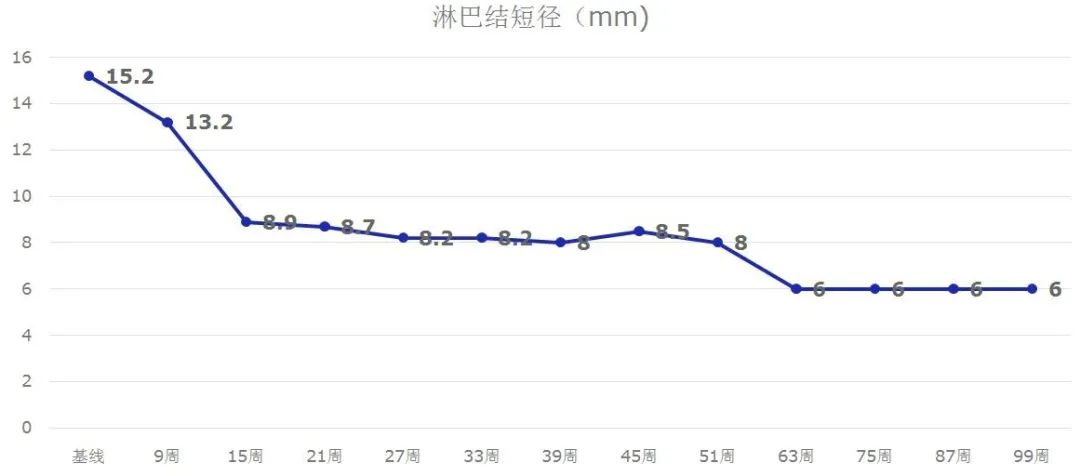
靶病灶(腹膜后淋巴结短径)缩小60.5%。
靶病灶影像学对比
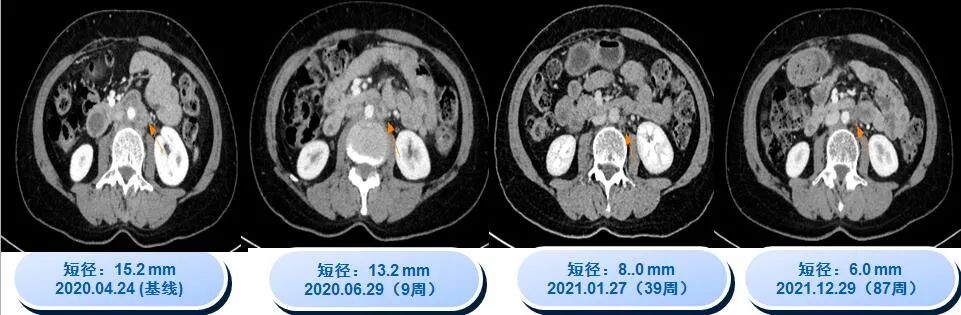
疗效评估:CR
治疗期间患者一般情况可,大小便正常,体重无明显改变;其他电解质、心电图等相关检查均正常,治疗过程中未出现免疫相关的不良反应。
治疗小结
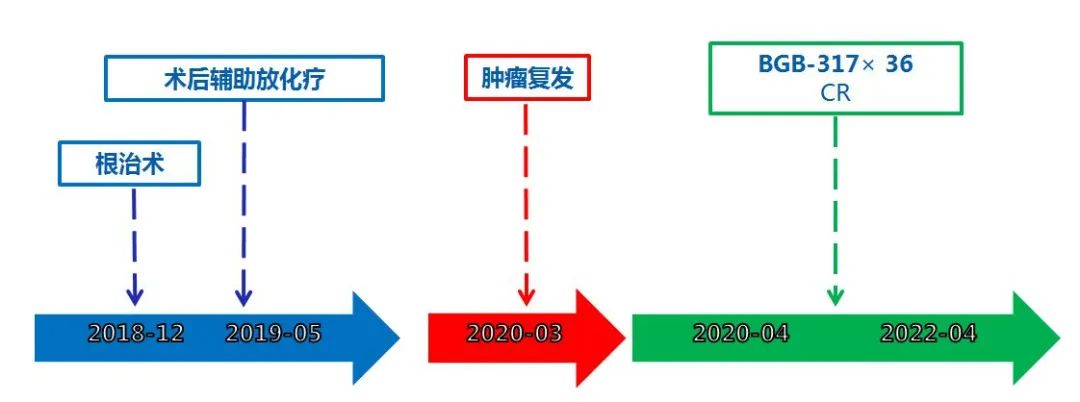
子宫内膜混合性癌(G3)IIIC1期患者,经过根治性手术,术后辅助紫杉醇+卡铂6个疗程化疗和放疗,经影像评估达到CR,进入随访阶段。治疗结束9个月,随访检查发现,患者病情出现新的进展,CT和PET-CT检查示腹膜后腹主动脉旁等多处淋巴结出现肿瘤转移,诊断子宫内膜癌复发。患者分子分型为MSI-H,放化疗后复发,满足进入临床试验的条件,有可能从免疫治疗中获益。该患者遂进入临床试验,开始替雷利珠单抗治疗,治疗后评估达到CR,迄今共计治疗36个周期,CR状态,表明替雷利珠单抗治疗晚期和复发性子宫内膜癌患者疗效良好,耐受性较好。
专家点评

周琦 教授
重庆大学附属肿瘤医院主任医师,教授,二级专技岗,博士生导师
国际妇癌联盟(IGCS)教育委员会委员,全国首席科学传播专家,中国抗癌协会常务理事,中国抗癌协会肿瘤内分泌专委会主任委员,中国抗癌协会妇科肿瘤专委会(CGCS)前任主任委员,中国临床肿瘤学会妇科肿瘤专家委员会副主任委员,全国宫颈癌防治协作组副组长,中国优生优育协会CSCCP副主任委员,中国医疗保健国际交流促进会妇产科专业委员会副主任委员,中华预防医学会肿瘤预防与控制专委会常委,重庆市医师协会肿瘤医师分会会长,重庆市医学(妇科学)首席专家。
主要研究方向为妇科恶性肿瘤放化疗抗性研究,以宫颈癌为代表的癌前病变逆转与干预治疗应用基础研究,肿瘤早期诊断方法研究,肿瘤的个体化基因靶向治疗、免疫治疗相关临床与应用基础研究,肿瘤精准治疗及相关基因诊断研究。擅长妇科恶性肿瘤的手术、放疗和化疗、肿瘤遗传咨询,特别擅长晚期卵巢癌手术及挽救性治疗。公开发表论文150余篇,最高影响因子35.3分。以第一完成人获省部级科技进步二等奖2项,主编及参编著作10部,国家专利2项。
子宫内膜癌在我国居女性生殖系统恶性肿瘤的第2位,据最新数据报告,我国每年新发子宫内膜癌病例7.11万,死亡1.71万,并且有年轻化和发病率上升的趋势。子宫内膜癌患者确诊时大部分为I期,局限于子宫体,早期子宫内膜癌患者手术治疗预后较好,5年生存率可达到90%,但复发和晚期患者的5年生存率仅20%。晚期复发性子宫内膜癌患者面临很大的治疗挑战,有提升治疗效果的临床需求。
近年来分子分型应用于子宫内膜癌患者,有助于指导患者治疗和预后判断。研究表明,在子宫内膜癌患者中,子宫内膜癌分型中微卫星不稳定型和POLE型,具有肿瘤突变负荷较高的特征,有更活跃的肿瘤免疫微环境,对免疫治疗敏感,是PD-1/ PD-L1抑制剂治疗的获益人群。因此,分子分型为优选子宫内膜癌个体化免疫治疗提供了临床依据。子宫内膜癌中MSI-H/dMMR的突变率约占28.3%,MSI-H/dMMR突变的微卫星不稳定型肿瘤作为复发晚期子宫内膜癌免疫治疗的优选人群。
PD-1抑制剂在已经公布的晚期实体瘤患者研究中疗效肯定,多款PD-1抑制剂已经成为晚期实体瘤患者的治疗选择,其优势人群为PD-L1阳性表达或MSI-H以及TMB高表达。KEYNOTE158研究表明,帕博丽珠单抗治疗MSI-H/dMMR晚期复发不可切除的子宫内膜癌患者,肿瘤客观缓解率达到57.1%,中位PFS达到25.7个月,改写了晚期不可切除子宫内膜癌患者治疗的历史,为这些患者的生存带来了获益。
BGB-A317-209研究首次公布了替雷利珠单抗治疗MSI-H/dMMR实体瘤患者的ORR达到45.9%。该研究共纳入13例子宫内膜癌患者,MSI-H/dMMR子宫内膜癌患者的ORR为46.2% (6/13),中位PFS和OS尚未达到,安全性良好。在这13例患者中,有3例达到CR,该例患者即为达到CR的病例之一。该患者迄今已经使用替雷利珠单抗治疗36个周期,仍然维持CR状态,没有不可耐受的毒性反应,疗效明显优于化疗,且生活质量较高。
替雷利珠单抗是PD-1单克隆IgG4抗体,是国产原研药,虽然PD-1抑制剂的作用靶点和抗肿瘤原理相同,但每一种PD-1抑制剂/PD-L1抑制剂有不同的药理特性。替雷利珠单抗的抗体Fab段与PD-1结合位点面大,更大程度地持久阻断PD-1与PD-L1结合,PD-1解离的速率减慢,与PD-1的亲和力高,抑制效率更高。其Fc段的改造消除了抗体依赖的细胞介导的ADCP效应,避免了肿瘤浸润性T细胞数量减少而影响抗肿瘤疗效。促进炎性因子释放和T细胞活化、半衰期长等等药理特性,增强了替雷利珠单抗的抗肿瘤活性。替雷利珠单抗将会使患者能够从免疫治疗中更加获益。
PD-1抑制剂替雷利珠单抗获批MSI-H/dMMR晚期实体瘤患者的适应证,为MSI-H/dMMR型晚期及复发性子宫内膜癌患者的临床疗效提高发挥重要作用,期待后续在子宫内膜癌患者真实世界临床研究中有更多临床疗效优异的证据,为晚期和复发性子宫内膜癌患者提供更多更好的临床治疗选择。我们期待进一步的研究,如为早期高危型子宫内膜癌患者添加免疫治疗以减少复发,免疫治疗用于一线晚期子宫内膜癌患者进一步提高疗效的研究结果问世并应用于临床。
参考文献
1. ScienceDirect [J]. Journal of the National Cancer Center, m5GeSdc; March 9, 2022; 5:38.
2. Nature. 2013 May 2; 497 (7447): 67-73.
3. J Clin Oncol. 2020 Jan 1; 38(1): 1-10.
4. J Li, et al. J Clin Oncol 2021; 39: (15_suppl)2569.
声明:本文仅供医疗卫生专业人士为了解资讯使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解资讯以外的目的,平台及作者不承担相关责任。
 妇产科在线APP下载
妇产科在线APP下载












