
王冬 教授
重庆市肿瘤医院妇科肿瘤中心教研室主任,主任医师,中国抗癌协会妇科肿瘤专业委员会常务委员、中国优生科学协会肿瘤生殖学分会常务委员、北京健康促进宫颈病变与宫颈癌防治专家委员会常务委员、中国抗癌协会家族遗传性肿瘤专委会委员、中国抗癌协会腹膜肿瘤专业委员会委员、重庆抗癌协会妇科肿瘤专业委员会常务委员、重庆市医学会妇产科专委会副主任委员、重庆医学会妇产科专委会肿瘤学组组长,重庆市肿瘤质量控制中心专家委员会委员等,荣获2010年度全国医药卫生系统先进个人。从事肿瘤临床、科研及教学工作20多年,擅长妇科恶性肿瘤的手术、化疗、放疗及综合治疗。主持及参与国家级、省部级课题20余项,主编著作2部,参编著作4部,发表论文30余篇。
病例介绍
初始治疗(PFS 29个月)
主诉
患者江X,女,51岁,因“体检发现CA125增高2+月,B超发现盆腔包块12天”,2015.11.16就诊于外院。
个人史
7+年前开始间断口服戊酸雌二醇片/雌二醇环丙孕酮片复合包装。G2P1,顺产1女,月经史无特殊。
家族史
母亲有原发性腹膜癌病史,于2018年死于腹膜癌。父亲健在,有三位兄妹。
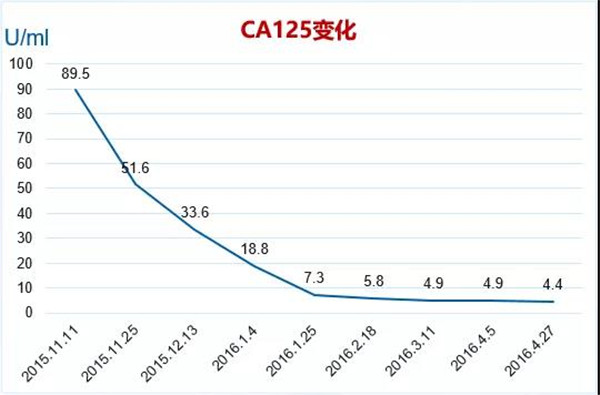
入院前CA125体检情况

妇科查体
外阴、阴道、宫颈、宫体(-)。
左附件区可扪及不规则肿块约4 cm,边界欠清,实性,无压痛。
三合诊:直肠粘膜光滑,指套无血染。
辅助检查
肿瘤标志物
CA125:89.5 U/ml,HE4:72 pmol/L。
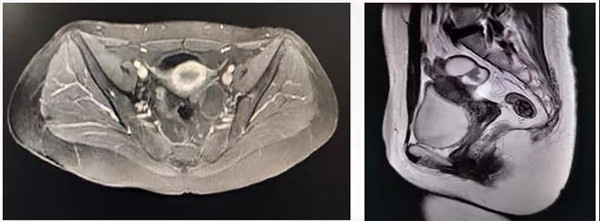
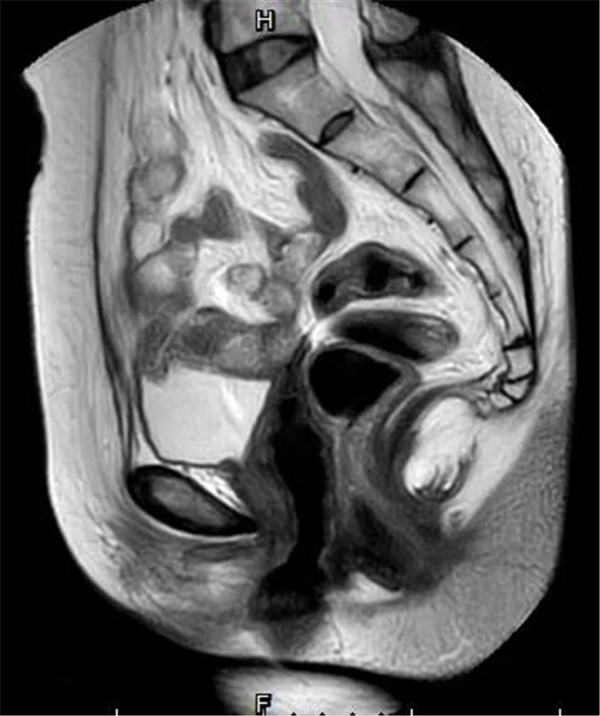
盆腹腔MRI
1. 左侧附件区囊实性占位,59 mm*38 mm,边界清晰,增强后囊壁及实性成分强化明显,考虑良性病变可能性大,囊腺瘤可能。
2. 宫颈小囊肿。
其他
胃肠镜、胸部CT、淋巴结彩超、乳腺彩超无异常发现。
入院诊断
盆腔肿物待查:卵巢囊腺瘤?卵巢子宫内膜异位囊肿?
手术治疗
2015.11.17 全麻下行腹腔镜探查术+全子宫切除+双附件切除+大网膜切除+双侧盆腔淋巴结清扫术。
术中探查
未见腹水,子宫前位,大小约6 cm*4 cm*3 cm,表面光滑,左侧卵巢呈不规则多房囊实性增大,以囊性为主,大小约5 cm*4 cm*3 cm,肿瘤表面局部见实性部分似菜花样突起约0.5 cm,输卵管走行于卵巢表面,稍增粗。右侧卵巢、输卵管外观未见明显异常。探查肠管表面、肝、脾、胃、膈下、大网膜未见明显异常。
术中冰冻病理检查
左卵巢恶性肿瘤。
手术减瘤彻底,无肉眼残留病灶(R0)。
术后病理检查
左卵巢高级别浆液性腺癌,左输卵管见癌组织,左宫旁、右宫旁、骶韧带、大网膜未见癌累及,左侧盆腔淋巴结未见癌转移(0/8),右侧盆腔淋巴结未见癌转移(0/13),慢性宫颈炎伴低级别鳞状上皮内病变,见挖空细胞,老年性子宫内膜,右侧附件。
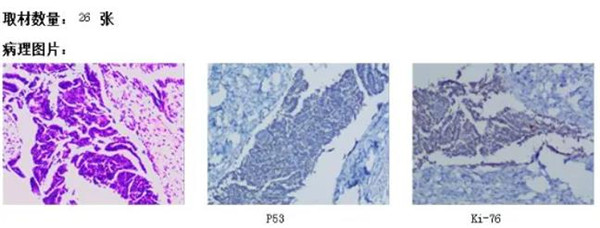
免疫组化
P53:5%+,CK7(+),ER 50%(+),PR(-),WT-1(+),MC(+),CR()-),Ki-67:50%+,CA125(+)。
术后诊断
卵巢高级别浆液性腺癌IIA期
术后辅助化疗
化疗
2015.11.23~2016.04.06,紫杉醇+卡铂静脉化疗6程。化疗期间出现Ⅳ度骨髓抑制,以血小板减少为主,最低水平为18*109/L。
疗效评估
依据实体瘤疗效评价标准(RECIST)评价疗效为CR。
2016.04.27 复查
盆腹腔MRI
1. 子宫及附件缺如,阴道残端未见异常。
2. 腹膜后及盆腔淋巴结未见肿大。
肿瘤标志物
CA125:4.4 U/ml;HE4:97 pmol/l。
规律随访2+年,期间CA125缓慢升高,未超过正常值。
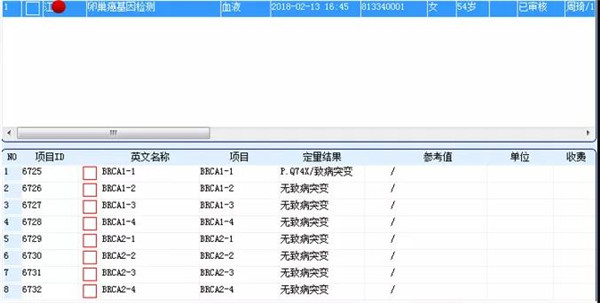
基因检测结果
复发治疗(PFS>24个月)
2018.09.17
肿瘤标志物
CA125:52.1 U/ml;HE4:55.6 pmol/L。
超声造影、活检
1. 超声造影:左锁骨上淋巴结34 mm*27 mm,考虑淋巴M超声造影声像。
2. 左颈中上方、右颈、双颌下、双腋窝、双腹股沟淋巴结肿大:反应性?
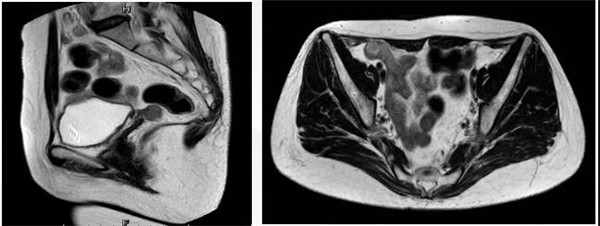
全腹MRI
1. 子宫缺如,阴道残端旁类圆形影,大小约1.8 cm*1.5 cm,强化欠均匀,原因待查,新生物不除外?
2. 左侧腹股沟渗出性病变,注意复查。
3. 腹主动脉旁多发淋巴结显示,较大者短径约0.6 cm,位于左肾门水平略偏下,待除外转移瘤。
2018.09.20
PET-CT
1. 卵巢癌术后改变,阴道断端结节,代谢增高,考虑复发。
2. 左侧锁骨上区、腰3椎体水平腹主动脉旁多发淋巴结肿大,代谢增高,符合淋巴结转移。
3. 鼻咽部代谢增高,考虑为炎性摄取可能性大。请结合临床或除外其他。
4. 双侧颈部、双肺门多发淋巴结,代谢轻度增高,考虑为反应性淋巴结增生。
5. 左肺上叶、双肺下叶多发条索影,考虑为慢性炎症。
6. 双侧肾结石,脊柱退行性改变。
2018.09.25
左锁骨上淋巴结穿刺
发现恶性肿瘤,结合免疫组化染色结果,符合卵巢低分化腺癌转移。
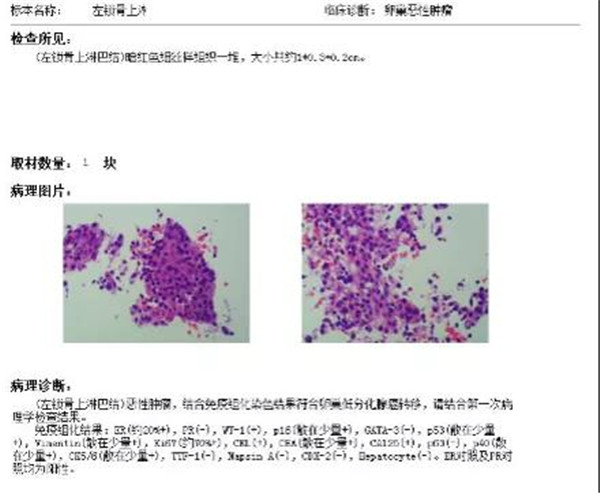
诊断
经MDT(多学科团队)讨论,诊断如下:
1. 左卵巢高级别浆液性腺癌ⅡA期外院术后化疗后铂敏感复发;
2. 阴道残端复发;
3. 左颈部淋巴结转移;
4. 腹主动脉旁多发淋巴结转移。
治疗
2018.09.29~2019.03.23,紫杉醇175 mg/m2+顺铂70 mg/m2方案化疗6程。
螺旋断层放射治疗系统(TOMO)放疗
2019.02.11 开始行TOMO放疗(肿大淋巴结同步加量):使用6MV-X照射。
范围:左锁骨上肿大淋巴结、左锁骨上淋巴引流区。
剂量:PLN(左锁骨上肿大淋巴结)55 Gy/25F(2.2 Gy/F),PTV 45 Gy/25F(1.8 Gy/F)。
第二阶段,肿大淋巴结加量放疗(螺旋断层放疗):使用6MV-X照射。范围:左锁骨上肿大淋巴结。
剂量:PLN(左锁骨上肿大淋巴结)6.6 Gy/3F。
2019.03.20 全部放疗结束。
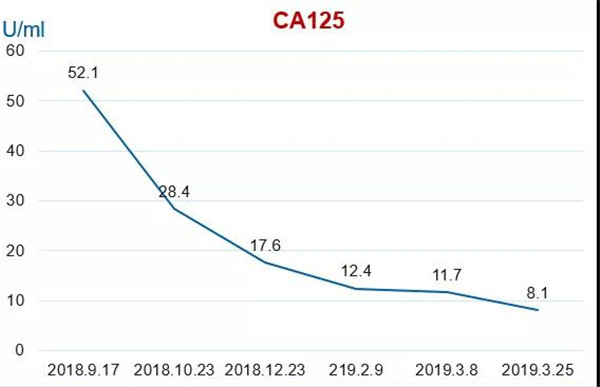
疗效评价
RECIST 评价疗效:PR。
2019.03.22 行颈部及全腹MRI,并与2018.12.20旧片对比:
1. 子宫缺如,阴道残端旁小结节,径约0.5 cm,较之前变化不大。
2. 前片所示左侧腹股沟渗出性病变,本次未见。
3. 腹主动脉旁多发淋巴结显示,较之前缩小,较大者短径约0.5 cm。
4. 双侧颈部 I-IV区未见肿大淋巴结显示,增强扫描未见异常强化。
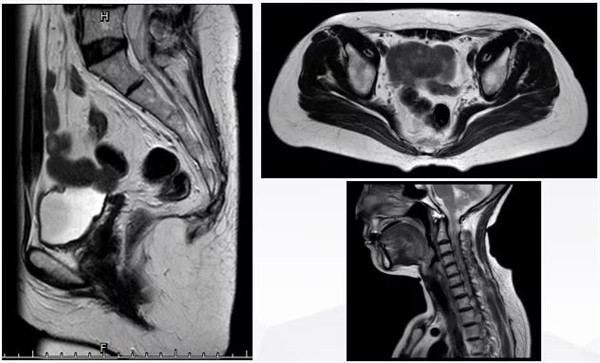
复发后维持治疗
2019.05 开始口服奥拉帕利300 mg bid 维持治疗至今。服药期间曾出现白细胞减少、轻微恶心、食欲下降等副反应。
2020.03.05 行全腹MRI,并与2019.11.17旧片对比:
1. 子宫缺如,阴道残端旁小结节,较前变化不大,径约0.5 cm,随诊。
2. 腹主动脉旁多发淋巴结,较前变化不大,较大者短径约0.3 cm。
3. 左肾小囊肿,余较前变化不大。
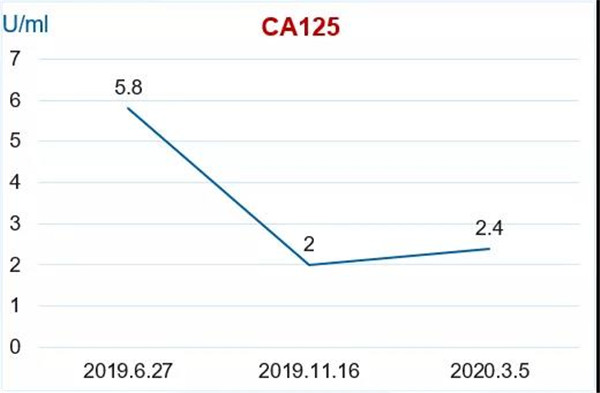
遗传咨询
近亲属g-BRCA检测结果
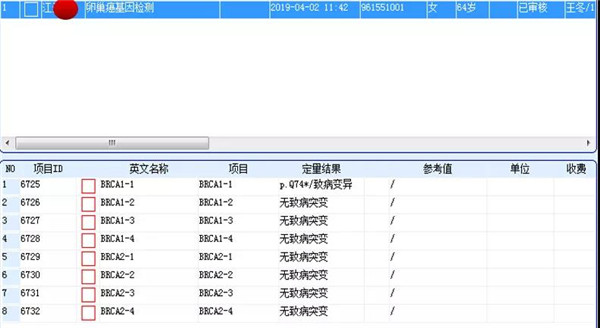
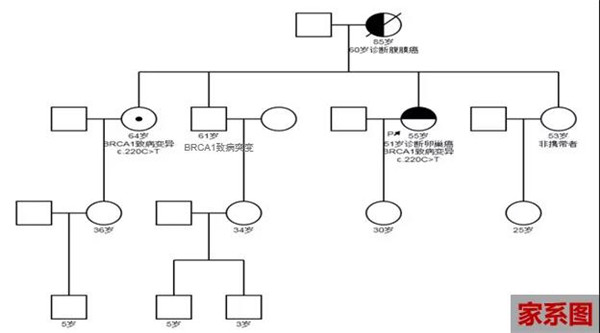
先证者BRCA1致病突变,患卵巢癌。母亲60岁诊断腹膜癌,85岁复发死亡,未行基因检测。
长姐64岁,检测BRCA1致病突变。
长兄61岁,BRCA1致病突变,目前体检未发现异常。
小妹行基因检测未检出相同变异。
咨询建议
1. 携带者和患者的一级血亲行BRCA基因检测;
2. 预防性输卵管卵巢切除;
3. 针对性的定期体检随访(乳腺MRI 等);
4. 参加乳腺癌风险监测的临床研究。
长姐行预防性卵巢输卵管切除术
术前肿瘤标志物正常。
2019.04.24在全麻下行“腹腔镜探查+双侧卵巢输卵管切除术(RRSO)”。术中腹腔冲洗液细胞学阴性。
术后病理检查
1.(右附件)输卵管局灶上皮增生活跃;卵巢组织。
2.(左附件)卵巢及输卵管组织。
免疫组化:PR(-),p16(-),WT-1(+),ER(+)70%,Ki-67(+)1%,p53(-),PAX-8(+),CK7(+),CA125灶(+)。
病例小结
本例患者于2015.11.16因“体检发现CA125增高2+月,B超发现盆腔包块12天”就诊于外院。入院前体检CA125为89.5 U/ml,盆腹腔MRI 发现盆腔肿物待查。2015.11.17全麻下行腹腔镜探查术+全子宫切除+双附件切除+大网膜切除+双侧盆腔淋巴结清扫术。手术减瘤彻底,无肉眼残留病灶(R0)。术后诊断卵巢高级别浆液性腺癌IIA期。
于2015.11.23至2016.04.06,紫杉醇+卡铂静脉化疗6程。化疗期间出现Ⅳ度骨髓抑制的不良反应,以血小板减少为主,最低水平为18*109/L。2016.04.27复查盆腹腔MRI 未见异常,CA125为4.4 U/ml,HE4为97 pmol/l。RECIST疗效评价为CR。根据2016年NCCN指南建议,卵巢癌II期治疗达到CR后,可考虑入组临床试验观察,使用帕唑帕尼或紫杉醇巩固治疗。经过充分沟通,患者选择观察,规律随访2+年,期间CA125缓慢升高,未超过正常值。

卵巢癌NCCN指南2016年第一版
2018.02.13患者检出BRCA1致病突变。2018.09.17复查发现肿瘤标志物CA125持续升高至52.1 U/ml,HE4达到55.6 pmol/L,MRI 未见明显的异常。2018.09.20行PET-CT检查发现复发和转移,2018.09.25左锁骨上淋巴结穿刺符合癌转移。此时,距离患者末次含铂化疗结束已有29个月。
经MDT(多学科团队)讨论,诊断如下:
1. 左卵巢高级别浆液性腺癌ⅡA期外院术后化疗后(铂敏感复发);
2. 阴道残端复发;
3. 左颈部淋巴结转移;
4. 腹主动脉旁多发淋巴结转移。
由于患者病灶广泛,不符合二次减瘤术的指征,首选化疗治疗,并在权衡利弊后,决定化疗期间同时行颈部淋巴结放疗。考虑到患者一线化疗时发生IV度骨髓抑制的不良反应,遂更换为紫杉醇175 mg/m2+顺铂70 mg/m2方案,于2018.09.29至2019.03.23静脉化疗6程。并于2019.02.11至2019.03.20行TOMO放疗。2019.03.22颈部及全腹MRI 示阴道残端旁小结节,径约0.5 cm;腹主动脉旁多发淋巴结较前缩小,较大者短径约0.5 cm。RECIST评价疗效PR。
2019.05开始口服奥拉帕利300 mg bid维持治疗至今。服药期间曾出现白细胞减少,轻微恶心、食欲下降等副反应,患者耐受可。截至目前已服药23个月,接近2年,CA125稳定在2 U/ml左右,且2020.03.05全腹MRI示,腹主动脉旁淋巴结较前缩小,表明奥拉帕利维持治疗效果良好,发挥了很好的抗肿瘤作用,为患者生存和生活带来获益。
此外,考虑到患者检出BRCA1突变,而调查患者家族史发现,患者母亲有原发性腹膜癌史,建议患者家属进行遗传咨询。其长姐亦检出BRCA1突变,沟通后进行预防性输卵管和卵巢切除。术前肿瘤标志物正常,术中腹腔冲洗液细胞学阴性,术后病理显示(右附件)输卵管局灶上皮增生活跃,表明此次预防性手术成功地筛查出了可疑增生,阻止了癌变的形成和发展。后续患者仍需动态监测卵巢癌、乳腺癌的发生风险,针对性地定期体检随访,以便及时发现和治疗相关疾病。
李佩玲教授点评

李佩玲 教授
李佩玲,主任医师,二级教授,博士生导师。
现任哈尔滨医科大学附属第二医院妇产科教研室主任、黑龙江省医学会妇产科学分会主任委员,黑龙江省妇科医疗质量管理与控制中心主任,黑龙江省预防医学会妇女保健专业委员会主任委员,中华医学会妇产科学分会、中国医师协会妇产科医师分会委员,《中华妇产科杂志》编委。临床专长为妇科恶性肿瘤诊治、盆底器官脱垂、妇产科疑难重患诊治,以及妇产科急危重患抢救。参编《妇产科学》等国家级规划教材5部,承担国家“十三五”及全国医疗技术推广项目26项,科研课题获奖30项,发表SCI 论文40余篇。以第一完成人获黑龙江省科技进步二等奖、黑龙江省医药卫生科学技术一等奖等,获“第九届中国医师奖”,入选首批省级“龙江名医”、“黑龙江省卫计委专业技术高层次人才库成员”,现为黑龙江省妇产科领军人才梯队带头人。
卵巢癌发病的相关因素尚未完全明确,大多为散发性卵巢癌,而目前已知的危险因素中,遗传因素影响较大。遗传性卵巢癌患者约占所有卵巢癌患者的15%,平均发病年龄较散发性卵巢癌患者早,多携带BRCA基因突变,罹患其他恶性肿瘤的风险增加。病理类型主要为浆液性乳头状囊腺癌,预后较好。
流行病学资料显示,无胚系BRCA基因突变的女性一生中患卵巢癌的几率为1%~2%,而有BRCA1突变的女性一生的患病风险为21%~51%,有BRCA2突变的女性一生的患病风险为11%~17%。因此,有必要对高危人群进行BRCA基因的检测。高危人群包括近亲有人患乳腺癌、卵巢癌或其他相关癌症,或绝经前患乳腺癌,或同时患多种相关的肿瘤,如乳腺癌、卵巢癌,或家族中有男性乳腺癌,或有德系犹太人血统等。
本例患者51岁时因“CA125持续增高,B超发现盆腔包块”就诊,结合肿瘤标志物数据、影像检查资料与术后病理资料,患者确诊为卵巢高级别浆液性腺癌IIA期。调查患者家族史发现,其母亲有原发性腹膜癌病史,因此该患者及其近亲均为罹患癌症的高危人群,建议进行遗传咨询。
患者本人基因检测发现BRCA1突变,兄妹几人中,另有长姐长兄也检出BRCA1突变,证实了遗传因素在患者及其近亲中的致病作用。根据指南,对BRCA1/2突变携带者,建议在35~40岁或完成生育后进行预防性输卵管和卵巢切除。并且在考虑预防性手术时,应与基因突变携带者详细讨论手术的风险与获益。
经过沟通,患者长姐选择接受手术,术后病理显示(右附件)输卵管局灶上皮增生活跃。这一结果令人欣喜,这意味着在遗传咨询的指导下,此次预防性切除输卵管和卵巢成功地筛查出了可能的代谢异常,将病变扼杀在摇篮中,避免了患者长姐遭受罹患卵巢癌的痛苦。但要注意,BRCA1突变与发生乳腺癌的风险也十分明确,此后还要注意动态监测乳腺安全,做到有针对性地预防和筛查,以便及时发现异常和治疗。
通过本例患者及其亲属的诊疗历程,我们不难看出,对卵巢癌患者进行基因检测并筛查出致病性突变,可以帮助医生对患者进行精准治疗,同时,对患者子女或其他一级亲属进行遗传咨询,可以使基因突变携带者得到及时干预,这将极大提高卵巢癌患者的早期诊断率,并降低疾病发病率。但对于一般人群,目前没有有效的筛查手段,也不支持进行常规的卵巢癌筛查。应当重视一些卵巢癌相关的临床症状,如腹胀、盆腔或腹部疼痛、腹围增加、易饱感,或尿频尿急,特别是这些症状新发,或经常出现,应及时进一步检查。
高迎春教授点评

高迎春 教授
高迎春,主任医师,医学博士,南京医科大学副教授,硕士研究生导师,淮安市第一人民医院妇产科主任,妇科主任。
中国医师协会肿瘤医师分会委员,中国医师协会微无创医师分会妇科ERAS专业委员会委员,江苏省医学会妇产科学分会委员,江苏省医学会妇产科学妇科内镜学组成员,江苏省妇幼保健协会妇女保健分会委员,江苏省预防医学会委员江苏省预防医学会内分泌学组成员,淮安市医学会妇产科学分会副主任委员。
曾获省妇幼新技术引进二等奖2项、市级新技术引进奖多项,发表SCI 论文4篇。擅长妇科各级各类手术,尤擅妇科腔镜下肿瘤手术;近年来在妇科快速康复外科领域积累了较丰富的经验。2017年1月至7月在日本国立癌症研究中心研修。
PARP抑制剂为卵巢癌患者的治疗和生存获益带来了革命性变化,引领卵巢癌治疗进入维持治疗和全程管理时代。目前已有多项研究数据显示,PARP抑制剂可显著改善卵巢癌患者的无进展生存时间(PFS)。
SOLO2研究是针对BRCA突变的铂敏感复发卵巢癌患者的一项随机、双盲、安慰剂对照的Ⅲ期临床研究。早期研究结果显示,与安慰剂对照组相比,奥拉帕利维持治疗组患者中位PFS延长13.6个月(19.1个月 vs. 5.5个月),复发或死亡风险降低70%(HR=0.30);独立盲法评估的中位PFS延长了24.7个月(30.2个月 vs. 5.5个月),复发或死亡风险降低75%(HR=0.25)。
2020年ASCO会议上,SOLO 2研究公布其总生存时间(OS)结果。未校正安慰剂组交叉使用PARP抑制剂的患者情况下,奥拉帕利组OS延长达12.9个月(51.7个月 vs. 38.8个月),死亡风险降低26%,5年生存率提高近10%(42% vs. 33%);校正交叉用药的患者后,奥拉帕利组OS延长16.3个月(51.7个月 vs. 35.4个月),死亡风险降低44%。此次研究结果的公布使奥拉帕利成为首个证明可显著延长铂敏感复发性卵巢癌患者OS的PARP抑制剂。
并且,研究中患者开始奥拉帕利治疗2年后,约70%患者仍接受300 mg BID起始剂量治疗。22%的患者接受奥拉帕利维持治疗超过5年,安慰剂组仅为9%。在长达5年的随访中,奥拉帕利的安全性与既往研究一致,不良反应以1~2级为主,可通过对症治疗得到有效管理,大部分患者(89%)能持续治疗直至疾病进展。可见,奥拉帕利用于BRCA突变的铂敏感复发性卵巢癌患者维持治疗,长期获益显著,安全性和耐受性良好。
本病例为BRCA1致病突变患者,是PARP抑制剂维持治疗的优势人群。经规范的二线治疗达到PR,存在阴道残端旁小结节径约0.5 cm,腹主动脉旁多发淋巴结径约0.5 cm。化疗结束一个月后,患者开始服用奥拉帕利300 mg bid维持治疗,服药期间曾出现轻度不良反应,均可耐受。至今已持续用药23个月,CA125始终稳定在2 U/ml左右,且病灶较前缩小,这表明奥拉帕利长期用药疗效确切,充分发挥了PARP抑制剂的抗肿瘤作用,使疾病产生由PR向CR发展的趋势。基于SOLO 2研究的OS数据,相信患者将在奥拉帕利的帮助下,获得更长久的生存获益。
 妇产科在线APP下载
妇产科在线APP下载












