
病例资料
基本情况
•张**,女,53岁
•复发性卵巢癌二次肿瘤细胞减灭术后7次化疗后
•查体:ECOG1,腹部陈旧性疤痕,腹部软,阴道残端愈合可,盆腔未及明显肿块,全身浅表未及明显肿大淋巴结。
详细病史
2013.03
因“右乳癌术后11年,腹胀、纳差2月”收入院,于宫体上方可及直径约6cm大小包块,外形不规则,与宫体无法分离
2013.03.06
手术治疗(外院),术中探查见:进腹探查:淡黄色腹水3100 ml,肝、胆、胰、胃、肠管及大网膜等无明显异常,紧贴脾脏下缘有一肿块,大小约6cm*4cm*4cm,子宫萎缩,双侧卵巢肿瘤约6cm*5cm*4cm,结节状,囊实性,未见明显正常卵巢组织,与周围组织粘连致密。遂行全麻下行卵巢癌根治术(全子宫双附件切除+大网膜切除+阑尾切除+瘤体减灭术),手术未达R0,肠系膜残留<0.5cm
术后病理提示浆液性乳头状癌,FIGO分期IIIC期
2013.08
术后卡铂500mg+紫杉醇210mg化疗8次,末次化疗时间2013.08.29
2013.12
行VP16+环磷酰胺巩固化疗3次,末次化疗时间2013.12.29
2015.04.24
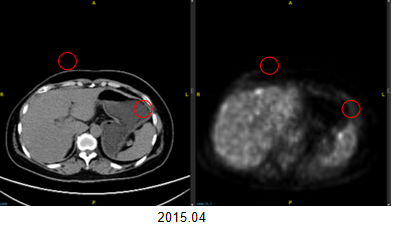
PET提示(图1)
1.卵巢癌术后化疗后,肝、脾包膜多发M。
2.右乳癌术后,颈胸部未见异常FDG代谢增高灶。
3.左侧咽隐窝慢性炎症;左下肺陈旧性病变;肝膈顶小囊肿可能;痔疮可能
2015.05.15
行复发卵巢恶性肿瘤细胞减积术(复杂肠粘连松解术+脾切除术+瘤体减灭+膈肌修补+肝修补术),术中见淡黄色腹水约200ml。子宫双附件缺如,盆腔腹膜见多处直径0.3-2cm结节。手术达R0
2015.10
术后予以白蛋白紫杉醇300mg d1+顺铂40mg d1 d2方案化疗一次,副作用大
改:紫杉醇脂质体210mg+卡铂500mg三次,副作用无法忍受
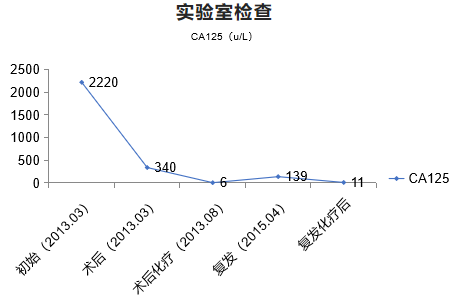
改:吉西他滨1.2g d1 d8,+顺铂40mg d1-d3 三次,末次化疗时间2015.10.10,治疗后CA125水平如图2
2015.11.10
进入SOLO2临床试验,基因检测提示BRCA2基因突变
维持治疗过程
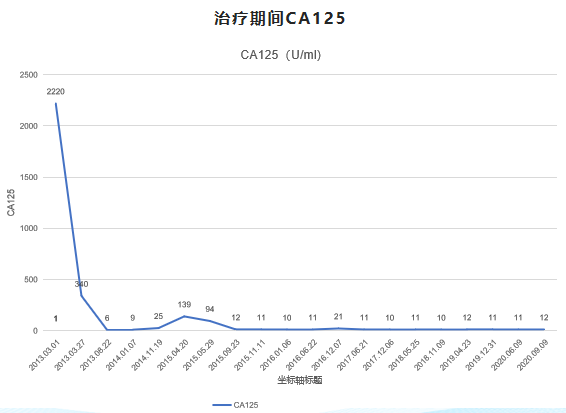
•2015.11.10开始使用奥拉帕利维持治疗至今,CA125检测数次基本均小于15U/ml(图3).
•不良反应:2015.12月患者开始I度恶心(间隔数日轻微恶心、呕吐),无药物治疗;2015.12开始乏力I度,I度贫血,无其他不良反应,可耐受,无需减量。
患者乳腺癌术后11年后原发卵巢癌,一线行卵巢癌根治术,手术未达R0,术后TC方案化疗8次加VP16+环磷酰胺巩固化疗3次。无进展生存期16个月后复发,为铂敏感复发。复发后行二次手术——复发卵巢恶性肿瘤细胞减积术,手术达R0,基因检测结果BRCA2突变,术后化疗后1月给予奥拉帕利维持,目前无进展生存期已达60个月,还在疾病无进展随访中。本例患者奥拉帕利维持治疗初期出现轻度不良反应且可耐受 ,无减量服药。
1.关于二次肿瘤细胞减灭术。
二次减瘤术指的是首次治疗患者在达到临床完全缓解后又复发,而再次施行手术治疗。按照程度不同又可以将其分为无肉眼残留(R0:无肉眼可见的残余灶)、满意的减瘤(R1:残余灶<1cm)、非满意的减瘤(R2:残余灶≥1cm)。SCS是NCCN指南中推荐的针对PSR卵巢癌的可选治疗方案。目前临床尚未对二次手术在改善患者预后的影响有定论,但确有部分患者在二次手术后生存期延长。需要指出的是,不同于初次细胞减灭术只要达到无肉眼残留或满意的减瘤就可以获得较为显著的生存获益,二次减瘤术则只有达到无肉眼残留才能拥有较为显著的生存获益。因此,在二次减瘤手术中应将无肉眼残留作为最终目标。有研究表明,每提高10%的完全切除率,患者中位生存时间延长3个月。
前期的GOG213等研究未能在PSR卵巢癌患者中证实SCS+后续化疗能带来长期生存获益,但亚组分析发现通过对患者进行筛选,比如达到R0切除者则可能有所获益,因此也发展出了AGO评分用于筛选适合SCS的患者。今年ASCO发布的DESKTOP-Ⅲ试验采用了与GOG213试验相似的设计,其筛选患者的标准依据“AGO评分法”,主要终点为OS。其结果从很大程度上回答了长期争议的SCS的获益问题,显示出SCS在部分合适人群中显著延长OS的获益。
除了AGO评分外,中国SGOG的SOC-1研究中采用的iMODEL SCR评分也是比较好的筛选SCS合适患者的方法。
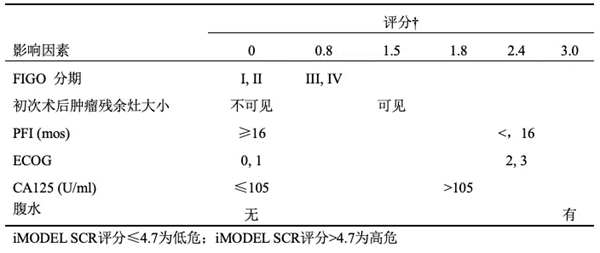
SOC-1研究是于2011年正式开展的前瞻性国内多中心RCT,旨在比较PSR卵巢癌患者接受SCS后续化疗对比单独化疗的疗效差异。SOC-1研究采用的是手术切除率预估模型“iMODELSCR风险评分系统”来选择随机分组的患者。iMODEL SCR评分≤4.7分的病例达到完全切除的机会较高(53.4%),适宜手术;评分>4.7的病例达到完全切除的机会较小(20.1%),不宜手术。
研究从2012年——2019年共招募了357例符合标准的复发性卵巢癌患者,随机分为二线化疗组和手术+后续二线化疗组,主要终点为无进展生存期(PFS)和总生存期(OS),次要终点为无治疗生存期(TFSa)。两组分别97%和96%患者接受了包含铂类药物的二线化疗,且分别有1.1%和10.1%的患者行贝伐珠单抗和PARP抑制剂维持治疗。总体患者中完整切除率为76.7%,在iMODEL>4.7的患者完整切除率为61.1%。两组的60天死亡率均为0。手术组和非手术组的中位无进展生存期分别为17.4个月和11.9个月(HR0.58,95%CI 0.45-0.74,P<0.001)。
从上述数据中我们看到,通过优化选择患者以及优化手术团队,二次肿瘤细胞减灭术可显著延长无进展生存期,另外对TFSa的中期分析表明,二次肿瘤细胞减灭术可能有利于复发性卵巢癌患者长期生存。
2.关于奥拉帕利维持治疗
(1)治疗前基因检测
奥拉帕利是全球及国内上市的首个PARP抑制剂,也是首个阻断同源重组修复缺陷(HRD)细胞/肿瘤DNA损伤应答(DDR)的靶向治疗药物。PARP抑制剂通过捕获与DNA单链断裂处相结合的PARP从而阻断其 DDR机制,导致复制叉停滞、崩溃并产生DNA双链断裂(DSBs),使癌细胞死亡。PARP药物的这类作用机制被称为“合成致死理论”,在一系列HRD阳性的实体瘤中获得了持续的阳性结果。
奥拉帕利在卵巢癌共获批四大适应症,维持和挽救两种用法:
①单药用于BRCA1/2胚系和体系突变,一线含铂化疗后达到CR/PR晚期卵巢癌患者的维持治疗。基于的是SOLO1的临床研究结果。
②联合贝伐单抗用于HRD阳性的,一线含铂化疗后达到CR/PR晚期卵巢癌患者的维持治疗。基于的是PAOLA1的临床研究结果。
③单药用于既往铂类化疗敏感的晚期卵巢癌,复发后采用含铂化疗达到CR/PR后的维持治疗。基于的是study-19和SOLO2的临床研究结果。
④单药用于既往接受三线或三线以上化疗进展的胚系BRCA1/2突变的晚期卵巢癌患者的挽救治疗。有效率为34%。
目前,在中国奥拉帕利在卵巢癌仅获批①、③适应症。
国内外指南推荐卵巢癌患者在初次病理确诊时即进行BRCA基因检测。BRCA基因包括BRCA1和BACA2。研究表明,BRCA1/2突变的肿瘤细胞对于诱导DNA双链断裂的铂类等化疗药物极为敏感。并且,卵巢恶性肿瘤如果具有体细胞或遗传性 BRCA1/2突变,则其从PARP抑制剂治疗中获益的机会更高。HRD包括BRCA1/2基因突变,和/或基因组不稳定性。除了BRCA基因外,还有数十种基因参与了HRD途径,包括BARD1、BRIP1、RAD51C、RAD51D和PALB2等。对这数十种基因进行检测后,检测人员会根据这些结果对患者的HRD进行综合评分,分值≥42分或BRCA突变者都会被定义为HRD阳性。据中国卵巢上皮性癌维持治疗专家共识(2020)所述,HRD阳性的卵巢癌患者相比于HRD阴性的患者,可更加获益于PARP抑制剂单药和双药联合维持治疗。因此,HRD阳性的卵巢癌患者可以选择PARP抑制剂来维持治疗。未来需要更有效的基因检测技术,明确获益人群,使卵巢癌维持治疗更为精准。
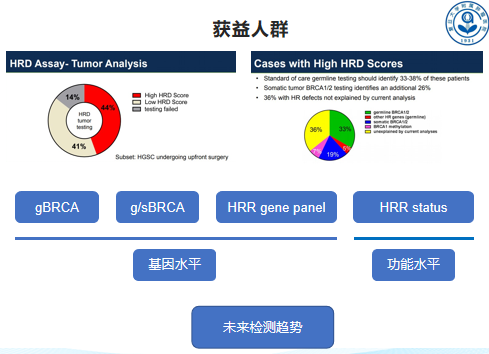
(2)SOLO2研究
近年来随着新兴靶向治疗药物的出现及相关临床研究结果的公布,已有临床研究证明,抗血管生成药物、PARP抑制剂等用于卵巢癌患者的维持治疗,可达到延长无铂间期或无化疗间期,改善患者治疗效果的目的。国内外的多个指南与共识均推荐卵巢癌维持治疗,并被广泛认可,逐渐改变了以往中晚期卵巢癌化疗缓解后观察随访,确诊复发后再治疗的模式,也改变了卵巢癌的治疗策。那么,维持治疗能否改善卵巢癌患者的5年生存率,带来真实的长期获益?
本例中患者初始治疗结束后的PFS为16个月,二线治疗结束后一个月后患者加入SOLO2研究,开始口服奥拉帕利至今,PFS已达5年,即60个月,患者疾病无进展,可见对于铂敏感复发卵巢癌,BRCAm者,奥拉帕利维持治疗可使患者生存显著改善。在奥拉帕利维持治疗初期,患者出现轻度不良反应,后逐渐耐受,无减量,无停药,服药5年,无其他严重不良反应出现,可见奥拉帕利的安全性、耐受性、服药依从性均良好。这一结果与今年ASCO会议上公布的SOLO2研究最新结果相同。
SOLO2研究是评估奥拉帕利单药维持治疗BRCAm的PSR卵巢癌患者的Ⅲ期研究。纳入BRCAm、既往接受过≥2线治疗且对最近一次含铂化疗响应的PSR(复发距上一次含铂化疗结束时间≥6个月)卵巢癌患者,按2:1随机接受奥拉帕利片剂(300mg ,bid)或安慰剂维持治疗,直至疾病进展或发生不可耐受的毒性反应。并根据对前线化疗的响应[完全缓解(CR)或部分缓解(PR)]及无铂间期长度(6~12个月或>12个月)进行分层。主要研究终点为研究者评估的PFS,次要研究终点为OS、第2次无进展生存(PFS2)、至下次治疗的时间(TFST)等。OS数据分析包含将安慰剂组交叉使用PARPi的患者删除后的校正分析,将患者随机入组时错误分层进行校正后的post hoc OS敏感性分析,以及采用Myriad基因检测验证后的胚系BRCA突变(gBRCAm)人群的OS分析。

最终数据截至2020年2月3日,数据成熟度达60%,两组中位随访时间均为65个月,关键基线资料相似。未校正安慰剂组交叉使用PARP抑制剂患者的情况下,相较于安慰剂组,奥拉帕利组OS延长了12.9个月(51.7个月对38.8个月),降低死亡风险26%,5年生存率提高近10%(42%对33%)。
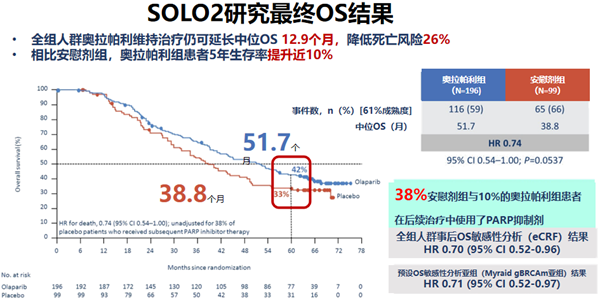
安慰剂组38.4%的患者在后续治疗中交叉使用了PARP抑制剂,使安慰剂组
OS有所延长。校正分析后,相较于安慰剂组,奥拉帕利组OS延长达到16.3个月(51.7个月对35.4个月),降低死亡风险44%。

相较于安慰剂组,奥拉帕利显著延长患者TFST(27.4个月对7.2个月),随访5年时,奥拉帕利组仍有28%的患者保持生存且未接受后续治疗,而安慰剂组仅为13%。
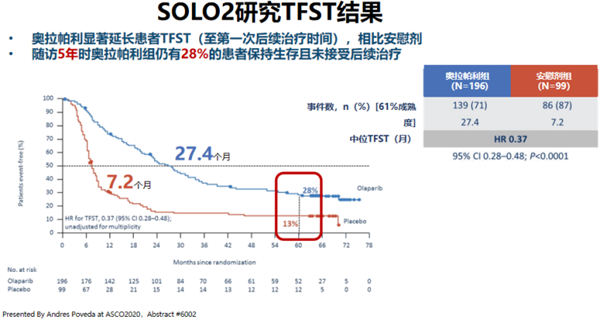
在超过5年的随访后,仍有22%的患者在继续接受奥拉帕利治疗,且未复发,也没有出现不可耐受的毒性反应,再次印证奥拉帕利的长期治疗获益和安全性;而安慰剂组仅有9%仍在接受安慰剂治疗。
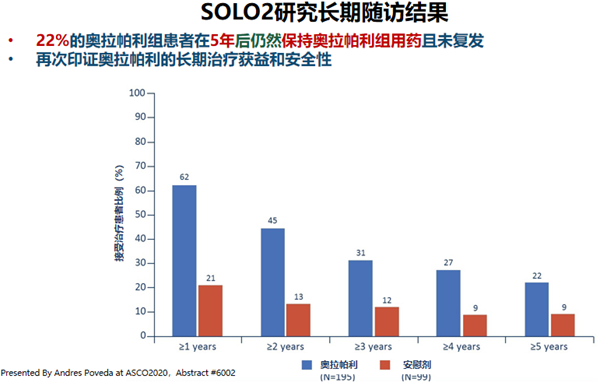
SOLO2长期随访显示奥拉帕利良好的长期安全性。2016年PFS分析至2020年OS分析显示,随着治疗时间延长,治疗相关不良反应发生率、剂量调整和终止治疗比例基本一致。随访时间长达65个月,不良反应发生率与既往研究类似,常见不良反应以1-2级为主,未出现新的不良反应事件。
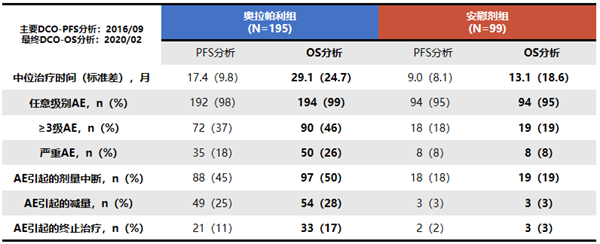
总之,SOLO2研究是首个报道携带BRCAm的PSROC患者PARP抑制剂维持治疗OS数据的III期临床研究。对比安慰剂,奥拉帕利维持治疗延长患者中位OS12.9个月,校正交叉用药数据后,奥拉帕利延长患者中位OS16.3个月,降低患者死亡风险44%。42%的奥拉帕利组患者在随访5年时仍保持生存,5年生存率提高近10%(相比安慰剂组),22%的患者≥5年时仍接受维持治疗未复发,奥拉帕利组患者TFST显著延长(相比安慰剂组)。长期随访结果中,奥拉帕利组剂量调整比例、终止治疗比例和AE发生率未显著升高。本患者初始治疗达CR后,16个月出现复发,在满意的二次肿瘤细胞减灭术(达R0)联合足量、足疗程含铂二线化疗达临床CR的基础上,开始奥拉帕利维持治疗,至今已经5年,远超过一线治疗后的PFS,且未发生疾病进展和不可耐受的毒性反应,可被认为达到了临床治愈,且患者仅在初期出现轻度不良反应,随用药时间的延长,不良反应消失,未减量,未停药,足见PSROC满意的二次肿瘤细胞减灭术+化疗+维持治疗是一有效的治疗方案,可为患者带来良好的临床获益。

复旦大学附属肿瘤医院妇科副主任;博士,教授,主任医师,博士生导师;中国临床肿瘤学会妇科肿瘤专家委员会委员;中国抗癌协会妇科肿瘤专业委员会委员;中国医促会妇产科专业委员会青年委员;上海市抗癌协会妇科肿瘤专业委员会委员;上海医学会妇科肿瘤专业委员会青年委员;上海医学会妇产科学专业妇科内镜学组委员;上海市抗癌协会癌症预防和筛查专业委员会委员
回看本例患者,在2013.03.06行卵巢癌根治术(未达R0),术后卡铂500mg+紫杉醇210mg方案化疗8次,末次化疗时间为2013.08.29,2013.12行VP16+环磷酰胺方案的巩固化疗3次,末次化疗时间为2013.12.29,治疗达CR,直至复发(2015.04.24),患者初始治疗后的PFI为20个月,PFS为16个月。2015.04.24 PET/CT检查显示卵巢癌肝脾包膜多发复发灶,CA125升高到 139U/mL,确诊患者卵巢癌复发。2015.05.15行二次手术--复发卵巢恶性肿瘤细胞减积术(R0),术后给予含铂化疗7次,2015.10.10化疗结束,达临床CR。二线化疗期间因不能耐受的化疗副作用,两次更改化疗方案。2015.11.10进入SOLO2临床试验,给予奥拉帕利维持,其基因检测提示BRCA2基因突变。从患者开始使用奥拉帕利维持治疗至今,CA125检测数次基本均小于15U/ml,PFS已达60个月,远超初始治疗后的PFS时间,还在无疾病进展随访中。
首先,患者为BRCA突变的铂敏感复发卵巢癌,影像显示为多灶复发,复发时CA125为139U/mL,肿瘤负荷较重,充分评估后选择复发卵巢恶性肿瘤细胞减积术(R0)联合化疗治疗。NCCN一直将二次肿瘤细胞减灭术列为PSR OC的治疗选项,具体而言,就是前次化疗完全缓解后无治疗间隔为6个月或以上、没有腹水而且病灶孤立的患者,可以考虑。可见手术和化疗依然是铂敏感复发性卵巢癌治疗的基石。
在中国的一些主要的癌症中心,复发卵巢癌二次肿瘤细胞减灭术(SCR)已成为标准治疗。
2011年开展的SOC1/ SGOG-OV2研究为Ⅲ期随机对照临床试验,入组无铂间期超过6个月的首次复发卵巢癌患者,经 iMODOL 评分结合 PET-CT 检查预估可达到 R0切除。患者随机分配到二次细胞减灭(SCR)序贯化疗(手术组)或仅二线化疗组(化疗组)。设定双主要终点,为无进展生存(PFS)和总生存(OS)。次要终点为累积的无治疗生存时间(TFSa),定义为总生存时间减去随机分组后累积手术和化疗的时间。今年的 ASCO 大会上报告的是 PFS 的最终分析结果。其结果:从2012年至2019年随机入选患者357例患者,175例化疗组患者中,6.3%的患者在随机分配治疗期间接受了手术,化疗组患者二次复发后接受手术治疗占比为36.9%。ITT 人群中,分别有97%和96%的患者接受了含铂二线化疗。手术完全切除(R0)率为76.7%,iMODEL>4.7的患者的 R0 切除率为61.1%。手术组和化疗组的60天死亡率均为0。术后30天≥3级的并发症发生率为5.2%。中位随访36.0个月,中位PFS在手术组和化疗组分别为17.4个月和11.9个月(HR=0.59,P<0.001)。以手术组更优。中位至开始首次后续治疗的时间(TFST)亦以手术组更优(18.1个月对比13.6个月,HR=0.59)。OS和TFSa数据尚不成熟。中位TFSa在R0切除亚组和化疗组分别为未达到和39.5个月(HR=0.59)。手术组的TFSa较化疗组显示出更好的长期生存结果。因此,对于经选择的患者,SCR能够显著延长PFS,且获益幅度较大。而TFSa的中期分析结果也提示 SCR可能有助于长期生存。
其次,患者基因检测为BRCA2基因突变,是PARP抑制剂维持治疗的显著获益人群,复发治疗缓解后通过奥拉帕利维持治疗无疾病进展生存时间长达60个月,SOLO2研究中两个治疗组的中位随访时间均为65个月,相较于安慰剂,奥拉帕利维持治疗前所未有地、极具临床意义地延长了患者OS 12.9个月,死亡风险降低26%(51.7个月vs38.8个月;HR0.74,95%CI 0.54-1.00,p=0.0537),同时提高了近10%的5年生存率,显著延长TFST;22%的患者持续使用奥拉帕利超过5年,仍未发生疾病进展,长期安全性良好。本病例和SOLO2的研究结果都让我们看到,只要患者携带同源重组基因缺陷(HRD)致病突变,50%的晚期卵巢癌患者的生存期可以逼近、甚而超越5年生存大关!因此,奥拉帕利作为首个在BRCA突变的PSR卵巢癌维持治疗中OS有一年以上获益的PARP抑制剂,对于BRCA突变的PSR患者显示出长期的治疗生存获益,是BRCA突变的PSR卵巢癌患者必不可少的标准治疗。其实,PARP抑制剂维持治疗治疗的获益并不仅仅局限在BRCAm铂敏感复发性卵巢癌患者。Study19研究已经显示BRCAwt患者PFS也显著延长,同时5年不复发的长期疗效与BRCA基因突变无关。11%的患者长达6年不复发。OPINION研究的最新中期分析更是进一步证实了奥拉帕利在non-gBRCAm 铂敏感复发性卵巢癌患者中的疗效,mPFS为9.2个月,安全性与既往研究相似。因此,对于铂敏感复发性卵巢癌患者,无论BRCA突变与否,奥拉帕利维持治疗均可以延缓其复发,且安全性好。
第三,本病例不仅真实的反映了奥拉帕利维持治疗用于BRCA突变的铂敏感复发卵巢癌患者,给患者带来的实际利益,同时强调了基因检测有助于制定和开展有针对性的、个体化的治疗方案,从而为患者带来更好的临床获益,也再一次证明了奥拉帕利在中国人群中应用的安全性。作为中国案例,对于中国患者的用药指导具有更大的意义。作为口服药物,临床医生和患者最为关注的,一是其有效性,二就是其不良反应小,患者可耐受。对于接受长期治疗的患者,药物安全性无疑是疗效获益的前提,患者必须在可耐受的情况下,才可能持续接受治疗从而获得好的疗效。SOLO2中,长达65个月的随访数据显示,奥拉帕利长期应用的不良反应发生率与既往研究类似,常见不良反应以1-2级为主,未出现新的不良反应事件。本患者在化疗耐受差的情况下,结束化疗4周内开始PARP抑制剂维持治疗,并且起始足剂量,仅初期出现轻微的恶心、呕吐、乏力和I度贫血,均可耐受,一直未减量,患者服药5年,依从性好,进而更加真实的反映了奥拉帕利长期服用安全。
总之,高复发风险是卵巢癌的特点,也是卵巢癌治疗中的巨大挑战,近年来靶向药物及维持治疗的发展为卵巢癌患者带来了新的希望。国内外的多个指南与共识均推荐卵巢癌维持治疗,并被广泛认可,逐渐改变了卵巢癌的治疗策略,尤其是铂敏感复发的卵巢癌患者,从本病例可以看出,经过满意的二次肿瘤细胞减灭术+足量足疗程化疗+维持治疗这一系列治疗,使患者OS显著获益。

复旦大学附属肿瘤医院浦东院区妇瘤科在吴小华多学科首席专家的领导下,以杨慧娟教授主诊组为主要诊治团队,自2019年11月11日正式收治第一例患者以来,已经全面收治各类妇科肿瘤手术患者近700例,疾病谱覆盖所有妇科恶性肿瘤,其中卵巢癌患者占44.5%。在围绕晚期和复发卵巢癌患者的手术治疗方面,团队就手术可切除性、手术获益、手术方式、手术耐受性及术后可能并发症等对每一个患者进行充分评估。对每一例手术患者团队强调围术期管理,在术前、术中和术后对患者进行全方位的支持、促进患者恢复。在子宫内膜癌和宫颈癌的手术治疗方面,团队更加强调微创和精准手术理念,根据患者的疾病分期、年龄和对生育的要求选择机器人辅助腹腔镜手术、腹腔镜手术或开腹手术。在少见肿瘤如外阴阴道恶性黑色素瘤、外阴癌等手术治疗中强调根治和功能恢复并重。
妇瘤科浦东院区门诊出诊医生更加多元化,患者可以根据疾病治疗阶段选择专病门诊和专家门诊。最近,浦东院区设立了吴小华教授团队多学科门诊和杨慧娟教授团队多学科门诊,团队成员包括了妇瘤科、病理科、影像科、核医学科及麻醉科等科室医生,是多学科综合治疗组从病房向门诊的延伸, 方便了危重疑难患者的就诊。经和患者及家属的一站式沟通,确立最终治疗方案,为患者提供专业精准的诊治方案,改善患者的就医体验,提升医疗服务效率和水平,并使患者和家属在治疗决策的选择过程中参与度更高。
在临床研究方面,妇瘤科的多项新药、新技术正在或即将在浦东院区开展,包括免疫治疗、靶向治疗、术中放疗、热灌注化疗等等。在保障患者的安全和获益前提下,鼓励符合条件的患者积极参与临床研究。为改善患者预后、特别是一些难治的妇科恶性肿瘤提供了新的治疗途径。
总之,妇瘤科浦东院区团队在医院和科室的支持下,继续秉承妇科肿瘤规范化、全程治疗的理念,以手术治疗为核心,临床研究为拓展,为患者提供精准规范的综合治疗, 改善患者预后,提高患者生活质量。
 妇产科在线APP下载
妇产科在线APP下载












