摘要
目的 筛选影响整倍体单囊胚移植成功率的关键因素。
方法 本项回顾性研究纳入2014年1月至2018年1月期间在上海集爱遗传与不育诊疗中心进行胚胎植入前遗传学检测(PGT)的冷冻整倍体单囊胚移植周期共956个的患者临床资料。按照移植结局,将患者分为妊娠组(n=509)及未妊娠组(n=447),比较两组间的临床资料,筛选出对移植妊娠率产生影响的关键因素;同时,进一步将妊娠组患者分为活产亚组和流产亚组,对比两亚组间的临床资料并利用logistic回归筛选对流产造成影响的显著性因素。
结果 妊娠组较未妊娠组,移植时子宫内膜厚度显著增厚[9(8,10)mm比8(8,10)mm](P=0.006);质量良好的囊胚相对于质量较差的囊胚临床妊娠率(59.2%比46.3%)及活产率(50.2% 比37.7%)显著上升(P=0.001)。此外,活产亚组与流产亚组相比,囊胚发育时间为流产相关风险因素,OR值为0.536(95% CI=0.309~0.929)。
结论 在整倍体单囊胚移植冷冻周期中,较厚的子宫内膜、发育较快以及级别较高的囊胚是种植成功的关键因素。维持后期妊娠的过程中,发育较快的囊胚(第5日)活产率更高,流产率更低。
【关键词】 胚胎移植; 妊娠结局; 整倍体囊胚; 囊胚质量; 囊胚发育
基金项目:上海市卫生和计划生育委员会科研课题(20174Y0116)
DOI: 10.3760/cma.j.cn101441-20200228-00091
现今,辅助生殖技术已成为治疗不孕症的重要手段而随着体外胚胎培养体系的不断完善,囊胚移植得到了广泛应用。研究认为囊胚移植有着更高的妊娠率,从而可以提高活产率[1-2]。而相对于双胎妊娠,单胎妊娠有着更高的活产率,同时也显著降低孕产妇的并发症,因此,选择性单囊胚移植近年来被逐渐推广[3-4]。有些学者研究显示发育较快的囊胚以及形态学评分较好的囊胚有着更高的着床潜能,从而获得更好的移植结局[5-6],而另一些研究则认为,囊胚形成的时间对胚胎种植潜能的影响存在争议[7]。近年来也有结果显示对反复种植失败患者进行整倍体单囊胚移植,可改善妊娠结局[8]。针对这些问题,本项回顾性分析2014年1月至2018年1月间在上海集爱遗传与不育诊疗中心进行胚胎植入前遗传学检测(PGT)的整倍体单囊胚冷冻移植周期的临床资料,旨在寻找影响整倍体单囊胚移植妊娠结局的关键因素,为调整胚胎移植策略提供参考。
一、研究对象及分组
回顾性分析2014年1月—2018年1月期间在上海集爱遗传与不育诊疗中心进行PGT并进行冻融胚胎移植(frozen-thawed embryo transfer,FET)的患者资料。纳入标准:①患者年龄20~45岁;②因夫妇一方染色体异常或者单基因病进行PGT周期;③进行标准常规促排卵方案,包括促性腺激素释放激素激动剂(gonadotrophin-releasing hormone agonist,GnRH-a)长方案和短方案,以及促性腺激素释放激素拮抗剂(gonadotrophin-releasing hormone antagonist,GnRH-A)方案。排除标准:①移植超过1枚以上胚胎;②宫腔粘连;③复发性流产及反复种植失败为指征的PGT周期;④卵裂期胚胎冷冻并解冻复苏后培养至囊胚期后进行活检的PGT周期;⑤经历2次活检的整倍体囊胚移植周期;⑥供卵及供精周期;⑦患者合并未控制的内分泌异常;⑧合并肿瘤。根据FET后妊娠结局,将患者分为妊娠组和未妊娠组,再将妊娠组细分为活产亚组和流产亚组。临床妊娠包括宫内妊娠及宫外妊娠。妊娠28周以前的宫内妊娠丢失定义为流产。本研究符合《赫尔辛基宣言》。
二、研究方法
1. 控制性超促排卵方案:包括短效GnRH-a长方案,短效GnRH-a短方案以及GnRH-A方案。短效GnRH-a长方案:在促排卵前的一个月经周期黄体期给予GnRH-a(达必佳,瑞士辉凌)连续注射14 d进行降调节,降调节第15日起根据患者的血清雌二醇、孕酮、卵泡刺激素(follicle-stimulating hormone,FSH)、黄体生成素(luteinizing hormone,LH)以及基础窦卵泡计数启动促性腺激素(gonadotrophin,Gn)包括尿促性腺激素(hMG,乐宝得,中国丽珠)或重组FSH(r-FSH,果纳芬,法国默克雪兰诺)促排卵治疗。GnRH-A方案采用灵活方案,即在月经周期第2日(D2)~第3日(D3)启动Gn促排卵,当主导卵泡直径达到14 mm时每日添加GnRH-A(思则凯,法国默克雪兰诺)0.25 mg直至扳机日。
2. 取卵、受精及胚胎培养:当1个及以上卵泡直径达18 mm以上即进行扳机,激动剂方案使用人绒毛膜促性腺激素(hCG,中国丽珠)5000~10 000 IU扳机,拮抗剂方案使用GnRH-a 0.2 mg联合hCG 2000 IU扳机,扳机后35~36 h进行取卵。所有周期均进行卵胞质内单精子注射(intracytoplasmic sperm injection,ICSI)授精,采用连续培养体系将受精后的胚胎培养至5~6 d,直至囊胚形成。囊胚评分及胚胎活检:所有囊胚均采用Gardner方法进行形态学评分,并根据囊胚发育情况分为D5及D6囊胚。5AA/AB视为优质囊胚,5BB/5AC/5CA视为良好,5BC/5CB视为较差囊胚。所有囊胚活检前均进行辅助孵化,滋养层细胞取5~8个进行送检后,囊胚进行玻璃化冷冻保存。本中心的冷冻标准为5BC和5CB以上的囊胚。
3. 移植前内膜准备:所有移植周期均采用人工激素替代(hormone replacement therapy,HRT)周期,于月经第3~5日开始口服戊酸雌二醇(补佳乐,德国拜耳)4 mg/d,月经第10日进行超声及激素检查,调整用药。当子宫内膜厚度增长至7 mm及以上时进行内膜转化,肌内注射黄体酮(浙江仙琚制药)60 mg/d或雪诺酮(法国默克雪兰诺)90 mg/d或安琪坦(法国博赏)600 mg/d阴道使用,内膜转化后的第6日进行单囊胚移植。
4. 冷冻胚胎复苏及移植:于移植当日上午进行囊胚解冻复苏,复苏后4~6 h进行胚胎移植,宫腔内移植1枚胚胎,移植前需评估囊胚扩张情况并进行记录。移植后每日予以地屈孕酮(美国雅培公司)20 mg口服,黄体酮40 mg肌内注射或雪诺酮90 mg/d或安琪坦600 mg/d阴道使用。
5. 妊娠随访:移植后14 d进行血清hCG检测,血清hCG阳性者移植后第25~28日行阴道超声检查,见妊娠囊诊断为临床妊娠。所有妊娠者接受持续随访,直至随访到明确妊娠结局(宫外孕、流产或活产)。分娩者随访内容包括产科并发症、分娩方式、新生儿孕周、性别、出生体质量、身高、Apar评分、出生缺陷等。
三、统计学分析
统计分析采用SPSS25.0软件,非正态分布数据采用中位数(第25百分位数,第75百分位数)[M(P25,P75)]显示,采用单因素方差分析或Kruskal-Wallis检验分析连续参数数据;计数资料以率(%)表示,用χ2检验或Fisher精确检验分析分类变量。采用二元logistic回归分析影响整倍体单囊胚移植结局的关键因素。P<0.05为差异具有统计学意义。
一、两组研究对象基本临床资料及取卵周期参数对比
本研究最终纳入956个FET周期。妊娠组与未妊娠组患者的年龄、基础FSH、AMH、BMI、促排卵Gn用量及使用时间,hCG注射日雌二醇水平差异均无统计学意义(P均>0.05)(表1)。
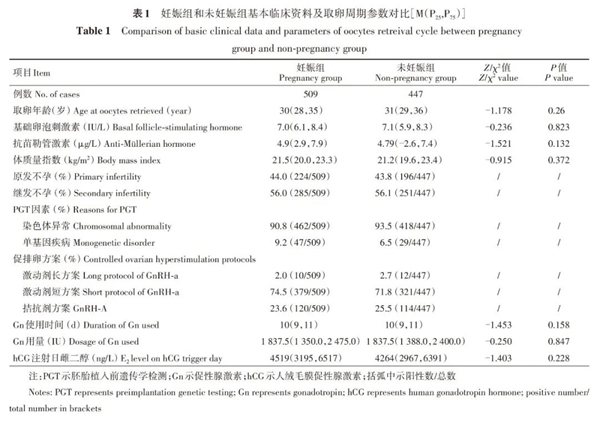
二、妊娠组和未妊娠组移植周期参数对比及移植结局比较
1. 妊娠组较未妊娠组相比:妊娠组较未妊娠组相比在移植年龄、移植时囊胚扩张比例上差异无统计学意义(P>0.05)。妊娠组移植时子宫内膜厚度较未妊娠组增厚,差异有统计学意义(P=0.006)。妊娠组较未妊娠组相比,质量良好的囊胚占比显著升高(45.1%比41.6%),质量较差的囊胚占比明显下降(39.1%比51.7%),差异均有统计学意义(P<0.01)(表2)。优质囊胚及质量良好的囊胚相对于质量较差的囊胚妊娠率显著上升[57.1%(40/70),59.2%(270/450),46.3%(199/430)],差异有统计学意义(P均<0.01)。优质囊胚与良好囊胚之间着床率差异无统计学意义(57.1%比59.2%,P=0.553)。妊娠组中D5囊胚比D6囊胚占比显著上升,差异有统计学意义(77.6%比68.2%,P=0.001);D5囊胚的妊娠率显著高于D6囊胚[56.4%(395/700)比44.5%(114/256),P<0.01]。
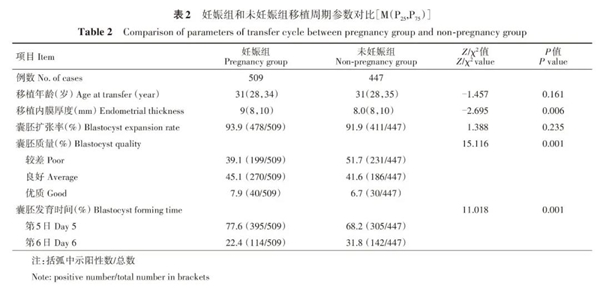
2. 妊娠相关因素logistic回归分析:结果显示,子宫内膜厚度、囊胚发育情况和囊胚质量为妊娠相关因素,OR值分别为1.111(95% CI=1.022~1.207)、0.654(95% CI=0.495~0.864)、0.668(95% CI=0.494~0.905)(表3)。
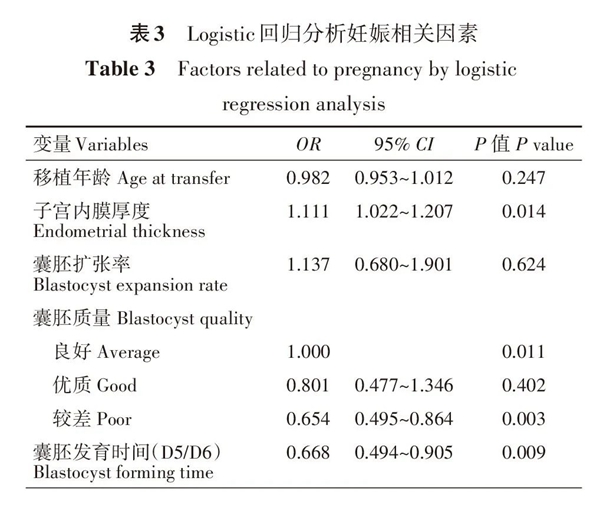
3. 囊胚质量及囊胚发育对活产率的影响:优质或者质量良好的囊胚活产率[48.6%(34/70)、50.2%(229/456)]相对于质量较差的囊胚活产率显著上升[37.7%(162/430)],差异有统计学意义(χ2=14.43,P=0.001;χ2=12.31,P<0.001);此外D5囊胚的活产率[48.3%(338/700)]比D6囊胚的活产率[34.0%(87/256)]显著上升(χ2=9.45,P<0.001)。
三、流产相关因素分析
将妊娠组数据分为活产亚组及流产亚组,其中活产亚组425例,宫内流产亚组79例,剔除宫外孕3例,死产2例。
1. 活产亚组及流产亚组的基本参数对比:活产亚组和流产亚组患者在移植年龄、基础FSH值、AMH值、BMI、移植时囊胚扩张率以及囊胚级别差异均无统计学意义(P>0.05)。活产亚组患者较流产亚组患者内膜较厚,但差异无统计学意义(P=0.22)。活产亚组D5/D6囊胚的比例明显上升,与流产亚组比,差异有统计学意义(P=0.007)(表4)。
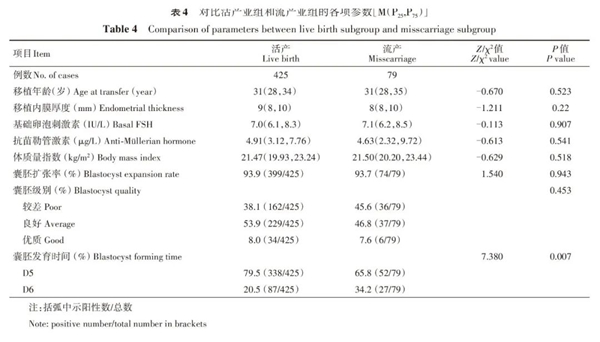
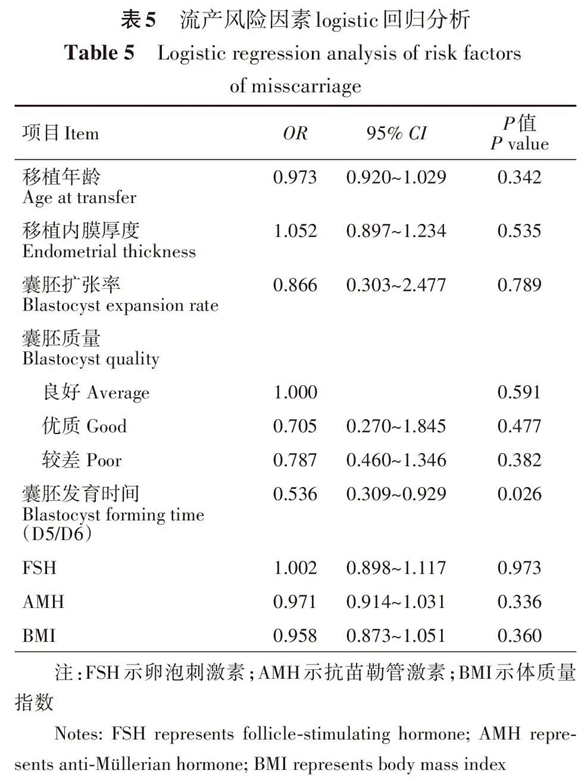
2. 流产风险因素的logistic回归分析:结果显示,囊胚发育(D5/D6)为流产相关风险因素,OR值为0.536(95% CI=0.309~0.929)(表5)。
随着辅助生殖技术的不断发展,对于妊娠结局的关注日益增长。而囊胚培养系统和冻融胚胎技术的不断提高,使冷冻囊胚移植成为越来越多生殖中心的选择。已有诸多研究表明,囊胚移植可以提高临床妊娠率[9]。与此同时,多胎妊娠已经成为辅助生殖最主要的产科并发症[10]。而很多学者认为,通过选择发育潜能较好的单个囊胚移植,在保证着床率的同时减少了移植胚胎数,从而降低了多胎发生率[6]。而对于整倍体囊胚,研究表明整倍体囊胚有着较高的着床率以及持续妊娠率[11],因此整倍体单囊胚移植也许会成为未来移植的方向。
本研究的结果显示,整倍体囊胚移植后临床妊娠率与子宫内膜厚度显著相关,妊娠组子宫内膜较未妊娠组明显增厚,这与已有报道[12]结果一致。本研究中另一个与临床妊娠相关的阳性指标即囊胚质量,虽然优质囊胚相对于良好囊胚在本研究中未显示出其着床优势,分析产生这一结果可能由于本研究中优质囊胚移植绝对例数较少,仅70例,占所有移植周期的7.32%,因此产生统计学偏倚。但在样本量都较大的质量良好的囊胚及质量较差的囊胚的对比中,前者的妊娠率显著上升。与此同时,囊胚的发育时间也非常重要,D5囊胚的妊娠率(56.4%)显著高于D6囊胚(44.5%,P<0.001),同时,logistic回归分析显示内膜厚度、囊胚发育情况和囊胚等级为影响妊娠的相关因素,这与其他在非PGT单囊胚移植的一些研究中得出的结论相似[6,13]。在影响活产的因素中,本研究结果提示,在维持妊娠的过程中,囊胚的质量对妊娠结局不产生影响,而囊胚的发育时间则起到了比较重要的作用,我们的结果显示,发育较快的囊胚活产率上升,流产率显著下降。本研究中虽然所有周期均移植整倍体囊胚,但流产率依然高达15.5%(79/509)。基于本研究中90%以上的病例因染色体异常而行PGT,近年来也有一些研究表明,夫妇一方染色体平衡易位患者行PGT移植后的流产率可高达21.6%[14],而排除胚胎染色体异常因素后导致流产的具体原因仍不明确;本研究79例流产中,有31例为中晚期流产(孕周>12周),而目前遗传学理论揭示,12周之前的流产,胚胎染色体异常的比率可高达60%,而12周以后的流产染色体异常的发生率下降至20%[15]。
本研究中未显示囊胚复苏后囊腔是否完全扩张会对移植结局产生影响。而Zhao等[15]的研究表明囊腔扩张与临床妊娠率呈正相关,分析这种偏倚可能是由于本研究中纳入的大部分囊胚滋养层细胞级别均为B级或C级,而复苏后囊腔扩张程度取决于滋养层细胞,可能是本研究未得出与其他研究类似结果的原因。
随着胚胎植入前非整倍体检测(preimplantation genetic testing for aneuploidies,PGT-A)技术的不断开展,在临床工作中,我们会时常发现,即便是患者进行了整倍体囊胚移植,依然会面临流产。本研究在排除复发性流产患者后,分析整倍体单囊胚流产率及活产率相关因素后提示,囊胚质量以及囊胚发育时间是影响活产率的显著相关因素。有学者认为,囊胚发育的速度与整倍体率无关[16],而我们的研究显示,在移植整倍体囊胚的情况下,D6整倍体囊胚移植后的流产率显著上升,高达23.7%(27/114),一定程度说明移植发育迟缓的整倍体囊胚面临较大的流产风险。这也提示我们,在PGT-A周期,发育迟缓的整倍体囊胚的移植价值和风险值得探讨。
综上所述,本研究表明,在整倍体单囊胚移植冷冻周期中,移植日较厚的子宫内膜以及形态学级别高的D5囊胚移植的患者临床妊娠率及活产率显著上升。本研究是一项回顾性研究,亚组分组中流产组例数少,且患者年龄分布范围较广,结果产生偏倚可能性较大,而妊娠的过程中,导致流产的因素较为混杂,因此需要更大样本的前瞻性队列研究来综合考量该结果。
参考文献(略)
 妇产科在线APP下载
妇产科在线APP下载












