随着现代电子技术和现代光学技术的发展,宫腔镜的开发和应用,妇科诊断和治疗的模式发生了革命性变化,使得原来开放的、有创的妇科诊断和治疗越来越多地被内镜手术和微创方法所替代,这里对近三年内其中的一些进展进行综述:
一、诊断方面
1.子宫内膜发育不良
Jacques E. Hamou 1991 最先描述了这一现象,其病理机制至今不明, 目前趋向于认为是生理性表现,已有报道多在月经黄体期或接受孕激素的治疗。需要与Rendu-Osler-Weber 疾病鉴别,该病常合并皮肤、粘膜和内脏的毛细血管扩张和动静脉畸形。Raffaele Paolett等【1】归纳总结其镜下表现为:暗红色迂曲的血管平行排列覆盖于整个子宫内膜表面。
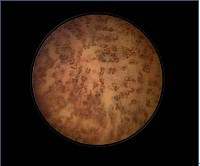
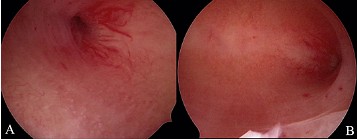
2.输卵管口太阳征:
输卵管口太阳征是慢性输卵管炎的宫腔镜下表现,表现为双侧的输卵管口被放射状充血排列的血管包绕。
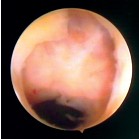
3. 剖宫产瘢痕憩室
Talamonte VH等【2】总结了剖宫产术后点滴状出血的20例患者中,18例(90%)患者在宫颈下1/3可见到剖宫产瘢痕,这些患者至少有一次剖宫产史,年龄在18到45岁之间,未服用激素,无其它影响宫腔解剖的手术史。镜下可看到有特征性的膨大和紧接着的前壁回缩,这是假腔存在的表现,2例患者没有假腔。究其原因,相比单纯缝合,连续锁边缝合可能干扰局部组织的血液循环,导致局部坏死和活瓣的形成。
4. 粘膜下肌瘤的新分类
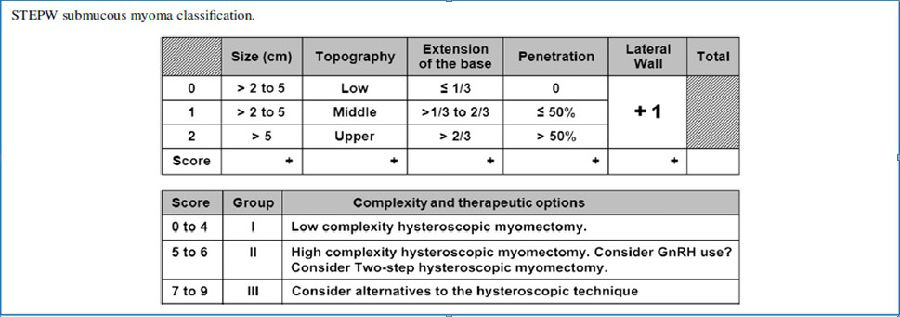
Ricardo Bassil Lasmar等【3】进行了一项对比肌瘤切除新旧分类预测能力的试验:总的肌瘤完整切除率:190/205(92.7%) ,不完全切除率15/205(7.3%),STEPW分类:评分≤4分全切率:140/140(100%) ,评分﹥4分全切率:50/65(76.9%),未能完全切除的15例评分都﹥4分,评分大于4分者手术时间长、并发症多、过度水化、使用GnRHa的机会相对较高;而旧的ESGE分类:156/164(95.1%)例0型和I型肌瘤,34/41(82.9%)例II型肌瘤被全切。
5.HNPCC/Lynch综合症(LS)筛查:
HNPCC/Lynch 综合症 (LS)是由于DNA错配修复基因(MMR)突变导致的遗传性综合症: MLH1, MSH2, MSH6 和 PMS2. Lynch 综合征终生内膜癌终生发生子宫内膜癌的风险为40–60%,对于30-35岁有推迟或不想接受手术的患者推荐定期子宫内膜采样,由于LS中筛查子宫内膜癌的已发表文献较少,子宫内膜癌筛查的有效性尚待定。已有的方式有:经阴/腹超声,经阴道超声和子宫内膜采样,宫腔镜,门诊宫腔镜子宫内膜采样(OHES)。其中OHES的特异性为89.8%(可信区间79.2,96.2%),有较高的阳性似然比:9.8(可信区间4.6,21) 和较低的阴性似然比0。而TVS的依次为为84.75 %(可信区间 73, 92.8 %), 3.28 (可信区间 1.04,10.35)和0.59 (可信区间 0.22, 1.58). 平均随访22个月,无漏诊的内膜癌。内膜癌的年发生率为3.57% (可信区间0.09, 18.35),息肉为10.71%(可信区间2.27,28.23),总的内膜病变为21.4%(可信区8.3,40.1)【4】。
二、围术期措施:
1.内膜薄化:
Pasquale Florio等【5】进行了一项随机、双盲、对照的临床对照试验,将91位患者分成2组,A组有46位,每天在阴道后穹窿放置达纳唑400mg同时服用三片叶酸作为安慰剂;B组患者有45位,每天口服达纳唑600mg,tid,同时阴道放置2片乳酸杆菌片作为安慰剂;在治疗期间两组病人都没有内膜出血。但是口服达纳唑一组,恶心(6/45; 13.3%)、呕吐(6/45; 13.3%)明显高于阴道组(P = 0.04)。口服和阴道用药组前,用药前内膜厚度分别为:6.6+0.4mm,6.5+0.3mm,差异不明显;用药10天后,内膜厚度分别为 4.2+0.2mm,5.8+0.6mm(P<0.001),差异具有统计学意义;用药30天后,内膜厚度分别为3.0+0.6mm,4.9+0.8mm(P<0.001)差异具有统计学意义。内膜无反应者,阴道组为1,而口服组为9,(P= 0.035),萎缩的同时带有内膜局灶增厚的阴道组为1个,口服组为10(P=0.02);总的来说,阴道使用达纳唑,内膜萎缩更明显,且代谢紊乱和副反应低于口服组。Ettore Cicinelli等【6】挑选了74位息肉术前的患者,患者息肉直径皆小于1.5cm,术前6个月的月经规律,将患者随机等分成两组:A组患者在增殖期(周期的第5-7天)进行手术;B组患者服用Qlaira 的9-11天进行手术,患者在月经期的开始服用淡黄色的药片10天。(每片包含2 mg 的E2 valerate 和3 mg 的dienogest)。结果,A、B两组的内膜厚度术前分别为:5.1 (±0.8) mm和4.7(±0.7)mm,术后分别为: 6.9(±0.8)mm和4.6(±0.7) mm(p<0.05),B组较A组薄;镜下A组有16(43.2%)位患者处于正常的增殖期,呈薄薄的淡粉色, 20位患者 (55.5%)内膜表面增厚不均质, 间质水肿,可见到畸形的血管。相反,B组中33位B(91.7%)患者内膜萎缩,规则,淡薄。宫腔镜术前Qlaira处理是一种廉价,有效的方法,且仅需服药10天,易于推广。
2.窄带成像:
窄带成像(NBI)是一种新的内镜技术,通过缩短可见光谱的范围,使得粘膜浅层微血管和粘膜表面的微结构增强。所使用的光谱波长范围为415±30nm和540±30nm。在妇科,NBI最近已被用于腹腔镜下识别腹膜表面的子宫内膜异位症,评估异位内膜的微血管厚度,以及诊断子宫内膜病变【7】
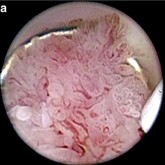
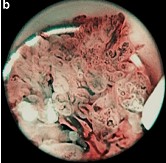
a.传统宫腔镜显示伴有血管的乳头状病灶突出于子宫内膜表面; b. 窄带成像清晰的显示乳头状突出病灶表面扭曲、扩张、螺旋状的不典型血管【8】。
Raffaele Tinelli等【9】回顾分析801例宫腔镜检查同时行普通光和NBI的患者。NBI与普通光的敏感性之比为93%vs81%(P<0.005),特异性为99%vs99%,阳性预测值为98%vs88%(P<0.005),阴性预测值为99%vs98%;子宫内膜低度增生的敏感性为82% vs 56%(P<0.005),特异性皆为99%,阳性预测值为79%vs71%(P<0.005),阴性预测值为98%vs 96%。而在高危增生中, 敏感度为60% vs20%(P<0.005),特异度皆为99%,阳性预测值为67% vs 25%(P<0.005),特异性和阴性预测值皆为99%。nbi对于检测低危和高危的内膜增生显示了较高的价值,提高了宫腔镜探测子宫腔病变的准确性,但尚需要多中心的试验来证实该项技术的真正价值。
3.防粘连:
预防术后粘连是临床上常常考虑的问题,Valerio Mais等【10】进行了一项meta分析,共选择了5个合格的随机对照试验,用来分析使用自体交联透明质酸后,病人的术后粘连情况;发现使用胶的患者术后粘连的情况明显低于未使用胶者。防止腹腔镜子宫肌瘤剔除术后粘连的OR 为0.248, 95% CI为:0.098-0.628;防止宫腔镜术后粘连的OR 为0.408, 95% CI为:0.217-0.766。Attilio Di Spiezio Sardo等【11】进行了另一种胶的研究,将110位患者分为2组,1组进行宫腔镜手术后,宫内使用聚乙烯氧化羧甲基纤维素钠, 第2组为对照组,仅进行宫腔镜手术。术后1个月,二探评估宫腔内粘连的比率与严重程度。同时评估宫颈口的宽度。放胶组宫内粘连的比率明显低于单纯手术一组(6% vs 22%,p<0.05),且第1组宫内中重度粘连的形成率明显低于第2组(33% vs="92%).此外,相对于第2组,第1组宫颈内口的改善率(41.9%vs18.2%),明显好转(p">0.05)。但需要进一步的证据来证明。
4.实时脉管流速监测仪:
宫腔镜术中监测液体进入体循环的速率要比监测液体的丢失量更重要。因为丢失量是到监测时进入病人体循环总的量,而不能动态的反应液体的吸收,液体的吸收速度有可能骤升骤降,如果我们知道液体的吸收速率,那么我们就可以在液体的丢失量不多,而液体的吸收速率上升时,提前采取措施;而在液体吸收量增加,液体速率下降时,照常进行手术。Atul Kumar等【12】从1993年3月到2010年2月共使用人工脉管流速监测泵进行了966例宫腔镜手术.之前监测时,需要一位额外的助手去计算,现在采用脉管流速监测控制器代替了那位助手,可以在显示器上实时,动态的描记出液体的丢失速率。从2010年5月到2011年8月,共使用该仪器进行了41例宫腔镜手术。手术皆顺利,液体平均丢失量为105(55–357)ml,平均手术时间为24(11-41)min。
三、规范治疗:
1.子宫内膜息肉:
AAGL搜集了1951年到2010年medline与embase上有关子宫内膜息肉的文献,并通过美国预防服务工作组的标准进行了回顾,在临床表现上:B水平(结论基于有限的研究)证据的结论有:年龄增长、服用它莫西芬、不育是子宫内膜息肉的高危因素;有内膜息肉的妇女,最常见的症状是异常子宫出血;随年龄增长,息肉恶变并不增长,但服用它莫西芬,有异常出血的症状能提高恶变的可能;A(结论基于充分的证据)水平的证据有:在25%的患者,息肉有可能会自然消退,尤其是小息肉(<10mm)。在诊断上:皆为b水平证据:经阴道超声能为子宫内膜息肉的检出提供较可靠的依据,有条件时应进行该项检查;彩色能提高经阴道超声检出子宫内膜息肉多的几率;增强宫内对比(不论有无3d超声),皆能提高子宫内膜息肉的诊断水平;盲视下的诊刮或活检不应用于子宫内膜息肉的诊断。而宫腔镜有可能是个不错的选择。治疗:a水平的证据:保守治疗对于无症状的小息肉是可以的;对于不育的患者,进行宫腔镜息肉切除术后,不论是自然受孕还是及进行辅助生殖都能提高受孕的几率;a水平的证据药物治疗目前尚不推荐;宫腔镜息肉切除术是仍治疗的金标准;对于有症状的绝经后患者,应进行组织学检查;c水平(证据是基于专家们之间的共识)的结论:目前不同的宫腔镜息肉切除术的临床结尚无不同;由于创伤更小,花费更低,对患者的危险更小,宫腔镜下息肉移除术要先于息肉切除术使用。对将来研究的建议:对于异常子宫出血行息肉切除术的患者,进行临床随机对照试验;不同子宫息肉去除术的花费比较;药物治疗子宫内膜息肉(包括炔诺酮宫内缓释系统)的随机对照试验;对于绝经后患者息肉恶变的多中心前瞻性研究,宫腔镜息肉切除术后的内膜息肉的复发率的前瞻性研究【13】。
2.子宫平滑肌瘤:
AAGL对于子宫平滑肌瘤进行了类似于息肉的总结,其中A水平:对于平滑肌瘤导致的不育,尽管术后生育率会提高,但仍会低于子宫正常的人群;制定治疗方案时要考虑到50岁以下的患者,粘膜下肌瘤恶变率极低;宫腔镜、超声子宫造影和MRI对于粘膜下肌瘤诊断的特异性和准确性都很高,而子宫输卵管造影对于诊断粘膜下肌瘤的特异性却低于前3者,经阴道超声的准确性与特异性也低于宫腔镜与超声子宫造影;在揭示肌瘤与子宫的肌层和浆膜的关系时,MRI要好于其它几种检查;对于2型粘膜下肌瘤和月经过多,同时有没有生育要求的患者,子宫内膜剥除术是一有效的治疗方法;宫腔镜肌瘤切除术前进行宫颈准备,能减少括宫的要求和子宫的损伤,可以术前使用昆布类和前列腺素类的药物,也可以术中行宫颈旁注射稀释的血管加压素;术前使用GnRHa有利于减轻粘膜下肌瘤术前的贫血;以下是基于B水平的证据:粘膜下肌瘤能导致月经过多,详细机制仍不明确,增加早孕流产的风险,LNG-IUS 能减少粘膜下肌瘤的发生;如果患者没有症状,且不打算生育,可以观察;含有孕激素的激素治疗,如口服孕激素、LNG-IUS或醋酸甲羟孕酮可以治疗异常子宫出血,延缓粘膜下肌瘤的生长;肌瘤剥除器械对于粘膜下肌瘤周围子宫内膜的影响尚不清楚;使用GnRHa的目的应是缩短手术时间,减少膨宫液的吸收以及肌瘤残留的几率;对于有生育要求的患者,当肌瘤数目大于3个,或肌瘤位于宫腔镜切除会损伤大片子宫内膜的位置时,应采用经腹入路手术;术后出血可用卡孕栓或球囊宫腔压迫处理;严格计算液体丢失量,尤其是使用监测系统,并遵循协会之前制定的液体丢失标准可以减少膨宫液引起的并发症; 单极电切时将外鞘紧靠在宫颈上;当不接触组织时,不启动电切,确保电极和周围隔离,减少使用高压电流的次数,会减少生殖道灼伤的机会;多个肌瘤切除术后,宫腔内的粘连更常见,在这种情况下,如果不育,二探并行粘连松解术是很必要的;以下是基于C水平的证据:异常子宫出血,且近绝经年龄的患者可以GnRHa提前绝经;如果患者有生育要求,那么不应进行栓塞和射频、冷冻、阻抗等肌瘤剥除治疗;宫腔镜术者应熟悉电外科的知识,使用单极时要注意电解质液的使用;当治疗深部的2型粘膜下肌瘤时,可以联合腹腔镜和超声;手术时,如果肌瘤对面的内膜没有切除,可以减少粘连的形成;对于术后粘连的患者,可以二探治疗【14】; Casadio P等【15】挑选了13位单个且≤5cm二型子宫平滑肌瘤的患者,而没有考虑肌瘤在肌层的游离缘;在术中采用B超等监测肌瘤肌层游离缘的变化;对于有经验的术者,II型肌瘤的切除可以不用考虑距子宫肌层游离缘;每次当切除的时候,肌瘤的游离缘就会上升。
Alyssa S.W. Wong【17】经宫颈向病变内注射血管加压素,采用一支 (20units,1mL) 血管加压素采用生理盐水稀释50mL ,注射器抽取10mL (4units) 的稀释液注入肌瘤,采用取卵针经过2.9-mm宫腔镜 (Karl Storz)的操作通道注入病变,电切时间3到32分钟,4例无液体吸收;时间最长,液体吸收为1000mL的1例为多发黏膜下肌瘤,包括一个直径5cm的2型肌瘤.所有病例均完整切除病变,并且出血少,视野清晰,无并发症发生。
3.宫颈上皮内瘤变:
Johannes Ott等【18】挑选了442位因宫颈上皮内瘤变进行宫颈转化区loop切除(LLETZ)的患者,同时进行宫腔镜检查;评估了手术的并发症和宫腔镜发现的B超未检出的子宫病变,28/442(6.3%)患者宫腔镜检查和/或同时进行的诊刮病理发现20例良性内膜息肉,2例宫颈息肉,1例子宫内小肌瘤,5例先天畸形(包括纵膈、弓形和单角子宫)但有38例(8.6%)患者出现了并发症,有2例与诊断性宫腔镜有关的是子宫穿孔(0.5%). 因而不建议对于LLETZ术的同时常规进行宫腔镜检查。
4.重度的Asherman综合症:
Erinn M. Myers等【19】对12位因重度Asherman而闭经的患者,手术前后口服E24–6mg qd4w,如果子宫内膜小于4mm,则继续服用到第8周,增加内膜的厚度, 术中在超声监护下进行粘连松解术,术中宫腔底部放置一三角形的球囊,术后3-7天移除,同时放入宫内节育器,继续口服E2,至术后4-10周,停药时移除宫内节育器。所有患者恢复了月经,小于39岁的9位患者中,有6位(67%)怀孕,其中4人足月产。对于重度的Asherman综合症的患者,应进行全面的管理。
AAGL【20】的C级的证据有:一些宫腔粘连采用期待治疗是可以的,目前没有证据支持采用盲法下的宫颈探查、诊刮,有症状的宫腔粘连患者可以在宫腔镜引导下进行治疗,致密广泛的粘连应有有经验的医生进行手术,没有严格的研究方案之前,不能轻易使用改善内膜血流的药物,没有证据支持宫腔粘连手术前、术中或术后可以或不可以使用抗生素,开腹手术应该作为宫腔镜手术失败后的最后方法,因为对内膜的抑制和炎症反应,不论曼月乐、铜环还是T型环都不能用于粘连分离术后,只有非常有限的数据支持粘连分解术后放置Foley导尿管或IUD,由于潜在的感染风险,除临床试验外,不建议使用。
B级的证据:宫腔镜直视下分离宫腔粘连,没有证据支持联合外部影像设施或腹腔镜监护能预防穿孔或改善临床结局,但如果合理使用,会将穿孔造成的损害降到最低,术后加或不加孕激素的雌激素治疗会降低宫腔粘连的复发。而在A级的证据中:屏障,例如透明质酸和自体交联透明质酸可能会降低粘连复发的风险,有益于粘连的治疗;但是由于对治疗后妊娠率的影响尚不清楚,目前不建议在严格的试验方案外使用。
5. T-型子宫:
Herve Fernandez等【21】对97例T型子宫合并不育的患者进行单极或双极由子宫角垂直切到子宫峡部直到子宫腔呈双侧对称的三角形,切口的深度不能超过5–7mm,并于2月后进行二探。术后48位(49.5%)患者怀孕57次。流产率由78%降到27%,活产率由0%增加到73%9%。宫腔镜下子宫成形术可以明显改善合T型子宫合并不育患者的妊娠率。
四、在生殖医学中的应用:
1.用于不孕患者的评估:
Herrera等【22】用宫腔镜检查不孕妇女1286例,38%有子宫因素,67%的HSG解释错误,IVF失败病例中38%宫腔镜检查有宫腔病变。所以宫腔镜应为不孕妇女的初始常规检查。Feghali等研究IVF前宫腔镜诊断的价值,回顾分析145例在第1个周期前宫腔镜检查的结果,发现45%宫腔有异常,包括子宫内膜炎、内膜息肉和肌瘤,内膜病变最常见。上述病变治疗后,妊娠率与正常宫腔同。子宫内膜炎用抗生素治疗,40%下一个月妊娠。故宫腔镜应作为IVF前的常规检查,可改善妊娠率。Elif Aylin Ta等对比了将359例不孕患者前同时进行宫腔镜和子宫输卵管造影(HSG)的检查,HSG的灵敏度为21.56%,特异性为83.76%,阳性预测值为55.26%,阴性预测值为70.75%。假阴性率为78.43%,假阳性率为16.23%。二者总的一致率为68.9%。并且宫腔镜检查异常的危险度随着患者年龄和不育时间的延长而升高。大于35岁的患者,尽管造影正常,但是之前进行过辅助生育的次数却增高。而在男性因素的不孕群体中,异常宫腔镜检查异常的危险度却下降。因而大于35岁和/或有两次以上接受辅助生育治疗失败的患者,即使是HSG正常,也应该行宫腔镜检查。
2.用于生殖医学方面的治疗:
Shang Yu Huang等【23】人对30位对促排卵方案反应好,但胚胎植入失败两次以上的患者,在促排卵的第4到7天,在患者的子宫内膜后壁距宫底10-15mm处活检造成小损伤后,再植入胚胎,30位患者都妊娠成功,妊娠率100%,而有相同症状的另外24例未进行活检的患者中妊娠率为46%。
3. 宫腔镜引导下宫角深部受精技术:
精子数量低于相应的阈值会影响受精,经直肠(TRG)和宫腔镜(HYS)引导下受精,当宫角深部注入1*106 个精子时, HYS(10/13,77%)与TRG(11/15,73%)之间的受孕率没有差别(P<0.10) ;当精子数量降至0.5*106时,HYS(3/15,20%)和TRG(4/13,31%)之间的受孕率仍无差别(P<0.10);联合受孕率分别为HYS13/28(46%),TRG15/28(54%),(P<0.10). 宫角深部采用阈值以下的精子数量受精时,采用不同的技术受孕率没有明显的差别。
4. 排卵日宫腔镜手术:
子宫内膜息肉在不孕患者中发生率为14.9%到26.5%,传统的超声检查,小的子宫内膜息肉可以漏诊,偶尔,在IVF周期刺激卵巢的治疗中会检测到子宫内膜息肉【24】:30岁不孕患者诉月经过多、不孕,超声提示2.6*1.4cm粘膜下肌瘤,门诊宫腔镜提示子宫左侧壁粘膜下肌瘤,随后20分钟内完成了子宫肌瘤剔除术,3周后因停经就诊,尿妊娩阳性,TVS见到一个1.62cm 妊娠囊,从BBT与妊娠囊的大小推测排卵在手术当天,40周时娩一2600g 男婴。第二例,30岁女性,6次诊刮后不孕2年,门诊宫腔镜见子宫上壁AFS分类的中度宫腔粘连形成,随后进行了15分钟的宫腔镜手术,患者因呕吐和停经4周后返回医院,超声提示6周的胚胎 ,从胚胎的大小看, 手术应该是在排卵日前后进行。因而,如果在IVF周期卵巢刺激的过程中发现了子宫内膜息肉,可以不用取消周期进行宫腔镜手术。
另有研究表明,宫腔镜可以通过扩张宫颈管、评估宫颈管和宫腔的方向、明确子宫的形状和宫腔深度降低胚胎移植的难度。此外,宫腔镜检查造成轻度的内膜损伤并引起损伤后的炎症反应 ,能引起细胞因子和生长因子的释放,炎症反应可能有利于内膜为植入做准备。
五、在计划生育中的应用:
1.绝育:
女性绝育术式有多种,随着宫腔镜的广泛开展,宫腔镜下绝育也渐渐成为可能。美国FDA分别于2002年和2009年通过了Essure?与Adiana?宫内绝育装置,Essure装置【25】是一个4cm带有弹性的微型螺丝圈,这一螺丝圈有一个不锈钢的内圈,一个含镍的有弹性的内圈,加上聚酯合成纤维构成。输卵管插管成功后,将线圈放入输卵管的近端,撤出插管。宫腔镜或摄片证实置入成功。 线圈内的聚酯纤维可引起3-4cm的输卵管的良性的慢性炎症和纤维化,最终使装置固定,并具有绝育作用。
而Adiana【26、27】首先通过射频使得输卵管上皮受损,随后在该部分放入一个3.5-mm 硅树脂模型。患者对这两种绝育器的满意度很相近。Essure需要生理盐水作为膨宫液,而adiana需要非离子化的膨宫液,因而液体负荷多,低钠血症的风险要高于Essure;Essure用于产后6周以后,而Adiana用于产后12周以后,Essure的主要优势是临床试验中的失败率为0%,如果放置得当,在6个月内输卵管的阻塞率为100%;而Essure的弱点是输卵管穿孔率和装置的排除率高,而且Essure的长度与侵入输卵管基质的深度要高于Adiana,所以对于输卵管痉挛的患者来说,操作难度要高,不过总体来说ESS305与Adiana 的植入率96.9% vs 94.7%没有大的差异。相对于Essure,Adiana的主要优点是输卵管远端梗阻与输卵管痉挛等患者,易于植入Adiana。目前尚未有Adiana导致的输卵管穿孔与装置排除的报道【28】,但在临床试验中有一例患者【29】植入Adiana后因异位妊娠而行手术治疗。B Povedano等【30】回顾分析了2003-2010年4306例置入Essure绝育装置的患者,其中4108位患者完成了3个月的随访方案。有115位患者出现了并发症,但是无需要住院治疗的患者,血管迷走反应是最主要的并发症,发生了85例(2.0%) ,有19例患者节育装置脱出, Ted L. Anderson等【31】回顾了645位置入Adiana的患者,置入后的第24、36个月的避孕率为98.7%。其中3例是子宫输卵管造影错误造成的,另外3例是置入的方法错误造成的。并发症率较低。
2.输卵管近端梗阻:
Keiko Mekaru等【32】搜集了61例腹腔镜诊断为单侧或双侧输卵管近端梗阻的患者,并由输卵管造影证实。其中35位患者的54条输卵管做了输卵管复通术。平均每条输卵管的成功率为25.9% (14/54),每位患者的成功率为37.1% (13/35)。 保留输卵管的患者中4例妊娠,其中1例为输卵管妊娠,1例流产。在61位患者中,除14位腹腔镜术后进行了IVF–ET, 13例怀孕(27.7%), 9 例活产,1例输卵管妊娠,3例流产。故而宫腹腔镜联合输卵管复通术对于输卵管性不孕未进行IVF–ET的患者是一个不错的选择。另一项门诊宫腔镜下输卵管通液中【33、34】,35例已预订腹腔镜下输卵管通液的不孕患者,82.9% 与腹腔镜下输卵管诊断相符;阳性预测值87.5%,阴性预测值76.7%。在宫腔镜下近端输卵管梗阻复通术中,70例不孕的近端输卵管梗阻患者,宫腹腔镜联合近端输卵管复通术,通过电话和问卷调查搜集术后信息。复通成功率:71.4%/人次,67.0%/管次;总的妊娠率是:55% /管次;复通术后从自然妊娠或克罗米芬诱导排卵到成功妊娠的时间大约:10.5±8.9月。
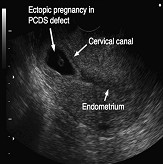
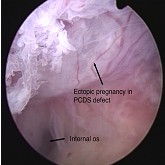
3.剖宫产瘢痕处妊娠:
两位患者,一位阴道无痛性出血3天,另一位瘢痕子宫术后随访,经阴道超声在瘢痕处分别可见2.1cm和1.9cm的孕囊,Yu Chang等放入阴道窥器后在宫颈4点和8点处分别向间质内注入10 mL稀释的血管加压素溶液(0.4U/mL;20u用50mL液体稀释) 。扩张宫颈后,识别寻找孕囊组织,随后用90度的电切环冷切除。电极旋转180度后将孕囊组织与子宫前壁分离,手术时间分别为20、18分钟,hCG水平分别在35、32天降至正常,在术后第一个月经周期,测得瘢痕缺陷的深度分别为9.7、6.5mm,上述病例行宫腔镜联合血管加压素宫旁注射治疗安全、有效。【35】
4. 清除残留的蜕膜组织:
Daniel T. Rein等【36】对95位终止妊娠后蜕膜残留患者的不同处理进行了评估:其中42位患者扩宫后进行了超声引导下的刮宫,另53位使用4mm的环状电切镜进行了清除;术后宫腔镜组有2例宫腔粘连(4.2%),而刮宫组有12例宫腔粘连(30.8%) (其中7例轻度粘连, 3 例单处致密粘连,1例广泛粘连1). 宫腔镜组的怀孕率为68.8%,而刮宫组为59.9% ;在小于35岁的患者中,宫腔镜组明显高于刮宫组 (78.1% vs 66.6%),差异具有统计学意义。宫腔镜手术的患者受孕时间也明显缩短(11.5月vs14.5月)。对于终止妊娠后蜕膜残留的患者,宫腔镜下清除蜕膜组织,妊娠率明显高于刮宫手术。
5.剖宫产瘢痕憩室:
Giampietro Gubbini等【37】对41位剖宫产瘢痕憩室合并不孕的患者进行了宫腔镜处理;术后1-2年内37位(90.2%)再次妊娠,并通过剖宫产分娩;4位(9.8%)患者在怀孕早期自发性流产。故而,宫腔镜憩室切除术对于保留、恢复剖宫产瘢痕憩室合并不育患者的不错选择。
6.胎盘植入:
胎盘异常侵入会导致部分性胎盘植入,常导致异常阴道出血或影响胚胎着床。B超多表现为:子宫和胎盘组织的界限不清,
在正常灰度图上不能辨认,有丰富的血流。在宫腔镜下宫腔和残留胎盘组织间的裂隙平面消失,应该和滋养层组织单纯的宫腔残留区别: 能容易的观察到裂隙层面,并且组织能通过刮宫或宫腔镜下不用电切成功去除 。手术时,宫腔镜下双极电切可以减少围术期出血,当看到浅肌层组织时,应该停止电切。术后应避孕6周,可以口服避孕药,6周后宫腔镜二探 /经阴道超声/ 或水超声。【38】
六、宫内组织粉碎器:
1.息肉与肌瘤:
Emanuel MH 和 Wamsteker K【39】报告用Collins电极在覆盖肌瘤的子宫内膜上作椭圆形切口,切口位置在肌瘤基底向宫壁翻转处,直至露出肌瘤,切断肌瘤周围的肌纤维,使肌瘤几乎全部突出于宫腔,有利于完全切除肌瘤。44例用此法完成了41例(93.1%),其中38例(92.6%)肌瘤24cm,3例(7.4%)>4cm。平均手术时间27min(10-45min)。此法适用于大部分位于肌壁间的肌瘤切除。2005年,美国食品与药品监督管理局同意TRUCLEARTM宫腔内粉碎器用于宫腔内病变的治疗,Emanuel和同事们【40】进行了一项对比研究,粉碎器和电切镜手术时间息肉平均为8.7min vs 30.9 min, 0型和1型肌瘤为16.4min vs 42.2min。使用TRUCLEARTM宫腔内粉碎器治疗了315位病人,其中37位进行了肌瘤粉碎,平均手术时间18.2min,灌流液缺失是440mL,有2位病人是2型肌瘤,转电切去除,278位患者进行了息肉手术,平均手术时间6.6min。所有的手术都顺利进行并可在切除肌瘤的同时吸出肌瘤碎片,手术视野清楚,避免了为取出肌瘤碎屑而多次进出电切镜导致的空气栓塞,明显减少了体液超负荷,低钠血症,子宫穿孔和等严重并发症。对于息肉和小于3 cm的0型和1型肌瘤,粉碎器手术安全有效。2009年,美国食品与药品监督管理局有通过了第二款宫内组织移除设备MyoSureR。Miller和同事【41】用该设备粉碎息肉的平均时间为37秒,粉碎0型、1型和2型肌瘤的平均时间为6.4min,肌瘤的平均直径为31.7mm,相对于TRUCLEARTM,MyoSureR直径更小,切割速度更快,更便于门诊手术时使用。
2.子宫纵膈:
除了息肉与肌瘤,Michiel Simons等用粉碎器来移除子宫纵膈,一位34岁,习惯性流产的患者,G4P0,超声检查提示子宫纵膈合并双角子宫,HSG的结果见下图:
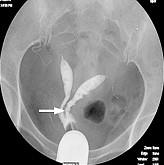
超声下子宫纵膈到达宫颈内口,纵膈下半部未见明显血流信号,未发现泌尿系畸形。采用truclear设备在腰麻下进行,第一刀切在纵膈中部,随后移除纵膈的前壁和后壁,直到完全移除或见到血流。向宫底方向切除,直到出现血流(共切除了2cm的纵膈)。手术时间23min,灌流液丢失270mL,出血<100ml。病理未见非典型增生。7周后二探,见一小纵膈和双角子宫。

随着设备的不断改进,技术的不断提高,培训的不断规范,近年来宫腔镜技术有犹如雨后春笋,蓬勃发展,在妇科产临床中应用的领域也在不断扩大,必将有着更加广泛的前景。
参考文献
【1】. Paoletti R, Di Spiezio Sardo A, Spinelli M ,et al. Hysteroscopic Diagnosis of Endometrial Vascular Dystrophy.Journal of Minimally Invasive Gynecology, 2012,19(5):543-4
【2】. Talamonte VH1, Lippi UG, Lopes RG ,et al. Hysteroscopic findings in patients with post-menstrual spotting with prior cesarean section. einstein. Einstein (Sao Paulo). 2012;10:53-6
【3】. Lasmar RB1, Lasmar BP, Celeste RK ,et al.A New System to Classify Submucous Myomas: A Brazilian Multicenter Study. Journal of Minimally Invasive Gynecology . 2012, 19, 575–580
【4】. Ranjit Manchanda, Ertan Saridogan ,Ahmed Abdelraheim, et al.Annual outpatient hysteroscopy and endometrial sampling (OHES) in HNPCC/Lynch Syndrome (LS).Arch Gynecol Obstet (2012) 286:1555–1562
【5】. Florio P, Filippeschi M, Imperatore A, et al. The practicability and surgeons' subjective experiences with vaginal danazol before an operative hysteroscopy. Steroids. 2012, 77 :528–533
【6】. Cicinelli E, Pinto V, Quattromini P , et al. Endometrial Preparation With Estradiol Plus Dienogest (Qlaira) for Office Hysteroscopic Polypectomy: Randomized Pilot Study. J Minim Invasive Gynecol. 2012 ,Epub ahead of print.
【7】. Barrueto FF, Audlin KM. The use of narrowband imaging for identification of endometriosis. J Minim Invasive Gynecol 2008;15(5):636–9.
【8】. Kisu I, Banno K, Kobayashi Y, et al. Flexible hysteroscopy with narrow band imaging (NBI) for endoscopic diagnosis of malignant endometrial lesions. Int J Oncol 2011;38(3):613–8.
【9】.Kids I, Banno K, SusumuN, etal.Magnifying hysteroscopy with narrow-band imaging for visualization of endometrial lesions. Int J Gynaecol Obstet. 2011 ,115:74-5
【10】. Raffaele Tinelli, Daniela Surico, Livio Leo ,et al. Accuracy and efficacy of narrow-band imaging versus white light hysteroscopy for the diagnosis of endometrial cancer and hyperplasia: a multicenter controlled study. The North American Menopause Society.2012, 18:1026-1029
【11】. Valerio Mais , Maria G. Cirronis,Michele Peiretti ,et al.Efficacy of auto-crosslinked hyaluronan gel for adhesion prevention in laparoscopy and hysteroscopy: a systematic review and meta-analysis of randomized controlled trials. European Journal 2 of Obstetrics & Gynecology and Reproductive Biology.2012,160:1–5
【12】. Attilio Di Spiezio Sardo, Marialuigia Spinelli, Silvia Bramante, et al. Efficacy of a Polyethylene Oxide–Sodium Carboxymethylcellulose Gel in Prevention of Intrauterine Adhesions After Hysteroscopic Surgery. Journal of Minimally Invasive Gynecology.2011,18:462-468
【13】. Lasmar RB1, Lasmar BP, Celeste RK et al. New Hysteroscopy Pump To Monitor Real-Time Rate of Fluid Intravasation. Minimally Invasive Gynecology.2012,19:369-75
【14】. AAGL Advancing Minimally Invasive Gynecology Worldwide. AAGL practice report: practice guidelines for the diagnosis and management of endometrial polyps. J Minim Invasive Gynecol. 2012 ,19 :3-10
【15】. AAGL Advancing Minimally Invasive Gynecology Worldwide. AAGL practice report: practice guidelines for the diagnosis and management of endometrial polyps. J Minim Invasive Gynecol. 2012 ,19 :152-71
【16】. Casadio P, Youssef AM, Spagnolo E, et al. Should the myometrial free margin still be considered a limiting factor for hysteroscopic resection of submucous fibroids? A possible answer to an old question. Fertil Steril. 2011,95:1764-8.
【17】. Alyssa S.W. Wong et al. Transcervical Intralesional Vasopressin Injection in Hysteroscopic Myomectomy—Description of a New Technique. Journal Of Laparoendoscopic & Advanced Surgical echniques,2013.23:258-260
【18】. Johannes Ott, Birgit Jatzko, Zoltan Nemeth,et al. Is routine hysteroscopy during LLETZ a valuable additional procedure? . AOGS. 2011 ,90: 1284–1286.
【19】. Erinn M. Myers, Bradley S. Hurst.Comprehensive management of severe Asherman syndrome and amenorrhea. Fertility and Sterility.2012, 97:162-165
【20】. AAGL Practice Report: Practice Guidelines for Management of Intrauterine Synechiae
【21】. Herve Fernandez, Olivier Garbin, Vanina Castaigne,et al. Surgical approach to and reproductive outcome after surgical correction of a T-shaped uterus. Human Reproduction, 2011,26:1730–1734
【22】. Elif Aylin Ta?sk?n, Bulent Berker, Batuhan Ozmen, et al. Comparison of hysterosalpingography and hysteroscopy in the evaluation of the uterine cavity in patients undergoing assisted reproductive techniques. Fertility and Sterility.2011,96:349-352.
【23】. Huang SY, Wang CJ, Soong YK, et al. Site-specific endometrial injury improves implantation and pregnancy in patients with repeated implantation failures. Reprod Biol Endocrinol.2011, 9:140
【24】. Lin YH1, Huang LW, Seow KM, et al. Hysteroscopic surgery can be performed around the day of ovulation without affecting implantation.Taiwanese Journal of Obstetrics & Gynecology .2012.51: 469-470
【25】. Essure? Permanent Birth Control System [instructions for use]. Mountain View, CA: Conceptus, Inc.; 2002.
【26】. Vancaillie TG, Anderson TL, Johns DA. A 12-month prospective evaluation of transcervical sterilization using implantable polymer matrices. Obstet Gynecol. 2008;112:1270-1277
【27】. Adiana? Permanent Contraception Instructions for Use and Radiofrequency Generator Operator’s Manual. Bedford, MA: Hologic, Inc.; 2009.
【28】. Connor VF. Essure: a review six years later. J Minim Invasive Gynecol. 2009;16:282-290.
【29】. Adiana Permanent Contraception System Summary of Safety And Effectiveness Data: PMA P070022.2010.
【30】. Povedano B1, Arjona JE, Velasco E, et al.Complications of hysteroscopic Essure_sterilisation: report on 4306 procedures performed in a single centre. BJOG. 2012
【31】. Ted L. Anderson, Thierry G. Vancaillie, et al. The Adiana System for Permanent Contraception:Safety and Efficacy at 3 Years. Journal of Minimally Invasive Gynecology,2011,18612-616
【32】. Keiko Mekaru ,Chiaki Yagi , Kozue Asato,et al. Hysteroscopic tubal catheterization under laparoscopy for proximal tubal obstruction. Arch Gynecol Obstet .2011, 284:1573–1576
【33】. T?r?k P1, Major T. Accuracy of Assessment of Tubal Patency With Selective Pertubation at Office Hysteroscopy Compared With Laparoscopy in Infertile Women. Journal of Minimally Invasive Gynecology.2012:19, 627–630
【34】. Chung JP, Haines CJ, Kong GW.Long-term reproductive outcome after hysteroscopic proximal tubal cannulation- an outcome analysis. Australian and New Zealand Journal of Obstetrics and Gynaecology 2012, 52: 470–475
【35】. Yu Chang, Nari Kay, Yung Hung Chen, et al . Resectoscopic treatment of ectopic pregnancy in previous cesarean delivery scar defect with vasopressin injection. Fertil steril.2011,96(2):e80-2
【36】. Daniel T. Rein, Torsten Schmidt, Alexandra P. Hess, et al. Hysteroscopic Management of Residual Trophoblastic Tissue Is Superior to Ultrasound-Guided Curettage. J Minim Invasive Gynecol. 2011, 18:774–778
【37】. Giampietro Gubbini, Gabriele Centini, Daniela ascetti,et al. Surgical Hysteroscopic Treatment of Cesarean-Induced Isthmocele in Restoring Fertility: Prospective Study. J Minim Invasive Gynecol. 2011,18: 234–237
【38】. Nisolle M1, Delbecque K, Perrier D'Hauterive S, et al. Hysteroscopic resection of abnormally invasive placenta residuals. ActaObstet Gynecol Scand 2013; 92:451–456
【39】. Emanuel MH, Wamsteker K. The Intra Uterine Morcellator: a new hysteroscopic operating technique to remove intrauterine polyps and myomas.J Minim Invasive Gynecol. 2005;12:62-66.
【40】. T .W.O.Hamerlynck,V.Dietz,B.C.Schoot. Clinical implementation of the hysteroscopic morcellator for removal of intrauterine myomas and polyps.A retrospective descriptive study. Gynecol Surg .2011, 8:193–196
【41】. Miller C, Glazerman L, Roy K, Lukes A. Clinical evaluation of a new hysteroscopic morcellator—retrospective case review. J Med. 2009;2:163-166.
 妇产科在线APP下载
妇产科在线APP下载












