【摘要】背景 子宫瘢痕妊娠是严重的孕早期并发症,随着二孩政策的放开,剖宫产率居高不下,子宫瘢痕妊娠发病率增高。目的 探讨不同治疗方法终止剖宫产术后子宫瘢痕妊娠(CSP)的应用价值及安全性。方法 回顾性分析2013年4月—2017年12月在安徽理工大学第一附属医院(淮南市第一人民医院)住院的44例CSP患者的病历资料,其中A组(n=16)选择子宫动脉栓塞联合B超引导下清宫术,B组(n=14)选择经阴道妊娠物清除及子宫瘢痕修补术,C组(n=14)选择甲氨蝶呤联合米非司酮药物杀胚后B超引导下清宫术。比较3组患者的年龄、妊娠次数、剖宫产次数、停经时间、术前血人绒毛膜促性腺激素(HCG)水平、术中出血量、手术时间、术后阴道流血时间、抗生素使用时间、住院时间、术后血HCG水平降至正常时间及并发症发生情况。结果 3组CSP患者的年龄、妊娠次数、剖宫产次数、停经时间、术前血HCG水平比较,差异均无统计学意义(P>0.05)。3组患者术中出血量、手术时间、术后阴道流血时间、抗生素使用时间、住院时间比较,差异有统计学意义(P<0.05);术后血HCG水平降至正常时间比较,差异无统计学意义(P>0.05)。术中出血量,A组<C组<B组(P<0.05);手术时间,A、C组<B(P<0.05);术后阴道流血时间,A组<C组(P<0.05);抗生素使用时间,A组<B组(P<0.05);住院时间,A、B组<C组(P<0.05)。3组术中无一例子宫穿孔、人工流产综合征、大出血、膀胱损伤及子宫切除,术后无一例药物性肝肾损害及白细胞计数下降。结论 子宫动脉栓塞联合B超引导下清宫术微创、安全,但有妊娠需求者慎选;经阴道妊娠物清除及子宫瘢痕修补术根治性强,但风险高;药物杀胚后B超引导下清宫术微创安全,但住院时间长。对于CSP的终止,应结合患者自身情况及不同生育需求制定个体化治疗方案。
【关键词】子宫瘢痕妊娠;剖宫产术;子宫动脉栓塞术;经阴道妊娠物清除;子宫瘢痕修补术;清宫术
随着二孩政策的放开,前次剖宫产的女性再次妊娠面临潜在的风险——子宫瘢痕妊娠等并发症,严重威胁女性的生殖健康[1-3]。剖宫产术后子宫瘢痕妊娠(cesarean scar pregnancy,CSP)是一种特殊的异位妊娠,指受精卵着床于前次剖宫产子宫切口瘢痕处[4]。瘢痕组织相对子宫肌层薄且弹性差,着床在此处的妊娠囊继续生长可能穿透子宫肌层甚至侵犯膀胱,诱发大出血、子宫破裂、休克等,一经确诊需及时终止妊娠。如何安全地终止妊娠,有效减少围术期出血,降低子宫切除风险一直是临床研究的重点。近年来临床治疗多采用经阴道或宫腹腔镜下瘢痕妊娠物切除等手术治疗,疗效确切但手术风险大;也有采用甲氨蝶呤等药物杀胚保守治疗,疗效不及手术。本文对安徽理工大学第一附属医院(淮南市第一人民医院)2013年4月—2017年12月住院治疗的CSP患者的资料进行回顾性分析,探讨微创而有效地终止CSP的方法。
1对象与方法
1.1 研究对象 选取安徽理工大学第一附属医院(淮南市第一人民医院)妇产科2013年4月—2017年12月住院诊断为CSP且符合纳入排除标准者44例,年龄22~45岁,平均(32.9±4.9)岁,停经35~65 d,平均(48.0±6.6)d。本研究经过安徽理工大学第一附属医院(淮南市第一人民医院)伦理委员会审核并批准,纳入者均根据自身治疗意愿签订知情同意书。
1.2 纳入与排除标准 纳入标准:经阴道彩超确诊为CSP,自愿接受治疗;入院后血常规、凝血功能、肝肾功能、心电图、胸部X线片等基本在正常范围;生命体征平稳;无高血压、心脏病、糖尿病等内科合并症。排除标准:合并子宫肌瘤、子宫畸形者。
1.3 治疗方法 根据患者意愿将治疗分为3组,A组(n=16)给予数字减影血管造影(DSA)下子宫动脉栓塞介入治疗,72 h内行B超引导下清宫术;B组(n=14)行经阴道妊娠物清除及子宫瘢痕修补术;C组(n=14)给予甲氨蝶呤联合米非司酮药物联合杀胚治疗,1周后行B超引导下清宫术。所有患者入院常规备血。A组:于患者右侧腹股沟区消毒铺巾进行局部麻醉,行Seldinger技术于右侧股动脉先后置入5F导管鞘及5FC2导管,运用导管导丝技术,先行左侧子宫动脉DSA,于透视下经导管缓慢推注高压明胶海绵适量,栓塞子宫动脉,直至铸型,再用1枚2 mm×2 mm明胶海绵颗粒加强栓塞。于腹主动脉下段成袢后,同法栓塞右侧子宫动脉。术毕拔管,穿刺处加压包扎,右下肢制动6 h。术后72 h内在超声引导下行清宫术。B组:常规外阴消毒铺巾,于膀胱宫颈附着处稍下方注射含缩宫素10 IU溶液10 ml,切开宫颈阴道部前壁黏膜,剪刀分离膀胱宫颈间隙,示指于间隙内向上及两侧分离,将膀胱自宫颈前壁推开直达膀胱子宫腹膜反折,剪开膀胱腹膜反折,暴露位于子宫瘢痕处的妊娠包块,于包块下缘切开,用艾利斯钳夹住子宫切口边缘,7号吸引管自切口进入宫腔,吸取孕囊及周围蜕膜组织,修剪切口薄弱瘢痕组织,在扩宫棒指示下以0号可吸收缝线连续缝合子宫切口,2-0可吸收线缝合宫颈阴道黏膜层,查无活动性出血,则用碘仿纱布卷填塞阴道,术后24~48 h取出。C组:入院后予甲氨蝶呤肌内注射1次,50 mg/m2,米非司酮口服,50 mg/次、2次/d、连续3 d,1周后在超声引导下行清宫术。
1.4 观察指标 通过查阅患者病历收集3组患者资料,包括年龄、妊娠次数、剖宫产次数、停经时间、术前血人绒毛膜促性腺激素(HCG)水平、术中出血量、手术时间、术后阴道流血时间、抗生素使用时间、住院时间、术后血HCG水平降至正常时间,术中并发症(子宫穿孔、人工流产综合征、大出血、膀胱损伤及子宫切除)发生情况,术后血常规、肝肾功能及患者一般情况(发热、腹痛、双下肢感觉及远端肢体血供障碍),月经复潮后彩超复查结果(子宫内膜厚度、瘢痕、有无宫腔粘连)及随访情况(有无经期及经量改变)。
1.5 统计学方法 采用SPSS 21.0统计软件对数据进行分析。计数资料以相对数表示,进行描述性分析。服从正态分布的计量资料以 (x±s)表示,方差齐时多组间比较采用方差分析,组内两两比较采用LSD-t检验;方差不齐时多组间比较采用Kruskal-Wallis H检验,组内两两比较采用Tamhane's T2检验。以P<0.05为差异有统计学意义。
2结果
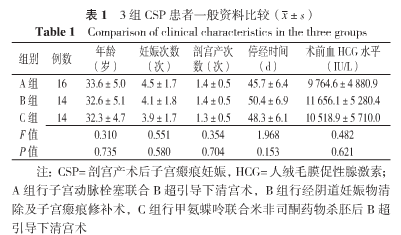
2.1 一般资料 3组CSP患者的年龄、妊娠次数、剖宫产次数、停经时间、术前血HCG水平比较,差异均无统计学意义(P>0.05,见表1)。
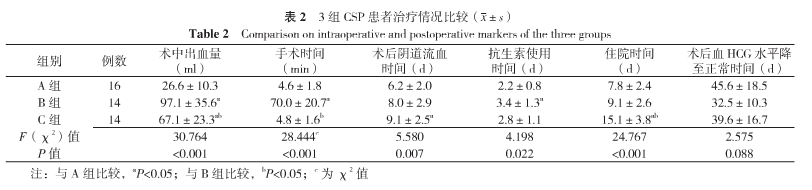
2.2 治疗情况 3组患者术中出血量、手术时间、术后阴道流血时间、抗生素使用时间、住院时间比较,差异有统计学意义(P<0.05);术后血HCG水平降至正常时间比较,差异无统计学意义(P>0.05)。术中出血量比较,A组<C组<B组(tAC=4.47,tAB=7.78,tBC=3.21;P<0.05);手术时间比较,A、C组<B组(tAB=11.81,tBC=11.77;P<0.05);术后阴道流血时间比较,A组<C组(tAC=3.30,P<0.05);抗生素使用时间比较,A组<B组(tAB=2.90,P<0.05);住院时间比较,A、B组<C组(tAC=6.72,tBC=5.27;P<0.05,见表2)。
2.3 并发症发生情况 3组术中无一例子宫穿孔、人工流产综合征、大出血、膀胱损伤及子宫切除,术后无一例药物性肝肾损害及白细胞计数下降。A组有1例患者并 发宫腔粘连,按周期口服炔雌醇环丙孕酮片3个月,症状缓解。B组术后有2例患者发热,抗感染及对症治疗后痊愈。 3组均于术后2个月内月经复潮,A组1例复潮后月经量少,复查彩超发现宫腔粘连,扩宫及药物对症治疗后缓解, 其余患者复潮后经量、经期与孕前无明显改变。
3讨论
3.1 CSP的诊断和发病机制 随着诊断技术水平的提高和剖宫产率居高不下,近年来CSP有明显上升趋势[5]。CSP具体发病机制不明,可能与剖宫产切口愈合不良有关[6],剖宫产瘢痕部位的内膜基底层缺损,形成通往宫腔的裂隙或通道,为胚胎植入提供了植入点[7]。经腹部联合阴道超声检查为诊断CSP首选方法,目前国际上沿用的诊断标准为:子宫前壁峡部剖宫产瘢痕处可见妊娠囊或包块,周围见丰富血流信号和低阻抗指数,妊娠部位的子宫前壁肌层变薄或缺损,宫腔和颈管内、附件区未见妊娠囊,子宫直肠陷凹无积液(破裂型除外)[8]。国内诊断更加细化,在原有诊断基础上,将CSP分为Ⅰ、Ⅱ、Ⅲ型[8],更有利于临床精准治疗。
3.2 CSP的治疗方法 手术治疗包括腹腔镜下、宫腔镜下、经阴道、经腹瘢痕妊娠物切除及清宫术[9],保守治疗包括子宫动脉栓塞术、射频消融或甲氨蝶呤等药物杀胚治疗。但是单纯手术治疗虽疗效确切但手术风险大,即便是微创也需在全身麻醉下完成,仍然存在手术并发症;而药物杀胚治疗过程长、失败率高,应根据患者孕龄、临床表现、CSP类型及生育需求,采用个体化方案。
3.2.1 子宫动脉栓塞联合B超引导下清宫术 该术式可以有效降低手术出血的风险,而且,明胶海绵颗粒栓塞动脉末梢,不损伤毛细血管网,子宫可通过其他交通支获得少量血供维持血运,不至于缺血坏死[10]。子宫动脉栓塞24 h后交通支恢复卵巢供血,不影响卵巢激素分泌功能。清宫术应在子宫动脉栓塞后72 h内完成,以防侧支循环建立导致清宫术中大出血[11]。A组随访有1例并发宫腔粘连,考虑是过度刮宫所致,但临床也有报道子宫动脉栓塞可能引起宫腔粘连[12-13]。
3.2.2 经阴道妊娠物清除及子宫瘢痕修补术 子宫瘢痕妊娠物清除及修补术是指在原剖宫产瘢痕部位切开子宫前壁肌层,清除妊娠囊及蜕膜组织后切除原瘢痕组织,修剪瘢痕及其周围微血管结构,重新加固缝合,能降低子宫切口憩室及再次CSP的风险[14],对于仍有妊娠需求的患者是首选治疗方案,但对术者手术水平要求高,不然再次缝合的切口仍有可能发生憩室或CSP。该手术可经阴道、开腹或腹腔镜下完成。开腹手术创伤大,腹腔镜手术受医疗器械及费用的影响不适于基层医院,阴式手术相对于开腹及腹腔镜手术更加微创,尤其适用于孕周少的患者。B组较A、C组治疗更为彻底,但是术中出血量多、手术时间长,术后感染风险相对较高,抗生素使用时间长。
3.2.3 甲氨蝶呤联合米非司酮药物杀胚后B超引导下清宫术 甲氨蝶呤是一种抗代谢药物和抗叶酸药物,能够抑制滋养细胞的生长增殖,减少中间型合体型滋养细胞的形成,导致胚胎变性坏死,从而达到治疗目的[15]。单用甲氨蝶呤治疗有效率接近80%,血清HCG水平下降较慢,存在大出血、子宫破裂的风险[16-17]。米非司酮是一种高效的孕激素拮抗剂,能与孕酮竞争孕激素受体,降低孕酮活性,促使绒毛滋养细胞变性坏死,最终导致胚胎死亡[18]。两者联用能够减少局部组织供血,降低清宫术中大出血发生率,疗效较单用更优。但是C组住院时间长于A、B组,术中出血量及术后阴道流血时间均长于A组。
综上所述,对于年轻要求保留生育功能的CSP患者,3种治疗方案均可行。子宫动脉栓塞联合B超引导下清宫术微创安全,围术期并发症少,尤其适用于盆腔粘连不宜经阴道或腹腔镜手术的患者,但是由于子宫动脉栓塞对生殖影响的不确定性[19],不能作为有妊娠需求患者的首选;经阴道妊娠物清除及子宫瘢痕修补术治疗CSP更加彻底,但对术者的手术操作技能要求高,术后感染及其他并发症的发生率相对较高;药物杀胚后超声引导下清宫术相对前两者更加微创,但是住院时间长,出血及治疗失败率高。应根据患者病情及不同需求,制定个体化治疗方案。本研究的不足在于纳入患者数量较少,并发症观察时间尚短,存在一定局限性。
作者贡献:李凡负责文章的构思、设计、统计学处理,负责文章的质量审校,并对文章整体负责;袁礼红、周萍负责数据收集、整理、分析。本文无利益冲突。
参考文献
略
 妇产科在线APP下载
妇产科在线APP下载












