十年病程,屡次复发,维持治疗在卵巢癌后线治疗中打破桎梏
时间:2021/6/7 18:22:58 作者:吴忧 李晓光
铂敏感复发 BRCA突变 HRD阳性 满意肿瘤细胞减灭术 二次减瘤术 新辅助化疗 去化疗 PARPi单药治疗*仅供医学专业人士阅读参考



 00:000:00
病例分享
00:000:00
病例分享


 00:000:00
病例点评
00:000:00
病例点评
既往卵巢癌治疗模式为初始肿瘤细胞减灭术+术后化疗或新辅助化疗+间歇肿瘤细胞减灭术+术后化疗,然而这一治疗模式难逃最终复发的厄运,且多程化疗会显著增加毒性,如何捍卫手术和化疗效果、减少卵巢癌的复发,提高患者生存率一直是亟待解决的难题。本次我们将分享一例初诊为中晚期卵巢癌患者,出现多次复发并转移,经多线治疗后应用尼拉帕利延长生存期的病例,为类似案例的治疗带去一定启示。
病例回顾
基本资料
患者女性,起病年龄55岁,慢性胆囊炎史,乙肝病毒携带(2006年),否认其他疾病病史和手术史,祖父患肺癌去世,否认其他家族肿瘤遗传病史。
治疗经过
✔第一阶段:初始手术+术后化疗+淋巴囊肿治疗
患者入院前主因“腹胀半年”,在当地医院诊为“慢性胆囊炎”并对症处理。后因“腹部膨隆伴喘憋2月”,入院前1周在当地医院行超声示:盆腔7~8 cm血流丰富肿物,大量腹水。未予处理,2010年9月10日主因“腹胀半年,发现盆腔肿物1周”至我院住院治疗。
查体:腹水征(+++)。妇科检查:盆腔左附件区可及约7~8 cm囊实肿物,活动受限,直肠窝结节不平。肿瘤标志物检测示CA-125 1228 U/ml。
影像学检查:盆腹增强CT示盆腔子宫后方囊实性肿物,双附件结构显示不清,大网膜弥漫增厚,双侧结肠沟侧腹膜多发结节状增厚,腹盆腔大量积液,考虑卵巢癌腹水,大网膜腹膜多发转移。
初始诊断:盆腔肿物,卵巢癌可能性大,腹水。
在手术治疗前,患者分别于2010年9月15日、10月12日行2周期新辅助化疗,方案为紫杉醇 300 mg+卡铂 600 mg。化疗后复查CA-125 34 U/ml;影像学检查结果为:子宫后方囊实性肿物较前明显缩小。
患者于2010年11月3日行经腹肿瘤细胞减灭术,手术达R0标准。术后病理示双侧卵巢组织符合低分化浆液性腺癌,膀胱腹膜、直肠前壁结节中见癌组织浸润。最终诊断:卵巢恶性肿瘤 低分化浆液性腺癌Ⅱc期。
2010年11月12日患者接受了第1周期的含铂化疗治疗(紫杉醇+卡铂)。术后20天,患者双下肢肿胀逐渐加重,伴发热,外院行超声考虑双下肢静脉血栓,CT不除外肿瘤复发(图1)。随后收入血管外科予溶栓抗凝治疗2天后,双下肢肿胀明显加重。
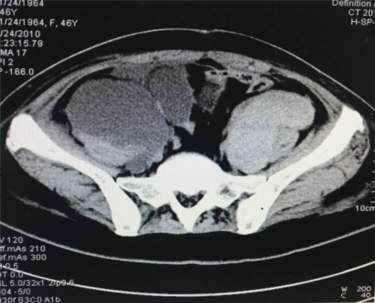
图1 术后20天外院CT检查结果
2010年11月26日患者急诊返院,查体双下肢明显红肿,无发热。辅助检查:Hb 87 g/L,AST 41 U/L。急诊超声提示双侧髂血管淋巴囊肿。遂紧急行双侧淋巴囊肿穿刺,放置引流管后,双下肢肿胀明显缓解。对症治疗约10天后双下肢肿胀基本消失。复查Hb 115 g/L,PLT 135 g/L,CA-125 16 U/ml。
2010年12月6日、2011年1月10日分别行术后第2、3周期含铂化疗,紫衫醇化疗后,患者淋巴囊肿反复增大伴发热,且出现骨髓抑制、肝功异常等,请佑安医院专家会诊后建议暂停化疗。对症治疗后,2011年7月复查CT提示淋巴囊肿已消退。
✔第二阶段:第一次复发+复发后治疗(含铂化疗)
*TC化疗后无进展间隔期PFI:13个月
患者2012年2月20日查盆腹增强CT提示新出现左隔下结节;4月23日复查CT结果为:左侧膈下软组织结节,较前增大,考虑腹膜转移;腹膜后小淋巴结,考虑肿瘤复发;阴道残端左上方结节,较前略饱满(图2)。CA-125 117.3 U/ml。
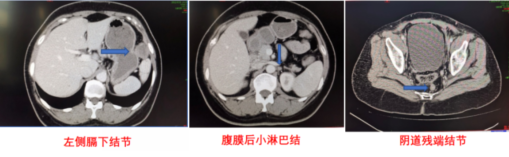
图2 2012年4月23日盆腹增强CT结果
患者自2012年4月24日起接受了6周期的含铂化疗(脂质体紫杉醇+卡铂),化疗后出现骨髓抑制,对症处理后好转。CA-125降至6.74 U/ml;盆腹增强CT结果为:原阴道左上方类结节消失,腹膜后多个小淋巴结较前缩小,左侧膈下转移灶明显缩小。疗效评估:部分缓解(PR)。
✔第三阶段:第二次复发+复发后治疗(手术+六甲密胺化疗)
*TC化疗后无进展间隔期PFI:4个月
2012年12月3日,患者复查盆腹增强CT提示:左膈下结节增大。未处理。2013年2月26日,复查CA-125 11.83 U/ml,盆腹CT:左侧膈下软组织结节,较前增大,考虑腹膜转移。
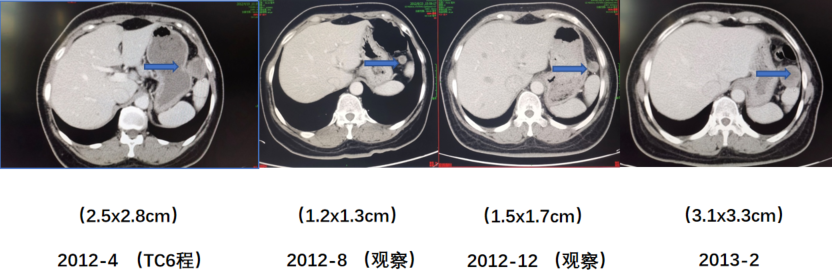
图3 第一次复发化疗后至第二次复发CT变化
2013年3月27日行第二次肿瘤减灭术,手术达R0标准。术后病理:纤维脂肪组织中见低分化癌,形态符合浆液性癌。术后予口服六甲蜜胺化疗,因胃肠反应明显,不足2周期停药。
✔第四阶段:第三次复发+复发后治疗(手术+含铂化疗)
*六甲密胺化疗后无进展间隔期PFI:44个月
2017年1月3日影像学检查提示复发。2017年2月查CA-125 78.71 U/m,盆腹增强CT结果提示:左侧盆壁结节较前增大,腹膜后多发肿大淋巴结,转移可能性大。妇科检查:盆底左侧可扪及4~5 cm肿物,活动受限。
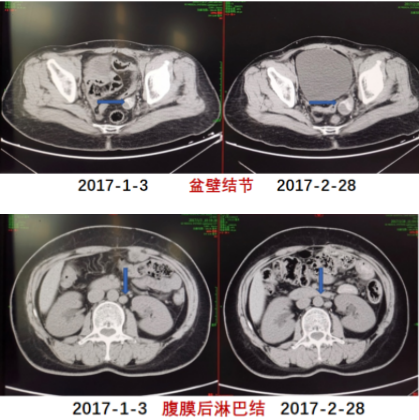
图4 第三次复发时两次影像学检查变化
2017年3月17日行第三次肿瘤减灭术,手术达到R0标准。术后病理:盆底肿物为高级别浆液性癌、腹主动脉左淋巴结转移性癌(4/8)。术后自3月28日起,患者行5周期含铂化疗(脂质体紫杉醇+卡铂),并再度出现骨髓抑制,对症处理后好转。CA-125降至4.25 U/ml。后患者要求停止化疗。
*停化疗后2周
2017年7月5日患者发热后出现腰痛,当地医院检查后考虑“骨转移”,遂于7月12日返院治疗。查CA-125 8.09 U/ml;影像学检查:胸部CT:新出现左肺下叶胸膜下结节,转移与肺梗塞待鉴别,双胸腔少许积液。骨扫描:胸10、腰4摄取增高,考虑良性。对症治疗后症状逐渐好转。其后1周再次出现骨痛加重,查CA-125 13.2 U/ml;PET-CT、MRI结果均提示骨转移。2017年8月25日予脂质体紫杉醇+奈达铂化疗,患者疼痛不缓解。多学科(MDT)会诊考虑“卵巢癌多次复发伴骨转移”,建议行姑息性放疗。放疗前骨穿病理结果未见肿瘤细胞,考虑化脓性骨髓炎。遂予以抗炎、抗结核、神经阻滞术等多种方法对症治疗,约2月后,患者症状逐渐好转并消失。其后未再出现和报告“骨转移”。
✔第五阶段:第四次复发+复发后治疗(含铂化疗+手术)
*TN化疗后无进展间隔期PFI:16个月
2018年12月复查CA-125 84.49 U/ml;影像学检查结果提示胰腺转移可能性大(图5)。
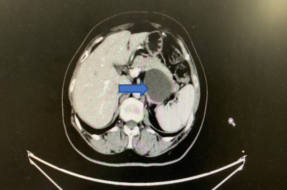
图5 第四次复发影像学检查结果
2019年1月患者CA-125升至147 U/ml。MDT第一次会诊后,自2019年1月8日至3月1日期间,予4周期含铂化疗(脂质体紫杉醇+奈达铂),化疗结束后CA-125降至6.4 U/ml。影像学复查结果为:胰腺后方肿物同前相仿,囊壁强化实性成分较前减少,内见液液平,不除外伴有出血(图6)。
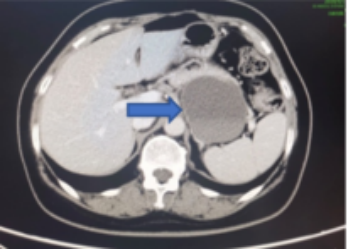
图6 含铂化疗后影像学检查结果
化疗结束后行第二次MDT会诊,并于2019年4月23日行第四次肿瘤减灭术,手术达R0标准。术后病理:分化差的癌伴陈旧出血及囊性变,符合卵巢浆液性癌复发。肿瘤侵及胰腺,并与肾上腺组织粘连。
✔第六阶段:第五次复发+PARP抑制剂维持治疗
*第四次减瘤术后无进展间隔期PFI:5个月
2019年9月复查盆腹增强CT:左肾前方结节较前增大,倾向为转移(图7)。CA-125指标正常。
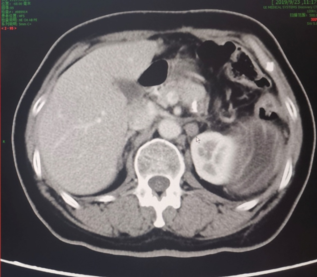
图7 第五次复发CT检查结果
患者基因检测结果为BRCA2致病突变。于2019年10月开始口服尼拉帕利200 mg QD。治疗期间无明显不良反应,未发生骨髓抑制情况等,未发生剂量减停。服用至今已逾18个月,CA-125保持稳定,复查影像学均未出现明显改变。
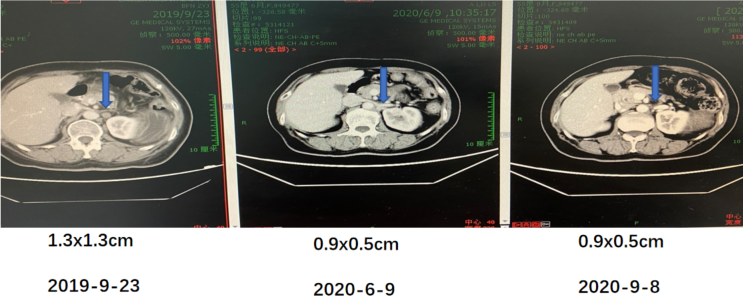
图8 尼拉帕利维持治疗期间影像学检查结果
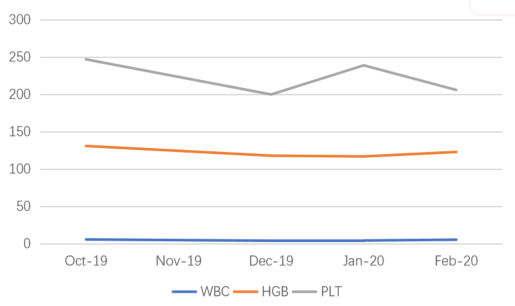
图9 尼拉帕利维持治疗期间血常规情况
病例总结
本例患者初发为中晚期卵巢癌,入院后经妇科检查、影像学检查及肿瘤标记物检测综合评估后,先行新辅助化疗2周期,疗后CA-125指标明显下降,肿物明显缩小;随即行第一次R0切除肿瘤细胞减灭术,术后含铂化疗第1周期后因淋巴囊肿,患者暂停化疗并对症处理,在其后进行的第2、3周期化疗时,均因紫杉醇用药后淋巴囊肿反复出现、肝功能异常等症状未用卡铂治疗。
初次治疗后患者多次复发并多发转移,在后续多次手术及多线化疗治疗期间,由于各种原因患者化疗未能保证足量足疗程,且频繁出现化疗副反应。直至第五次复发时,患者CA-125指标正常,影像学检查仅为小的孤立病灶,经综合评估患者开始口服尼拉帕利维持治疗。治疗期间患者无明显不良反应,未发生骨髓抑制情况等,未发生剂量减停。获得了较为满意的临床获益。
专家点评
卵巢癌的治疗一直困扰着临床医生和患者,随着PARP酶抑制剂的研究取得诸多成果,卵巢癌的治疗模式已转变为手术+化疗+维持治疗,以此延长患者的无铂治疗间期,让更多患者受益。本例患者初发为中晚期卵巢癌,虽经标准化的治疗模式,亦难逃复发的厄运。
根据2020年ASCO年会口头报告公布的AGO DESKTOP Ⅲ研究结果表明:首次复发和无铂间期>6个月,且经AGO评分为阳性的患者,相比单纯含铂化疗组,二次减瘤术联合含铂化疗组患者的OS、PFS和TFST均获益,同时死亡率和并发症发生风险无明显增加。研究还发现患者获益的关键在于“手术达到R0切除”。本例患者前四次复发时手术均达到了R0切除,这对患者的长期生存起到了关键作用。在患者11年半的生存期中进行的化疗疗程相对较少,其中有两次术后化疗均出现了严重的并发症,这影响了患者的生存质量和治疗周期。这就提示我们在治疗疾病过程中,应密切关注并发症的发生,及时开展多学科讨论,明确有效的治疗方案;在规范化治疗的同时,也需考虑个体化诊疗;并且不应仅局限于关注患者的PFS与OS,其生存质量也同等重要。
在第五次复发时,因前一次手术后患者恢复较慢,加之前几次化疗出现了并发症,患者抗拒继续接受化疗治疗。经基因检测,患者为BRCA2致病突变,故予尼拉帕利维持治疗。基于AVANOVA2研究结果:无论患者HRD状态或无化疗间隔时间,与单独尼拉帕利治疗组相比,尼拉帕利联合贝伐珠单抗治疗组的PFS显著改善(11.9个月 [95% CI 8.5-16.7] vs 5.5个月 [3.8-6.3],HR 0.35 [95% CI 0.21-0.57, p<0.0001])。根据尼拉帕利维持治疗铂敏感复发卵巢癌的全国多中心Ⅲ期随机对照试验——NORA研究结果显示,意向治疗(ITT)人群中位PFS达到18.3个月,较安慰剂组显著延长了超1年,且无论gBRCA突变及非突变亚组还是其他预设亚组,尼拉帕利组均一致显著生存获益。
对于本例患者,尼拉帕利维持治疗以来,无明显不良反应,未发生骨髓抑制情况等,CA-125波动稳定,影像学检查结果也均未出现复发表现,服药至今已逾19个月,显著延长了患者复发周期,生活质量也得到了提升。这也引发了我们进一步思考,PARP酶抑制剂能否替代化疗?若本例患者先行化疗,后再加用尼拉帕利维持治疗,是否可获得更佳临床疗效?如今尼拉帕利用于治疗铂敏感复发性卵巢癌已进入医保,相信未来可惠及更多患者。
阅读量:2418 | 点赞量:0
-

分享
-

收藏

 2418
2418