BRCAwt/HRD-卵巢癌患者一线维持治疗实现长期获益
时间:2022/12/7 14:30:01 作者:丁楠 范江涛
初始治疗 BRCA野生型 HRD阴性 高复发风险 满意肿瘤细胞减灭术 新辅助化疗*仅供医学专业人士阅读参考


 00:000:00
病例分享
00:000:00
病例分享

 00:000:00
专家点评
00:000:00
专家点评
卵巢癌作为女性生殖系统三大恶性肿瘤之一,病死率据妇科恶性肿瘤首位。因其起病隐匿,发现时往往即为晚期,且常伴随远处转移。虽然大多数患者经过初始治疗可获得临床缓解,但仍有70%在3年内复发,5年生存率不足50%[1]。因此,如何巩固初始治疗成果,并尽可能延缓复发成为临床医生积极探索的领域。多腺苷二磷酸核糖聚合酶(PARP)抑制剂作为一线维持治疗正是这一领域的重要探索成果。本期分享的病例为一例BRCA野生型/HRD阴性卵巢癌患者,患者在接受围术期化疗并实现R0切除后,及早启动了尼拉帕利一线维持治疗,病情稳定已达20个月,并计划治疗至36个月。现将病例内容详述如下。
病例回顾
基本资料
患者女,50岁,2020-10-23因“检查发现盆腔包块1年余”入院。LMP:2020-9-29。G2P2,顺产2孩。2017年行腹双侧输卵管结扎术,2019年因甲状腺癌行双侧甲状腺切除术,患有皮肌炎并接受治疗。否认恶性肿瘤家族史及遗传病史。
妇检:外阴发育正常,阴道通畅,黏膜无潮红,内有少许淡黄色液体,无异味。宫颈肥大,Ⅰ度糜烂样变,子宫触诊欠清,盆腔内触及不规则包块,大小约12×10 cm,固定。
超声:盆腔内混合回声包块(卵巢肿瘤?),大小120×94×96 mm,边界欠清,形态不规则,内回声不均,可探及丰富血流信号。
肿瘤标志物:CA125:403.8 U/ml;CA153:178.6 U/ml;HE4:187.6 PM。
CT:子宫后方及两侧旁见囊实性肿物影,增强后扫描实性部分明显强化,肿物与子宫后壁、直肠前壁分界不清;盆壁未见确切肿大淋巴结,腹膜后见数枚小结节状软组织密度影,增强后扫描中等程度强化,其中较大者约1.0 m×0.6cm。

图1 CT(腹部+盆腔)
2020-10-27穿刺活检:拟诊盆腔恶性肿瘤,形态倾向卵巢高级别浆液性癌。结合免疫组化结果,符合高级别浆液性癌。
免疫组化:PAX-8(+),CA-125(+),P53(+),WT1(+),CK7(+),CK20(-),ER(强+,90%),PR(强+,90%),Ki-67(约50%-60%)。
初步诊断:卵巢高级别浆液性癌
治疗经过
✔第一阶段:新辅助化疗+手术治疗+辅助化疗
新辅助化疗:给予患者TC方案3程,前两次剂量为紫杉醇脂质体250 mg+卡铂600 mg(2020-10-30、2020-11-22),第三次紫杉醇脂质体260 mg+卡铂600 mg(2020-12-13)。化疗结束后CA125:42.3 U/ml,HE4阴性。
2020-12新辅助化疗后B超评估:双附件区混合性回声包块较前缩小左(87 mm×55 mm×51 mm、右27 mm×18 mm×18 mm)。

图2 化疗后评估-B超
2021-1-05新辅助化疗后CT评估:盆腔内两侧附件区病灶体积较前缩小。两侧附件区可见囊实性肿物影,边界清楚,范围约6.4 cm×2.9 cm(左),2.8 cm×2.2 cm(右);腹膜后多发小淋巴结,较大者约0.6 cm×0.6 cm。
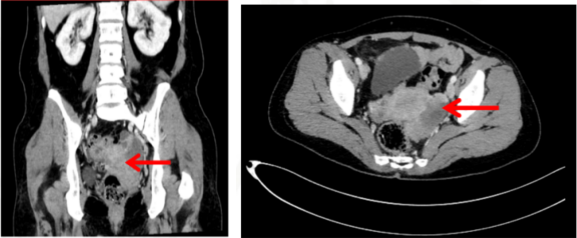
图3 化疗后评估-CT
2021-1-8行中间型肿瘤细胞减灭术,术中见左侧附件与盆底、部分直肠表面致密黏连,左侧卵巢不规则增大,大小约5 cm×4 cm×4 cm,实质性,表面可见菜花样肿物。手术达到R0切除。术后病理示,左附件包块考虑为卵巢高级别浆液性癌,直肠肿物考虑为转移性或浸润性卵巢高级别浆液性癌。免疫组化结果支持以上诊断。
术后辅助化疗:给予患者TC方案3程,剂量分别为紫杉醇脂质体250 mg+卡铂600 mg(2021-01-12)、紫杉醇脂质体250 mg+卡铂700 mg(2021-02-03)、紫杉醇脂质体240 mg+卡铂500 mg(2021-02-24)。化疗结束后CA125降至7.1 U/ml。基因检测结果提示,患者为BRCA野生型/HRD阴性。
✔第二阶段:PARP抑制剂一线维持治疗
2021-3-26起给予患者尼拉帕利200 mg qd维持治疗至今。密切随访患者维持治疗期间的不良反应。用药后的前三个月,叮嘱患者每周监测血常规,关注血常规变化,均稳定。肿瘤标志物CA125、HE4及其他标志物稳定,维持治疗期间患者影像学无明显变化。
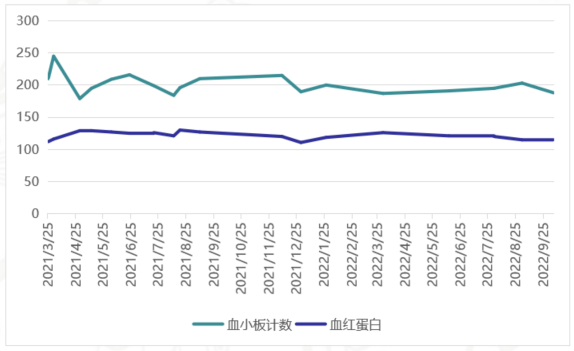
图4 维持治疗期间血小板、血红蛋白变化图
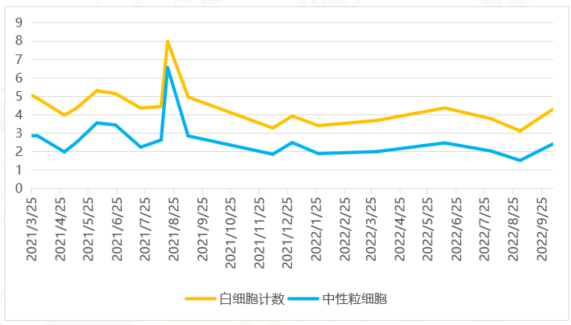
图5 维持治疗期间白细胞、中性粒细胞变化图
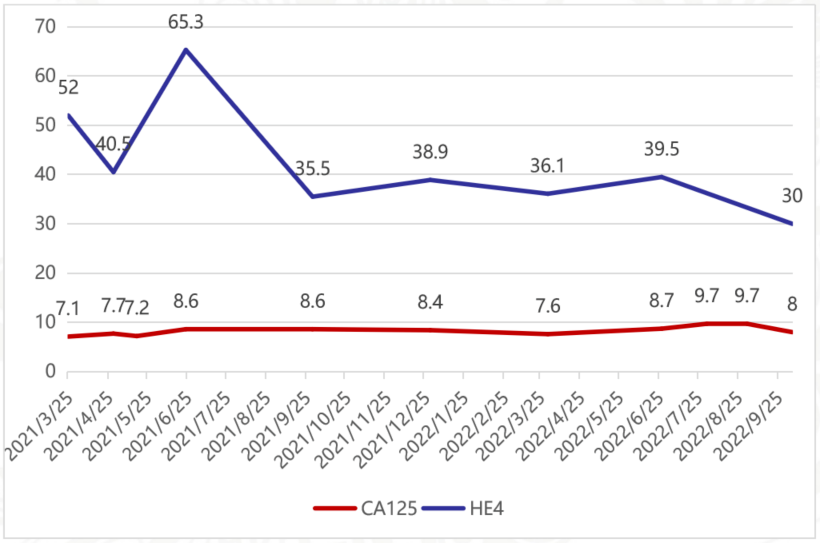
图6 维持治疗期间CA125、HE4变化图
2022-10-1随访:妇科超声显示卵巢癌术后,盆腔及髂窝内未探及明显囊、实性肿块声像。CDFI:髂血管频谱未见明显异常。腹部泌尿系超声:肝内多发稍高回声团(肝血管瘤?),双肾实质内稍强回声团(肾错构瘤?),胆、胰、脾回声未见异常,双侧输尿管未见扩张,门静脉主干及其分支回声未见异常。腹主动脉旁未见肿块。甲状腺癌术后:甲状腺区域未探及明显肿块声像,双侧颈部各区未见明显异常淋巴结。
下一步治疗计划:若无特殊,拟继续尼拉帕利维持治疗至36个月。
病例总结
患者为50岁绝经前女性,因“检查发现盆腔包块1年余”入院,经各项检查后诊断为卵巢高级别浆液性癌。首先给予患者3周期TC方案新辅助化疗,CA125、HE4水平明显改善,B超及CT影像学评估也提示患者病灶较前缩小。遂对患者行中间型肿瘤细胞减灭术,达到R0切除。术后病理符合(右附件包块)卵巢高级别浆液性癌诊断,并考虑直肠转移。给予3周期TC辅助化疗,CA125进一步降低。基因检测结果提示BRCA野生型/HRD阴性。以尼拉帕利作为术后一线维持治疗方案,治疗过程中无明显不良反应发生,肿瘤标志物和病情稳定。自应用尼拉帕利以来,患者已坚持用药近20个月,计划治疗至36个月。
专家点评
卵巢癌的规范化、个体化治疗对提高卵巢癌5年生存率非常重要。本病例患者为一位50岁绝经前女性,初步诊断为卵巢高级别浆液性癌,肿瘤体积较大。2022年美国国立综合癌症网络(NCCN)临床实践指南指出[2],对于手术条件不佳或较难实施满意的肿瘤细胞减灭术的卵巢癌患者,建议先给予新辅助治疗。根据推荐,患者于2020年10月30日开始接受三周期紫杉醇+卡铂的新辅助治疗,治疗达PR。患者顺利接受中间型肿瘤细胞减灭术,实现R0切除。术后病理确诊卵巢高级别浆液性癌并存在直肠转移。继续给予3周期紫杉醇+卡铂辅助化疗,患者CA125水平进一步降低。
《上皮性卵巢癌PARP抑制剂相关生物标志物检测的中国专家共识》指出[3],约18%的上皮性卵巢癌与种系突变有关,大多数来源于BRCA1和BRCA2,也包括同源重组途径中的其他基因和错配修复基因。2022 NCCN指南建议对所有初诊为上皮性卵巢癌患者进行基因筛查(BRCA,HRD)。经检测,该患者为BRCA野生型/HRD阴性。2019年美国临床肿瘤学会(ASCO)报道的真实世界研究显示,BRCA野生型卵巢癌患者末次含铂化疗后不进行维持治疗发展为铂耐药的风险增加。一旦铂耐药后患者疾病快速进展,愈后不佳。可见晚期卵巢癌容易复发,在规范手术+化疗基础上,一线维持治疗是标准治疗方案。
PRIMA研究主要评估了尼拉帕利对比安慰剂用于晚期卵巢癌患者的一线维持治疗的疗效[4],研究结果显示,无论BRCA/HRD状态,尼拉帕利一线维持治疗均为患者带来明确临床获益,对于HRD阴性患者,尼拉帕利也能使疾病进展或死亡风险下降32%。PRIME研究则是根据中国人群特点开展的研究[5],研究对患者进行个体化给药,对于基线体重<77 kg或血小板计数<150K/µL的患者起始给药剂量考虑为200 mg。结果显示,不计生物标志物状态,尼拉帕利经个体化给药均能使患者临床获益,且耐受性良好。尼拉帕利因此成为目前唯一获FDA/NMPA批准用于BRCA野生型/HRD阴性患者单药维持治疗的PARP抑制剂。
患者自2021年3月26日起使用尼拉帕利200 mg qd维持治疗,至今已20个月。期间无明显不良反应发生,血小板、中性粒细胞、血红蛋白等血液指标和CA125、HE4等肿瘤标志物均稳定,影响学评估也无明显变化。这提示,该例患者正从尼拉帕利长期维持治疗中持续获益,未来计划治疗至36个月,以进一步巩固目前取得的治疗成果。
参考文献
[1]中华医学会妇科肿瘤学分会. 现代妇产科进展,2020,29(5): 321-328.
[2]《2022NCCN卵巢癌包括输卵管癌及原发性腹膜癌临床实践指南(第1版)》.
[3]中国抗癌协会妇科肿瘤专业委员会.《上皮性卵巢癌PARP抑制剂相关生物标志物检测的中国专家共识》. 中国癌症杂志,2020年第30卷第10期, 841-848.
[4]González-Martín A, Pothuri B, et al. Niraparib in Patients with Newly Diagnosed Advanced Ovarian Cancer. N Engl J Med. 2019 Dec 19;381(25): 2391-2402.
[5]Li N, Zhu J, Yin R, et al. Efficacy and safety of niraparib as maintenance treatment in patients with newly diagnosed advanced ovarian cancer using an individualized starting dose(PRIME Study): a randomized, double-blind, placebo-controlled, phase 3 trial. Presented at: 2022 SGO Annual Meeting on Women’s Cancer; March 18-21, 2022. Phoenix, Arizona.
阅读量:2683 | 点赞量:0
-

分享
-

收藏

 2683
2683