附件包块(包含卵巢、输卵管或周围组织肿块)多由妇产科医生发现,通常很难明确诊断。大多数肿块是在体检或做盆腔成像时意外发现。少数肿块可能出现急性或间歇性疼痛症状。处理决策往往受患者年龄和家族史影响。虽然大多数肿块为良性,诊断评估的主要目的是排除恶性肿瘤。本文旨在提供青少年、孕妇及非妊娠妇女附件肿块的评估和处理指南,并概述可能为恶性、需要转诊或需要妇科肿瘤专家会诊的附件包块的鉴别标准。
背景
鉴别诊断
盆腔肿块包括妇科或非妇科来源的(框1)。结合考虑盆腔肿块位置与患者年龄和生育情况有助于缩小鉴别诊断范围。妇科来源的附件肿块可能为良性,也可能为恶性卵巢疾病;输卵管或卵巢病变如输卵管积水或异位妊娠;子宫异常如子宫肌瘤或苗勒管病变。非妇科来源的盆腔肿块少见,可能与其他器官系统有关,包括胃肠道和泌尿系统来源。转移性癌症病例,尤其是来源于乳腺癌,结肠癌,或胃癌,首发表现可能为附件肿块。
恶性肿瘤的风险因素
女性群体中卵巢癌最重要的独立性风险因素是年龄,且在绝经开始,卵巢癌发病率陡然增加。根据2009-2013年SEER报告数据,卵巢癌诊断的中位年龄为63年,69.4%患者55岁或55岁以上。绝经后妇女附件肿块虽然多为良性肿瘤如囊腺瘤,但恶性肿瘤的发病风险远远高于绝经前妇女。
卵巢癌最重要的个人危险因素是有乳腺癌或卵巢癌的家族史。区分卵巢癌家族史和卵巢癌综合征家族史很重要。对于有一位家庭成员卵巢癌的35岁女性,卵巢癌发病率从人群发生风险1.6%增加至5%。然而,BRCA1基因突变的妇女,其卵巢癌、输卵管癌或腹膜癌发生风险在70岁之前约41 - 46%。BRCA2基因突变的妇女,其卵巢癌、输卵管癌或腹膜癌发生风险在70岁之前约10 - 27%岁。 70岁以上且有Lynch综合征的妇女其卵巢癌发生风险约5 - 10%。增加卵巢癌发生风险的其他因素包括未经产、月经初潮早、绝经晚、白色人种、原发性不孕和子宫内膜异位症。
框1. 附件肿块的鉴别诊断
妇科
•良性
−功能性囊肿
−卵巢子宫内膜异位囊肿
−输卵管卵巢脓肿
−成熟畸胎瘤(皮样囊肿)
−浆液性囊腺瘤
−粘液性囊腺瘤
−输卵管积水
−卵巢冠囊肿
−肌瘤
−苗勒管异常
•恶性
−上皮癌
−生殖细胞肿瘤
−转移癌
−性索或间质肿瘤
非妇科
•良性
−憩室脓肿
−阑尾脓肿或囊肿
−神经鞘瘤
−输尿管憩室
−盆腔肾
−膀胱憩室
•恶性
−胃肠道癌症
−腹膜后肉瘤
−转移癌
总体评估
病人个体特征、体格检查结果、影像学结果和血清标志物水平有助于将盆腔肿块分成良性、性质未定或可能恶性,可指导医生恰当处理。
病史和家族史
个人病史与详细妇科病史和症状回顾是对患者评估的重要组成部分。此外,家族史和其他风险因素回顾有助于评估恶性的可能。
附件肿块伴随的一些症状能完善鉴别诊断。例如,育龄妇女出现急性腹部或盆部疼痛可能有出血性卵巢囊肿。所有育龄妇女都应评估妊娠相关性疾病如异位妊娠。单侧出现间歇性盆腔疼,继而急性加重,可能提示卵巢扭转。钝性、渐进性盆腔疼痛伴发热、畏寒、呕吐,并有阴道分泌物提示可能为感染性疾病如输卵管卵巢脓肿。有报告称妇女出现急性或慢性痛经或性交痛提示可能有子宫内膜异位症。持续腹胀、弥漫性腹痛、过早饱腹感可能是恶性肿瘤的征象。异常子宫出血或绝经后出血可能是由性索间质肿瘤产生的雌激素引起的。
体格检查
体格检查应从生命体征和一般身体表征评估开始。包括颈部、锁骨上、腋窝和腹股沟淋巴结触诊,肺部听诊,腹部触诊、听诊,盆腔检查(包括会阴、宫颈和阴道视诊;双合诊,按照规范检查直肠阴道)。虽然盆腔检查(即使病人在全身麻醉下)识别附件包块的作用有限,特别是患者身体质量指数大于30,检查发现与附件恶性肿瘤相关的附件肿块可以是形态不规则、质地坚硬、固定、结节状、双侧或与腹水有关。有以上表现的良性疾病包括子宫内膜异位症、慢性盆腔感染、出血性黄体、输卵管卵巢脓肿和子宫平滑肌瘤。
影像学
经阴超声是评估附件肿块最常用的成像技术。超声检查可评估肿块的大小和组成(囊性、实性或混合),侧别,是否有分隔、壁结节、乳头状赘生物或盆腔积液。彩色多普勒超声对评估盆腔病变的血管特征有用。当盆腔正常解剖结构因既往手术破坏,肿块超出盆腔范围或不能进行阴道超声检查时,腹部超声也是很有用的辅助检查。
计算机断层扫描(CT)、磁共振成像(MRI)和正电子发射断层扫描(PET)不建议在初始评估附件包块时使用。基于有限的数据,MRI在对恶性肿块正确分类方面优于经阴超声,整体检出率较低。然而,MRI可清楚鉴别盆腔肿块是否为卵巢来源,特别是平滑肌瘤。
目前,CT成像的最佳用途不是检测和辨别盆腔肿块,当基于超声图像、检查结果或血清标记物怀疑恶性肿瘤,CT可辅助评估是否有腹部转移,。CT扫描可发现腹水、大网膜转移、腹膜种植、盆腔或腹主动脉旁淋巴结肿大、肝转移、梗阻性肾病,还可能发现另一个原发癌部位,包括胰腺和结肠。
实验室检验
实验室检验可明确盆腔肿块的可疑病因。如疑似妊娠,育龄期妇女应做妊娠测试。如疑似感染,需全血计数并做淋病和衣原体感染检验。根据病史和检查结果有价值的其他实验室检验包括尿常规、粪便隐血试验或肠道相关的其它评估和血清标志物检测。
血清标志物检验
血清标志物结合影像学用于评估恶性肿瘤的可能性。研究最广泛的血清标志物是癌抗原125(CA 125),但非恶性组织中表达水平较低。CA 125水平升高可出现在子宫内膜异位症、妊娠、盆腔炎性疾病和非妇科来源的癌症。评估绝经后妇女的附件肿块和识别肿块为非黏液性上皮癌,CA 125检测最有用(表1)。80%上皮性卵巢癌患者会出现CA 125升高,但只有50%患者为 Ⅰ期疾病。最近,人类附睾蛋白4可作为区分良恶性肿块的潜在有用的生物标志物。如根据危险因素、症状或超声疑似为不常见的卵巢癌病理组织类型,测量β-HCG水平、L-乳酸脱氢酶、甲胎蛋白或抑制素可协助评估(表2)。
研究证实生物标志物系列结合临床和影像学评估区分附件肿块良恶性的作用。美国食品和药品管理局批准了两种不同的血清肿瘤标志物系列试验进一步评估女性盆腔肿块为卵巢癌风险:1)多因素指数分析法,定性血清肿瘤标记物系列;2)卵巢恶性肿瘤的风险算法。这些方法已被批准用于18岁以上且有确定附件包块需要手术的妇女。多因素指数分析法包含五个与卵巢癌相关的血清生物标志物(CA 125 II、转铁蛋白、转甲状腺素蛋白[前白蛋白 ],载脂蛋白A-1和 β2-微球蛋白),并用专有算法将恶性肿瘤的风险评分定为0–10。卵巢恶性肿瘤风险算法包括CA125,人类附睾蛋白4和绝经状态。绝经状态的变量截止值用于多因素指数分析法和卵巢恶性肿瘤风险算法(表1)。
多模式检测
已开发的诊断算法包括血清标志物、临床评估和超声结果。对于卵巢癌的诊断和初步处理,英国国家卫生和临床优化研究院指南建议将计算恶性肿瘤风险指数版本Ⅰ作为评估的一部分。恶性肿瘤风险指数计算使用了血清CA125水平(U / ml)、超声扫描结果(根据结果评分为0、1或3分)和绝经状态(1分表示绝经前,3分表示绝经后)。一项系统回顾发现恶性肿瘤危险指数评分为200分时,其合并后的预测敏感性为78%(95%置信区间[ CI ],71 -85%)和特异性 为87%(95% CI,83 - 91%)(表)。
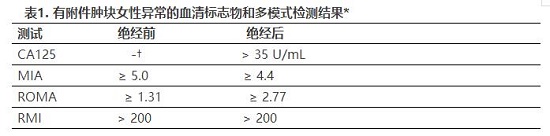
缩略词:CA,癌抗原; MIA,多因素指数分析法; ROMA,卵巢恶性肿瘤的风险算法;RMI, 恶性肿瘤风险。
*血清生物标志物和多模式检测利于确定是否将附件包块患者转诊或请妇科肿瘤专家会诊。目前证据不足以推荐任何明确测试。
†绝经后妇女CA 125水平的特异性和阳性预测值均高于绝经前妇女。之前美国妇产科学院指南把CA125 大于200 U/ml作为将有附件包块的绝经前女性转诊给妇科肿瘤专家的阈值。该值基于专家意见得出;无证据基础的阈值目前可用。因此,妇科医生应联合CA 125与其他临床因素作为是否请会诊的判断指标。
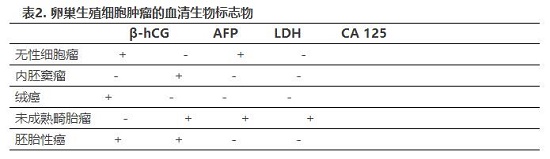
缩略词: AFP, 甲胎蛋白; CA, 癌性抗原; LDH,乳酸脱氢酶。
 妇产科在线APP下载
妇产科在线APP下载










 京公网安备 11010202008857号
京公网安备 11010202008857号