一、基因异常、细胞凋亡与子宫内膜异位症
1. 基因变化与子宫内膜异位症
EMs虽为一种良性病变,但其颇具侵蚀性,并有细胞增殖和新血管生成等特点,有学者认为该病的发生发展与肿瘤类似,基因突变和过度表达也是该病发生的重要因素。近年来随着实验技术的改进与提高,许多证据证实EMs存在多种基因的缺失与过度表达。基因片段的缺失或突变可导致基因激活、转录异常、表达产物改变,使基因正常的生物学功能丧失,导致各种疾病的发生,同样,EMs也遵循了这一规律。
有学者认为,EMs的产生与环境等众多辅助因素的激发作用有关,是由多个位点基因和环境因素相互作用所导致的一种遗传性疾病。有研究表明,卵巢癌候选基因与子宫内膜异位症候选基因有可能具有相同的染色体位点。因此,基因的变化在EMs发生发展中起重要作用。
与正常女性相比,EMs患者的在位子宫内膜在基因表达上存在某些差异,这些基因表达异常包括:与侵袭性有关的基质金属蛋白酶(MMP)和尿激酶型纤溶酶原激活物(uPA)过量表达,MMP组织抑制物(TIMP)和血浆素原活化因子抑制物(PAI)表达不足,与血管发生有关的血管内皮生长因子A(VEGF-A)过量表达,可能与抗凋亡有关的c-kit、DAD-1的异常或过量表达,与局部雌激素过量有关的芳香化酶异常表达和17β羟类固醇脱氢酶(17βHSD)表达不足,与孕酮反应性有关的孕酮受体α/β比例异常,以及与炎症反应有关的环氧合酶2(COX-2)过量表达。
2.细胞凋亡与子宫内膜异位症
细胞凋亡(Apoptosis)又称程序性细胞死亡(programmed cell death,PCD),由Kerr教授于1972年首先提出,是指有核细胞在一定条件下通过启动内部机制,经过一系列的细胞变性,最终发生死亡的过程。正常子宫内膜同样存在凋亡的调节,参与凋亡的调节基因有:bcl-2、bcl-x、bax、fas,TNFR、PD-1、c-fos、c-myc和p53,其中bcl-2和fas起主要作用,p53可能与Bax起协同作用。
近年来细胞凋亡与内异症的关系受到许多学者的关注,研究认为EMs的发生与细胞凋亡能力的下降有关。细胞凋亡是真核生物有核细胞死亡的一种方式,受高度调节的生理性过程,细胞以凋亡方式自杀,对机体的自身稳定起了积极作用,若此环节发生异常,则会出现细胞堆积而引起疾病甚至肿瘤的发生。内异症患者的子宫内膜细胞凋亡率下降,脱落的细胞能逃逸机体的清除,继续生长到异位病灶中,从而促进内异症的发生。异位内膜凋亡率低于在位内膜,在位内膜凋亡率低于正常子宫内膜,说明EMs患者在位及异位内膜对凋亡的敏感性均明显下降,异位内膜较在位内膜下降更明显,且无周期性变化。因而可以推测,内膜组织自发性的凋亡减弱和对凋亡的敏感性下降可能是引发EMs的一个原因。
目前对子宫内膜凋亡调节基因的研究主要集中于bcl-2、bax。bcl-2是目前发现的与凋亡关系密切的原癌基因之一,其功能在于延长细胞寿命并增加细胞对多种凋亡刺激因子的抵抗性,故称之为“凋亡抑制基因”。bax作为bcl-2对抗基因,可以加速细胞死亡,称之为“凋亡促进基因”。bcl-2与bax的比例决定了细胞在受到凋亡信号刺激时是否发生调亡,bax蛋白与bcl-2蛋白具有20%的同源性,能与bcl-2结合形成异源二聚体,从而对抗bcl-2抑制细胞凋亡的作用。内异症患者异位内膜的细胞凋亡率低于正常妇女的子宫内膜,并且bcl-2蛋白的表达明显升高,而bax蛋白的表达又明显降低,提示这些凋亡率降低的子宫内膜异位至腹腔后,对细胞毒作用的反应敏感性降低,同时组织的抗凋亡性增强,得以逃避免疫监视而在子宫腔以外存活、种植、侵袭和发展,形成异位病灶。
bcl-2是细胞凋亡线粒体通路的主要调节因子,当细胞中的bcl-2蛋白表达升高时,细胞的凋亡过程即受到抑制,细胞生存时间延长,其在子宫内膜中的表达规律与TNF-α相反。月经期TNF-α的诱导作用及bcl-2保护作用的丧失共同导致了子宫内膜细胞凋亡的周期性脱落。正常妇女子宫内膜细胞在增殖早期和分泌晚期达高峰,子宫内膜异位症患者的在位内膜上皮和间质的细胞凋亡率较正常妇女低3~4倍,异位内膜细胞凋亡率较相应的在位内膜更低,异位内膜对雌激素的敏感性强于孕激素,故处于持续增生状态,TNF-α表达较弱,而bcl-2表达较强,bcl-2保护细胞的作用强于TNF-α诱导细胞凋亡的作用,因而异位内膜细胞不易凋亡。
bax于1993年首次发现,它是调控凋亡的bcl-2家族的前凋亡成员,参与线粒体通路。有研究表明bcl-2和bax两蛋白之间的比例是决定对细胞凋亡抑制作用强弱的关键因素。p53可能与bax有协同作用,共同促进凋亡,在内异症中,二者均降低,导致子宫内膜细胞抗凋亡能力增加,进一步促进EMs发生发展。另外,bax和fas在异位症患者在位内膜和异位内膜中表达较低,使异位内膜细胞抑制凋亡能力增强。由于子宫内膜异位症患者月经期剥脱的子宫内膜中的细胞凋亡率低,具有生物活性的内膜细胞随经血逆流至腹腔,增加种植机会。这些凋亡率低的子宫内膜异位至腹腔后,更不易凋亡,且对细胞毒作用的反应敏感性降低,从而促发子宫内膜异位。
XIAP是凋亡抑制蛋白(inhibitor of apoptosis proteins,IAPs)家族中的一员,是IAPs家族最具有潜在抑制活性的蛋白质。Smac是新近发现位于线粒体内外膜间隙的促凋亡蛋白,作为XIAP上游的信号分子,可与XIAP相互作用。研究发现XIAP表达增高且缺乏周期性变化在EMs发病机制中可能扮演了重要角色,Smac随XIAP表达的增高而增高,呈正相关关系。Smac通过解除了XIAP对于caspase-3、caspase-9等的活性抑制作用,限制了XIAP增高可能引起过度凋亡抑制导致的癌变倾向,表明在EMs发病机制中,线粒体促凋亡因子Smac在EMs良性疾病特性方面发挥了重要作用。
凋亡基因的改变对内异症治疗具有重要的意义。临床实践中,可以引入凋亡抑制基因的拮抗基因,或通过药物和其它细胞因子诱导异位内膜细胞的凋亡,以期将内膜细胞从抵制凋亡状态解放出来,达到治疗内异症的目的。EMs患者的异位和在位内膜抗凋亡基因表达增强,促凋亡基因表达明显降低,致使EMs患者子宫内膜的凋亡率下降,抗凋亡能力增强,故通过促性腺激素释放激素类似物来诱导异位内膜细胞的凋亡,降低子宫内膜的抗凋亡能力,使脱落的子宫内膜细胞在异位的生存能力减弱,从而治疗内异症。
目前细胞凋亡在子宫内膜异位症中的研究尚处于初级阶段,子宫内膜异位症凋亡基础的研究,尤其是利用现代分子生物学技术研究凋亡基因、凋亡抑制基因将开辟子宫内膜异位症诊治的很有希望的领域。
二、细胞粘附与子宫内膜异位症
细胞与细胞、细胞与细胞外基质间的粘附作用是多细胞生物的基本生物学现象。粘附作用是通过一系列位于细胞膜表面的细胞粘附分子(cell adhesion molecules,CAMs),或称为细胞粘附受体所介导的。CAMs除参与多种生理及病理过程外,在胚胎的发育分化,正常组织的维持,损伤的修复,炎症和免疫反应以及肿瘤的转移等方面都起着重要的作用。研究发现,人类子宫内膜的腺上皮及基底膜均有多种CAMs的表达,有些呈周期性变化,并与子宫内膜“着床窗”(window of implantation)的开放同步。某些CAMs的异常表达可能参与了异位子宫内膜的定位、粘附及种植过程,并可通过干扰子宫内膜对受精卵的接受性导致不孕。
CAMs是指由细胞合成存在于细胞表面或细胞外基质中,介导细胞间或细胞与细胞外基质(extracellular matrix,ECM)间粘附作用的膜表面糖蛋白,由细胞外区、跨膜区和细胞内区三部分组成,少数通过肌醇聚糖磷脂“抛锚”于细胞膜。到目前为止已发现的CAMs有50种以上,分别属于免疫球蛋白超家族(immunoglubin superfamily,IGSF)、整合素家族(intergrinfamily)、选择素家族(selectin family),钙粘附素家族(cadherin family)以及一些未归类的细胞间粘附分子如CD44、CD45、CD22等,其表达受E2、P和多种生长因子、细胞因子的调节,以维持正常的生理、生殖功能。EMs患者存在某些细胞粘附分子的异常表达,如EMs腹水中可溶性细胞粘附分子(ICAM-1)表达过强;内膜间质细胞有ICAM-1的基础表达,当有IL-1β存在时,ICAM-1表达增强。bINF-γ和IL-6能刺激体外培养的腹腔巨噬细胞产生可溶性ICAM-1,从而降低NK细胞的活性。可溶性ICAM-1是异位内膜与免疫细胞之间联系的重要因子,可能是异位内膜细胞逃避细胞免疫监视的机理之一。因此,可以说细胞粘附分子对异位内膜细胞的定位、粘附和种植起重要作用。
近几年国内外在对EMs发病机制研究中发现,CAMs对于异位子宫内膜在子宫腔外生长的初期起着重要作用,尤其是ICAM-1,即CD54具有关键性作用。
1.免疫球蛋白超家族(IGSF):IGSF是钙依赖性的细胞黏附分子,包括细胞间黏附分子1(ICAM-1)、ICAM-2、血管细胞黏附分子(VCAM-1)肿瘤细胞介导的胶原酶激活因子(CD147)等,其中与EMs发病关系最密切的是ICAM-1,其共同特点是胞膜外部分的结构类似于免疫球蛋白的功能区,此家族的CAMs与整合素家族成员可互为配体-受体。
细胞间粘附分子-1(intercellular adhesion molecule,ICAM-1)即CD54分子,是T细胞免疫激活的一个重要标志物,属于细胞粘附分子中免疫球蛋白超家族中重要的一员,是含有505个氨基酸的跨膜糖蛋白,主要存在于上皮细胞和内皮细胞表面,血清可溶性细胞粘附分子-1(sICAM-1)是其可溶性的脱落片段。研究发现ICAM-1在异位内膜的表达较正常及在位内膜增高,升高的ICAM-1增加了呈递抗原的功能,在分泌期,在位子宫内膜ICAM-1表达减弱,表明EMs患者此期内膜与基底膜粘附性降低,易于异位。也有研究证实,内异症患者血清sICAM-1水平明显升高,且升高的水平随内异症病变程度而增加。内异症血清sICAM-1作为一个敏感指标,其水平明显增高,并随病情加重血清sICAM-1水平亦明显上升。
2.整合素家族:整合素家族是广泛分布的细胞表面粘附分子,是一组介导细胞与细胞、细胞与ECM间黏附的跨膜糖蛋白,大多在白细胞表面表达,其配体为细胞外基质成分,如纤维粘连蛋白、纤维蛋白原、胶原蛋白、体外粘连蛋白等。所有整合素家族均为由α、β亚单位通过非共价键链接起来的异二聚体。根据β亚单位的不同,可分为三个亚家族:①β1亚家族(VLA组),该亚家族至少包括6个不同的成员(α1β1、α2β1、α3β1、α4β1、α5β1、α6β1),它们可在各种类型的细胞表面表达;②β2亚家族(LFA组),它包括三个成员,即LFA-1、Mac-1和P150,90,三者均在白细胞上表达,故又称为白细胞整合素亚家族;③β3亚家族(血小板唐代白组),有两个成员(体外粘连蛋白受体VNR和血小板蛋白Ⅱb/Ⅲa),两者主要表达于内皮细胞和血小板上。整合素具有多种生物学功能,如参与免疫细胞间粘附作用、调节机体发生发育、参与伤口修复以及血栓形成等等。有学者认为整合素β参与了内膜组织的异位粘附过程,并通过诱导T淋巴细胞的凋亡,从而逃避免疫监视,除此之外,异位症在位内膜整合素αγβ3的表达较对照组显著增强,整合素αγβ3的改变有利于血管的发生及内膜种植。
3.选择素家族:选择素家族均为高糖基化的单链跨膜糖蛋白,已被鉴定的选择素有选择素-E(E-selectin)、选择素-P(P--selectin)和选择素-L(L-selectin)。选择素家族的CAMs在结构上均有外源凝血样区,EGF样区和C3、C4结合蛋白样区三部分组成。其外源凝血素样区是受体-配体结合的部位。选择素表达于白细胞、活化的内皮细胞以及血小板表面,它可在血流状态下介导白细胞与血管壁的初步附着。
4.钙粘附素家族:钙粘附素家族是一组钙依赖性跨膜糖蛋白,主要通过同型分子参与介导特定组织或器官同型细胞间黏附,参与维持组织结构的完整性。广泛分布于各种类型的细胞表面,可分为:①上皮型钙黏蛋白(E-cadherin):主要存在于人和动物上皮细胞,是维持上皮细胞形态和结构的完整性和极性的重要分子。②神经型钙黏附蛋白(N-cadherin),分布在神经和肌肉组织。③胎盘型钙黏附蛋白(P-cadherin),分布于胎盘和上皮组织以及发育阶段的其他组织。钙粘附素主要介导细胞与细胞之间的相互作用,为细胞间连接的主要成分,并以此构成组织的细胞骨架。其粘附作用具有同源性,即表达同源性钙粘附素的细胞将发生粘附。
上皮型钙黏蛋白(E-cadherin)是钙黏附分子中最具代表性的一类,其作为重要的肿瘤侵袭性抑制因子,在子宫内膜异位症发病中的作用日益受到重视。研究证实EMs患者在位及异位子宫内膜上皮细胞E-cadherin的表达均低于正常内膜,E-cadherin的表达下降还可以导致分泌移动生长因子受体升高,子宫内膜细胞移动性增强,使EMs患者子宫内膜上皮细胞易于移动而“异位”;而E-cadherin的表达降低,又可导致子宫内膜上皮细胞基质金属蛋白酶-2(matrix metalloproteinase,MMP-2)的分泌明显增加,使细胞易于从宫腔表面脱离的同时,也具有了蛋白水解酶的作用,以及浸润和种植的能力。所有的这些变化都有利于EM患者子宫内膜上皮的移动、浸润和种植。
5.其他粘附分子:CD44是一种高度异质性的多功能的单链跨膜透明质酸受体,存在于细胞表面,是一种重要的膜糖蛋白,配体是细胞外基质(ECM)蛋白,主要参与细胞与细胞、细胞与ECM间的特异性粘连。其在多种肿瘤的发生、发展,尤其是转移中起促进作用。研究认为EMs异位内膜上皮细胞CD44表达异常增高,导致子宫内膜腺上皮细胞易于在异位处侵蚀ECM并在异位处种植、生长,使异位子宫内膜腺上皮细胞表现为浸润现象。
尽管目前还缺乏详细、深入的研究探讨子宫内膜异位症中CAMs的作用,但子宫内膜异位症发生、发展过程中细胞间相互作用及多种细胞因子的存在,提示粘附分子对异位内膜的免疫粘附可能起不可忽视的作用。综合一些研究结果,CAMs至少在以下几方面参与内膜异位症的发病机制:①腹腔液中免疫细胞选择性渗出可能与CAMs在不同类型细胞表达的差异以及细胞因子对CAMs表达的不同调节作用有关。②CAMs介导细胞移动,这对异位内膜达到宫腔外部位的选择性定位具有促进作用。③CAMs参与异位内膜细胞与基质的粘附,这是细胞存活、繁殖所必需的,这主要由整合素家族粘附分子介导。④CAMs参与细胞间的粘附,主要由钙粘附素家族的CAMs以自身识别方式作用,保证异位内膜细胞的聚集。
综上所述,整合素、选择素、钙黏附蛋白、免疫蛋白类等黏附分子均在子宫内膜上表达,黏附分子参与异位内膜的黏附,侵袭及血管生成,其表达异常与EMs的发生发展密切相关。目前,直接针对黏附分子的治疗已应用于许多免疫与炎症性疾病,如已有应用整合素抗体抗血管生成治疗肿瘤的临床实验报道。
三、细胞外基质重塑与子宫内膜异位症
基质金属蛋白酶(matrix metalloproteinases,MMPs)是一个高度保守的锌离子依赖性的内切蛋白水解酶家族,是细胞外基质降解的主要蛋白水解酶,可降解细胞外基质的大多数蛋白,在细胞外基质重建中起重要作用,其活性可被TIMPs和α-巨球蛋白所抑制。基质金属蛋白酶组织抑制剂( tissue inhibitor of metalloproteinase, TIMP)是MMP的天然抑制物,近年来研究表明MMP和TIMP在内异症中的异常表达可能与内异症的发生发展有关,且MMP/TIMP的比例增加与经期逆流于腹腔的内膜侵袭生长于异位部位有明显相关性。在人的正常子宫内膜组织中,不同的MMPs在月经周期中的表达不同,子宫内膜间质可表达数种MMPs,这些酶可能参与子宫内膜重建、囊胚种植及滋养层浸润。但研究发现,在子宫内膜异位症患者的异位内膜中也表达多种MMPs蛋白,且部分MMPs在异位内膜中表达水平明显高于在位内膜组织,并不受月经周期的影响。迄今为止,MMPs在子宫内膜异位症患者异位内膜中过度表达的机制尚不十分明确。有关子宫内膜异位症患者在位子宫内膜和异位子宫内膜MMPs表达的差异主要集中在MMP-2和MMP-9基因上,有关其它在子宫内膜周期中表达的MMPs在在位和异位内膜中表达差异的研究文献报道还相对有限。
MMP-1是MMPs家族中的主要成员,在异位内膜组织中的过强表达,尤其在异位内膜间质中的过强表达,表明其在子宫内膜异位症的发生发展中发挥重要作用。MMP-1的水解活性受其天然特异性组织抑制因子TIMP-1的紧密调控,生理状态下MMP-1与TIMP-1之间存在着一种动态平衡,这种平衡是协调ECM降解与重建、维持内环境稳定和结构完整的重要因素。

图1-4 MMP-2在EM异位内膜(A)、在位内膜(B)、正常内膜(C)中的表达
MMP-2是MMPs含量最丰富、最具代表性和分布最广泛的一种明胶酶,在人的血清、脑脊液、滑膜液中均有MMP-2存在,MMP-2通过清除损伤的胶原,使一些明胶或受损的胶原不在组织中沉积下来。MMP-2在异位内膜组、在位内膜组、正常内膜组中均有表达,在异位内膜组表达尤为显著,使异位内膜组织具有侵袭腹膜及周围组织的能力,并且在盆腔、腹膜内不断种植生长,在子宫内膜异位症的发生发展中发挥重要的作用。MMP-2在异位内膜组织中的表达失去其在正常子宫内膜组织中的月经周期性变化,这可能是临床上应用激素治疗异位症失败的原因之一(见图1-4)。
MMP-3主要分布在EMs的腺上皮细胞和间质细胞,异位内膜中的MMP-3表达随EMs临床分期的升高而增强,提示其与EMs的侵袭呈正相关。
MMP-7属于基质溶解素的一种,降解蛋白聚糖、纤维连接蛋白、层粘连蛋白、弹性蛋白、胶原Ⅳ等,主要分布在腺上皮细胞的胞浆内,而在间质细胞内无表达。MMP-7在正常内膜组织中表达率最低,在EMs在位、异位内膜组织中表达率高,在位内膜 MMP-7的高表达是疾病发生的关键。
MMP-9与MMP-2同属明胶酶,称为明胶酶B,可降解基底膜的主要成分,与炎症细胞有较大的联系,并且是具有侵袭能力的关键物质。巨噬细胞和中性白细胞都是MMP-9的主要来源。MMP-9在子宫内膜异位症的发病进程中起到了决定性作用,它促进了异位组织细胞外基质的降解和血管的生成,而这恰恰是内异症疾病进展的关键所在。研究认为腹腔液MMP-9含量与血清不同,腹腔液中,MMP-9表达较血清明显增多(见图1-5)。
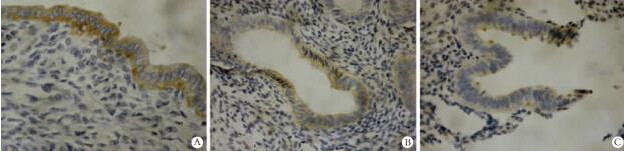
图1-5 MMP-9在EM异位内膜(A)、在位内膜(B)、正常内膜(C)中的表达
MMP-14是第一个发现的位于细胞膜上的MMP,又称之为Ⅰ型膜基质金属蛋白酶(MT1-MMP),不仅本身具有降解ECM的能力,而且能激活另一种MMP即明胶酶A(MMP-2)。MMP-14在内膜异位症的发生过程中,与其他MMPs家族成员(包括MMP-9)均起到了降解细胞外基质、辅助内膜细胞异位种植的作用。
研究表明子宫内膜异位症患者的异位内膜中MMP-1和MMP-3蛋白表达均明显高于在位内膜,表明MMP-1、MMP-3蛋白的异常表达可能与子宫内膜异位症的发生和发展有关(MMP-1为胶原酶,MMP-3为间质溶素,二者的高表达均可增加细胞外基质的降解能力,所以异位组织中MMP-1、3的高表达可能表明细胞降解细胞外基质的能力增强,与组织的重建、出血及种植有关),而子宫内膜异位症患者的在位内膜和异位内膜中MMP-7和MMP-9蛋白表达无明显差异。MMP不同基因型携带者的患者子宫内膜组织相关基因转录活性和蛋白的表达可能不同,其结果可能导致不同个体在位内膜的差异,从而造成发病风险的不同,并且推测不同的MMPs基因在子宫内膜异位症发生和发展的不同阶段作用不同。
四、血管形成调控分子与子宫内膜异位症
尽管EMs的发病机理众说纷纷,但异位灶在腹腔种植成功后,其进一步的发展则必须要有新生血管提供血液,显然血管形成在内异症的发病中起重要作用。血管形成(angiogenesis)的概念最早在1935年使用,是指从原先存在的毛细血管中形成新生血管的过程,在胚胎发育、慢性炎症及恶性肿瘤的生长转移中具有重要作用,是一涉及多种细胞及多种分子的复杂过程,受到多种因素的调控。血管生成过程深入研究却源于对实体瘤生长的研究。随着分子生物学的发展和血管生成理论的进一步成熟,越来越多的证据表明血管生成在异位症的发生发展中占有重要位置。当脱落的子宫内膜附着在腹膜或其他部位时,异位内膜本身及其周围组织新的血供建立和维持是子宫内膜种植存活和异位症发生的基本条件。己经有数种具有血管形成活性的细胞因子被鉴定,其中包括:①成纤维细胞生长因子(FGF):它分为酸性FGF(a-FGF)和碱性FGF(b-FGF)两大类。FGF有刺激成纤维细胞、内皮细胞增殖及趋化作用,是血管形成因子之一,尤其在VEGF协同作用下,在月经周期中参与子宫内膜的修复和新生血管形成。FGF在原位或异位内膜的增生和血管形成中起一定作用。②胎盘源性的生长因子(PIGF)。③转化生长因子-a(TGF-a)。④转化生长因子-β(TGF-β):是一类多功能的调节细胞生长分化的细胞因子,有研究表明TGF-β含量在EMs患者腹腔液中较正常妇女明显升高,它可刺激多种细胞合成和分泌纤维连接素及胶原蛋白,参与粘连形成,同时对巨噬细胞、中性粒细胞和成纤维细胞有趋化作用,说明TGF-β通过多种途径参与EMs的发生发展。⑤白介素8(IL-8):EMs患者腹腔液中升高的IL-8主要由巨噬细胞分泌,腹膜间皮细胞亦可产生。目前研究认为IL-8可促进子宫内膜间质细胞增生及其对纤维素基质的粘连,使之在EMs的病理改变过程中发挥作用。⑥血小板来源的内皮生长因子(PDGF):它是内皮细胞趋化剂,通过活化磷酸胸腺嘧啶核苷参与血管形成。⑦肿瘤坏死因子-a(TNF-a):是一种多功能的细胞因子,EMs患者腹腔液中升高的TNF-α主要来源于巨噬细胞,且与病情严重程度相关。已研究证实它是重要的血管生成因子,可促进内膜异位灶的血管形成和盆腔粘连;⑧血管内皮生长因子(VEGF)等等。其中VEGF不仅可直接而特异地作用于血管内皮细胞,促进其增殖、移动及分裂,同时还增加微血管的通透性,使血浆蛋白外渗形成暂时性的基质,便于血管形成,关于VEGF的详述见本章第二节。
EMs患者的子宫内膜中,VEGF的表达高于正常内膜,而TPS-1的表达则低于正常内膜,表明内异症患者的在位内膜的血管形成活性增强。LI-6及IL-lβ可刺激子宫内膜间质细胞VEGF的分泌,对异位灶的血管形成有正调节作用。TGF-βl可刺激TSP-1的分泌,对血管形成有抑制作用。这些在内异症患者的腹水中浓度升高的细胞因子,有可能通过刺激或抑制有直接作用的血管形成分子的分泌来参与内异症的血管形成。
内分泌腺体来源的血管内皮生长因子(endoerine-glnad-derived vascular endothelial growth factor EG-VEGF)是近期美国学者发现的一种新的血管形成有丝分裂因子,它能特异性地诱导甾体激素内分泌器官的毛细血管内皮细胞增殖、迁移和膜孔形成,这恰恰是甾体激素分泌器官的特点之处,因此研究者认为EG-VEGF的功能同VEGF家族相似而又互补,其结构完全不同于VEGF。EG-VEGF的高度组织特异性给卵巢等器官血管形成相关的增殖病变带来了更广泛的研究前景。异位症为雌激素依赖性疾病,而EG-VEGF的表达水平也与雌激素水平密切相关,VEGF与异位症的密切关系提示EG-VEGF有可能在异位症发生、发展中起重要作用,比VEGF更具高度特异性,VEGF在异位症中的作用正是因为缺乏这种特异性而限制了其在异位症治疗中的应用,因为抑制VEGF的表达,不但抑制了异位症的发生,也抑制了心、脑等重要器官的血供,所以,EG-VEGF的研究更有价值。
血管生成理论及其相关细胞因子的研究,为探讨子宫内膜异位症的发病机理、发生、发展开辟了一个新的领域。随着分子生物学的研究进展,期望通过血管生成的研究,在目前药物及手术治疗的基础上,在子宫内膜异位症治疗方法上能有所突破。
五、细胞因子与子宫内膜异位症
EMs的发病机制至今尚未完全阐明,但免疫细胞分泌的细胞因子造成的腹腔内环境改变越来越受到人们的关注。细胞因子(cytokioe)是由机体的免疫细胞和某些非免疫细胞经刺激而合成和分泌的具有生物活性的小分子多肽类蛋白,能调节多种细胞的生理功能,其生物学作用主要有:参与免疫应答和免疫调节、刺激造血功能、作为免疫细胞递质参与神经内分泌免疫网络的调节,包括淋巴细胞产生的淋巴因子和单核巨噬细胞产生的单核因子等。EMs患者腹腔局部的细胞免疫功能异常,表现之一就是许多细胞因子的分泌量发生改变,这些细胞因子的改变一方面引起相应的免疫功能改变,另一方面,这些细胞因子在控制或促进局部异位内膜的种植和发展中起着作用。已知白细胞介素(IL)、肿瘤坏死因子(TNF-α)、转化生长因子(TGF-β)、干扰素(IFN)、集落刺激因子(CSF)等均是免疫细胞产生的细胞因子,在免疫系统中起着非常重要的调控作用。大量研究表明,EMs患者腹腔液中巨噬细胞数量增多、活性增强,活化的巨噬细胞释放IL-1、IL-6、IL-8、IL-10及TNF等一系列细胞因子,导致腹腔液中上述细胞因子水平升高,通过刺激T、B淋巴细胞增殖、活化,介导免疫反应,使前列腺素合成增加及局部纤维母细胞增生,胶原沉积和纤维蛋白形成,最终使盆腔纤维化和粘连,促进了EM病理生理变化的发生发展。 近年来对异位症患者的外周血、腹腔液和病灶的细胞因子变化进行了广泛的研究,发现与异位症有关的细胞因子主要有以下几种:
1.白介素因子(interleukin,IL)
众多研究表明:IL-1、IL-2、IL-4、IL-6、IL-8、IL-12、IL-13等因子与子宫内膜异位症有关。众多的研究认为IL的变化,一方面,影响机体免疫功能,使得内膜逃逸免疫监视和杀伤,产生种植;另一方面,从不同的角度激活T和B淋巴细胞,介导免疫和炎性反应,导致局部粘连形成,促进细胞的分化和增殖,抑制生殖,关于IL的描述详见本章第二节。
2.肿瘤坏死因子-α(tumor necrosis factor,TNF-α)
TNF-α是由免疫活性细胞合成和分泌的一类介导炎症和免疫反应的多肽类蛋白,它作为一种作用广泛的细胞因子具有抗肿瘤、抗感染及促血管生长等作用,具有多种生物学效应。在内异症的发生和发展过程中,它可促进子宫内膜细胞增殖,诱导腹膜间质细胞表达黏附因子,利于异位子宫内膜黏附在腹膜表面,同IL-6、IL-8一样还可造成盆腔纤维化和局部黏连,在腹膜病灶周围形成新生微小血管,参与内异症的病理过程。许多研究证实它的水平的升高与疾病严重程度呈正相关,并且TNF-α的水平在腹腔液和外周血中都随着病情的加重而升高,各期比较差异都有统计学意义,证明其水平的变化与病情的发展密切相关。有学者认为子宫内膜异位症患者腹腔液TNF-α浓度与巨噬细胞数量和活性呈正相关;EMs患者血清TNF-α水平与EMs复发有关,EMs患者血清TNF-α水平的动态检测有作为EMs疗效评价、复发及预后的重要指标。可见TNF促进异位内膜增殖,炎细胞浸润,新生血管形成,组织粘连,从而形成以为病灶。
3.趋化性细胞因子
趋化性细胞因子分为C-C、CXC、C、CX3C4个家族。单核细胞趋化蛋白属于C-C亚家族,包括MCP-1、MCP-2、MCP-3。MCP-1对单核巨噬细胞有趋化和激活作用,异位病灶的趋化性导致腹腔内巨噬细胞和淋巴细胞增多,MCP-1的上升招募并活化巨噬细胞,巨噬细胞不仅数量上增多,而且活性增强,巨噬细胞产生一系列细胞因子,加重炎症。
4.激活调节因子RANTES(regulated activation normal T cell expressed and secreted)
正常淋巴细胞表达和分泌的RANTES是一种趋化因子,为正常T淋巴细胞分泌,影响巨噬细胞的募集与激活。RANTES也被认为与子宫内膜异位症的发病有关,其血清浓度增高,且与子宫内膜异位症严重程度呈相关性。虽然荧光磁共振能量传递技术检测RANTES基因型和启动子区-403→A和-28C→G,未发现染色单体和基因型频率明显变化,但不能排除RANTES其他基因型与子宫内膜异位症的关系。体外培养中发现在位与异位内膜均可分泌RANTES、TNF-α、和INF-γ的作用可增强RANTES的分泌。
5.转化生长因子(transforming?growth?factor ,TGF)
TGF也是一种由T淋巴细胞的巨噬细胞分泌的细胞因子,在子宫内膜异位症患者也明显升高。TGF-β是一类具有多种生物功能的多肽类生长抑制因子,属于TGF-β超家族,是一种以抑制免疫为主的负向调节因子,广泛存在于动物正常组织细胞和转化细胞中,参与了哺乳动物多种细胞的生理病理过程。目前已鉴定出5种不同类型的TGF-β异构体即TGF-β1~TGF-β5,几乎存在于所有正常细胞和变异组织中,在哺乳动物体内有TGF-β1~β3种形式,在人体内主要发挥作用的是TGF-β1。TGF-β还是最具潜能的纤维化与血管发生的诱导剂。近年研究表明,在内异症的多个环节中TGF-β均存在重要作用,尤其在粘连的发生中更起到始动作用。由于免疫反应调节性降低造成局部免疫系统的功能失衡,从而导致异位病灶逃脱了免疫监视,为子宫内膜在异位处生长创造了条件,故而证实TGF-β的异常表达与异位内膜的生长及腹腔黏膜的黏连有关。在培养中,TGF-β能够刺激一些细胞生长,而抑制另一些细胞生长。由于TGF-β可以对抗淋巴细胞的许多应答反应,在子宫内膜异位症的发病中占有重要地位。如在多克隆有丝分裂原作用下,TGF-β抑制T细胞的增殖和抑制淋巴毒T淋巴细胞的成熟。在卵巢的异位内膜组织中已经发现TGF-β1、TGF-β2、TGF-β3及其受体Ⅰ、Ⅱ显著高于在位内膜组织,而且异位内膜组织中的巨噬细胞是TGF-β的主要来源,TGF-β通过旁分泌和自分泌的作用在异位内膜囊肿细胞的增殖中起着重要的调节作用。异位内膜中TGF-β1表达显著增加,且在基质细胞中呈强表达,而在上皮细胞中表达较弱,认为TGF-β1在内异症的发病机理中担当重要的角色。
六、氧化作用与子宫内膜异位症
近年来,氧化应激在子宫内膜异位症中的作用受到越来越多的关注,氧化应激与多种疾病的发生发展密切相关,并有研究发现其在其它疾病中的作用与在子宫内膜异位症中相似,因此,氧化应激是否与子宫内膜异位症不孕机制相关成为目前研究的热点。
氧化应激(oxidative stress,OS)是指体内氧化与抗氧化作用失衡,倾向于氧化,导致中性粒细胞炎性浸润,蛋白酶分泌增加,产生大量氧化中间产物,主要表现为卵泡液中活性氧簇(reactive oxygen species,ROS)增加和抗氧化剂减少或缺失,ROS清除不足,导致ROS在体内增多从而引起细胞氧化损伤。为了对抗ROS的毒副作用,机体拥有一个广泛的抗氧化系统以限制ROS的产生及蓄积,使其失活并修复受损细胞。人体内有两种类型的抗氧化剂,一种是酶类抗氧化剂(如超氧化物岐化酶、过氧化氢酶和谷胱甘肽过氧化物酶)和非酶类抗氧化剂(如维生素E、维生素C、牛磺酸和谷胱甘肽)。它们中一项若缺乏或不足,则可影响整个抗氧化系统的功能。Murphy等研究认为子宫内膜异位症的发生源于氧化应激或与之相关,盆腔子宫内膜异位症中,腹膜腔内活化的巨噬细胞可促进氧化应激的发生,并产生大量过氧化物。
ROS是一把双刃剑,在正常的生理过程中是重要的信号分子,而在病理过程中也起着重要作用。实验发现EMs患者血清及卵泡液中ROS水平均升高,且血清中抗氧化剂水平均降低,表明氧化应激在EMs患者体内确实存在。同时,EMs患者卵泡液中ROS水平显著升高,而超氧化物歧化酶(super oxide dismutase,SOD)和维生素E(vitamin E,VE)处于低水平,从而推论卵子质量可能受到氧化应激的影响,导致研究组成熟卵率和受精率较对照组显著降低。
已有研究表明,子宫内膜异位症患者腹膜腔内存在氧化应激。然而,氧化应激是否与子宫内膜异位症性不孕的发病机理有关仍不清楚。氧化应激对人类生育潜能的影响越来越受到关注。有文献指出ROS对卵母细胞成熟、卵巢类固醇激素的合成、排卵、胚胎种植、囊胚形成、黄体溶解和妊娠期黄体的维持都存在影响。同时氧化应激对受精和种植前胚胎发育的影响也已得到证实。因此,关于子宫内膜异位症患者卵泡液或颗粒细胞中是否存在氧化应激并损害卵子质量,进而对临床结局造成影响已成为了近年来研究的热点。
氧化应激在妊娠的维持、正常的生产过程和早产的启动中都起着一定的作用,也有文献报道氧化应激与妊娠期高血压疾病、葡萄胎、自由基所致出生缺陷和流产的病理生理有关。目前有正在逐渐兴起的学说提出OS对子痫前期也有一定影响。许多研究表明,子痫前期存在明显的氧化应激,并认为氧化应激增强是子痫前期发病的病因之一。Harma等观察到,补充抗氧化剂可以使高危孕妇的子痫前期发病率降低2/3,这将为子痫前期的预防和治疗提供新的选择。
七、在位内膜与异位内膜分子生物学研究
1.在位内膜
子宫在位内膜的生物学特质在内异症发病中起重要作用,甚至决定作用。研究证实,内异症患者和非内异症妇女的在位内膜之粘附、侵袭和血管形成能力均有明显差异,其强侵袭能力等生物学特质使其易于发生内异症。作为重要的前列腺素合成限速酶的环氧合酶-2(cyclooxygenase-2,Cox-2)能增加侵袭性、诱导血管形成,在内膜异位症患者的在位内膜,其表达亦明显增高,使之有助于内膜细胞的粘附侵袭。RANTES(regulated activation normal T cell expressed and secreted),正常T淋巴细胞表达和分泌的受激活调节因子可使单核巨细胞游出,激活,发生免疫异常,发生粘附和血管形成,促使EMs发生;内异症在受到RANTES之影响的同时,又正反馈地提升RANTES。这一“链式反应”在EMs患者的在位内膜表现十分明显。参与雌激素转化的P450在内膜异位症患者在位内膜亦呈高表达状态。
2.异位内膜
异位内膜组织内的E、P受体(R)表达均低于在位内膜,受内源性激素的影响较小,ER缺乏周期性变化,异位内膜组织内ERmRNA的5~7外显子的表达率高于正常位置内膜。PR则有周期性变化,在分泌期有持续高表达,在内膜异位囊肿早期腺上皮PR持续存在。有报道在内膜异位囊肿的内壁表面PR与正常内膜相同。异位内膜组织内的细胞之间ER、PR表达也存在明显差异,但卵巢的异位子宫内膜这种与在位内膜的差异相对较小,因而对激素具有周期的反应性。
芳香化酶P450是雌激素生物合成的关键酶,是细胞色素P450的一种,由血红蛋白和酶蛋白组成,可催化C-19雄激素转化为E2。正常子宫内膜和肌层不表达此酶,而子宫内膜异位症、子宫腺肌症患者宫腔内膜及腹腔种植病灶中均有芳香化酶的高度表达,这种表达受细胞因子和生长因子的调节。提示异位内膜有局部合成E2的能力,局部E2的增多一方面促进异位内膜的种植和增生,另一方面导致不孕。有报道EMs和子宫腺肌症的子宫内膜存在NO合成酶的持续高表达。
八、免疫异常与子宫内膜异位症
1.体液免疫
研究发现子宫内膜异位症患者的子宫内膜有补体C3及IgG沉积、血清总补体水平相应下降。另外,子宫内膜异位症患者血清及腹腔液补体C3及C4水平比对照组升高。Mathur从子宫内膜异位症患者的血清、宫颈及阴道分泌物分离出抗子宫内膜组织的IgG及IgA自身抗体。进一步研究发现,血清中子宫内膜抗体仅作用于子宫内膜异位症患者的子宫内膜及异位种植组织;很少与正常生育组的子宫内膜抗原反应。此外,Wild等研究显示,仅子宫内膜异位症患者IgG F(ab)2与内膜抗原反应;而患者的IgG Fc段及正常生育妇女IgG F(ab)2并不能与内膜抗原结合。Ⅲ~Ⅳ期子宫内膜异位症患者,外周血磷脂抗体阳性率为56.3%,明显高于除外子宫内膜异位症的正常生育期妇女。以上事实说明,子宫内膜异位症患者体内可能产生多种自身抗体及多克隆B细胞激活。这种多克隆B细胞激活,可能扰乱了子宫内膜异位症患者的神经-生殖内分泌-免疫调节网格。
子宫内膜异位症符合自身免疫性疾病的大部分经典特征:多克隆B细胞激活、组织损伤、多器官累及、女性易感、家族史、其他自身免疫病患病率增加。然而,将子宫内膜异位症看作自身免疫病仍需更多的证据。
最近人们还注意,子宫内膜异位症患者甚至其亲属属过敏体质,容易对各种致敏原如尘埃、花粉。青霉素类药物、香水等化学制品发生过敏反应,并引起过敏性疾病如荨麻疹、哮喘、过敏性肠炎等。子宫内膜异位症及白色念珠菌也和这些过敏性疾病一样存在IgE介导的迟发型变态反应。因此,子宫内膜异位症是否与过敏性疾病发病机制相似,需进一步探讨。
CA125抗原是主要由卵巢癌表达的肿瘤相关抗原。子宫内膜异位症患者CA125抗原高度表达,而且腹腔液中CA125浓度高于外周血,子宫内膜异位症患者体内CA125水平的升高可能由于异位灶及在位内膜上皮细胞共同分泌增加所致。研究表明,随着子宫内膜异位症的加重,CA125抗原浓度及发生率均呈明显增加,因此,系列检测CA125抗原将有助于监测患者病情进程。
2.细胞免疫
自发性子宫内膜异位症恒河猴T细胞反应性降低,对自体子宫内膜细胞免疫受抑。与未患子宫内膜异位症不孕妇女相比,患子宫内膜异位症的不孕妇女针对自体子宫内膜细胞的T细胞毒性明显下降。关于子宫内膜异位症患者外周淋巴数目的改变目前无统一的说法。
与未患子宫内膜异位症的正常生育期妇女比较,子宫内膜异位症患者外周血CD3、CD4细胞及CD4/ CD8比例明显下降;血清IgG及补体C3、C4明显升高,细胞免疫功能明显下降。
NK细胞是大颗粒淋巴细胞,杀伤携有靶分子或包被了抗体的细胞,子宫内膜异位症患者外周或腹腔液NK细胞对自体或异体子宫内膜细胞毒性明显降低。在中度及重度子宫内膜异位症腹腔液局部NK细胞活性下降更明显,因而不能有效防止返流的子宫内膜细胞的腹腔种植及生长,在子宫内膜异位症发病机制中有重要作用。另子宫内膜异位症患者血清或腹腔液处理NK细胞,使NK细胞杀伤活性明显下降,但NK细胞百分率无明显改变或增加。
3.腹腔局部免疫
单核-巨噬细胞系统在维持细胞免疫过程中起核心作用。巨噬细胞在腹腔内含量最丰富,在局部免疫应答中起重要作用。子宫内膜异位症不孕症患者腹腔巨噬细胞数显著增加,巨噬细胞浓度及激活增加,子宫内膜异位症严重程度似乎与巨噬细胞数无明显相关,但轻、中度子宫内膜异位症巨噬细胞数较高。一些研究分析巨噬细胞激活状态与子宫内膜异位症及不孕症相关性,显示巨噬细胞激活状态比巨噬细胞浓度更重要。子宫内膜异位症患者腹腔巨噬细胞高度激活,其分化程度亦高于未患子宫内膜异位症的生育期妇女。
一些研究证实,子宫内膜异位症的巨噬细胞激活伴随多种生长因子产生,如PDGF、TGF-β及EGF。这些生长因子刺激子宫内膜间质细胞增生,推测它们增强了子宫内膜细胞的异位种植。TGF-β能严重抑制T、B细胞及NK细胞的功能。PDFG增强子宫内膜间质细胞最大限度地生长刺激。
可溶性细胞介质、 细胞因子,具有多种生物学活性,包括调节生长、激活及趋化作用。子宫内膜异位症腹腔液TNF-α、IL-1、IL-6、IL-8、单核细胞趋化蛋白(MCP)-1和IFN-γ升高,提示这些细胞因子参与子宫内膜异位症发展。
总之,免疫性因子可影响妇女子宫内膜异位种植的易感性。免疫改变包括循环自身抗体增加,腹腔巨噬细胞增加并激活,T细胞反应性及NK细胞活性下降。这些免疫变化造成子宫内膜异位症患者着床率下降。
 妇产科在线APP下载
妇产科在线APP下载










 京公网安备 11010202008857号
京公网安备 11010202008857号