【编者按】子宫内膜癌是妇科常见的恶性肿瘤之一,最近几十年在中国发病率呈逐年上升的趋势。早期发现子宫内膜癌,不仅能够减少患者的死亡率和复发率,而且能够改善患者的生存质量。随着微创技术的进展,宫腔镜已经越来越被应用于子宫内膜癌的诊断和治疗。尽管大量的研究已经证实宫腔镜用于诊断子宫内膜癌的价值,然而关于宫腔镜应用的真正价值仍然存在一些担忧,故此需要进行进一步的调查和探讨。

目前的争论热点
宫腔镜与分段诊刮术在诊断子宫内膜癌时效果的区别。
癌细胞随宫腔镜检查媒介逆行性播散的潜在危险。
2012年宫腔镜诊治规范
1、宫腔镜检查的适应症:可疑宫腔内的病变,均为宫腔镜检查的适应症。包括异常子宫出血、宫腔内占位性病变、宫内节育器异常及宫内异物、不孕不育、宫腔粘连、子宫畸形、宫腔影像学检查异常、宫腔镜术后相关评估、阴道排液和(或)幼女期阴道异物。子宫内膜癌和宫颈管癌手术前病变范围观察及镜下取活检。2012中国的宫腔镜指南提出子宫内膜癌及宫颈管癌为宫腔镜检查的指征。
2、宫腔镜检查的禁忌症:宫腔镜检查无绝对禁忌症,某些情况下为相对禁忌症。包括体温>37.5度;子宫活跃性大量出血、重度贫血;急性或亚急性生殖道或盆腔炎症;近期发生子宫穿孔;宫腔过度狭小或宫颈管狭窄、坚硬、难以扩张;浸润性宫颈癌、生殖道结核未经抗结核治疗;严重的内、外科合并症不能耐受手术操作。
3、宫腔镜手术中常用技巧:
子宫内膜活检术:在宫腔镜直视下评估宫腔形态及宫腔和(或)宫颈管病变,对可疑病变部位进行活检,注意活检组织的大小。
子宫内膜切除或去除术:以环状或球状电极顺序切除或凝固子宫内膜,切除或凝固深度应包括子宫内膜全层及其下方2~3mm的肌肉组织。
4、2015年美国妇产协会(ACOG)指南中提到,宫腔镜尽管并非必须,但仍推荐和诊刮一起进行,以识别不连续的病灶及其背景内膜。这种联合检查可以为真正的内膜癌前病变提供确诊的最佳机会,并能排除相关的内膜癌变。门诊以一次性器械进行内膜活检对于绝大部分内膜癌患者而言是可靠而准确的,已经成为组织学评估内膜的首选方法。内膜癌的初期治疗应该包括完整的手术分期(全子宫及双附件切除,盆腔及腹主动脉旁淋巴结切除,腹膜细胞学腹腔冲洗的收集)。只有在和内膜癌诊疗专家(如妇科肿瘤专家)进行咨询之后,才能决定其他治疗方案以取代上述初期治疗方案。
宫腔镜在子宫内膜癌诊治中的优势与缺陷
宫腔镜诊断子宫内膜癌的优点:1,可依据肿块外观定性;2,与普通诊刮相比,能够帮助子宫癌症分期;3,定位直视下活检,提高检出率;4,判断宫颈管内有无癌浸润,为子宫内膜癌分期。
宫腔镜与彩色多普勒超声对比
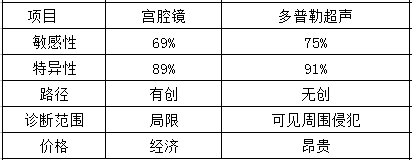
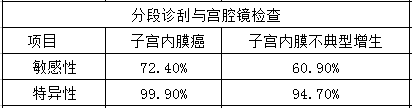
传统的分段诊刮漏诊率高达10-15%,对子宫内膜不典型增生的漏诊率则更高。一项研究表明,传统诊刮中有60%刮出子宫内膜组织<50%,16%刮出内膜组织<25%。宫腔镜检查相对于传统诊刮,漏诊率更低,且对子宫内膜不典型增生的敏感性更高。
宫腔镜诊断子宫内膜癌的缺点:1,费用相对普通分段诊刮更昂贵;2,膨宫液逆流入腹腔可能造成肿瘤向附件和盆腔扩散;3,膨宫液逆流入盆腔可能造成人为因素的分期错误。
宫腔镜腹水阳性率:美国一例临床试验对64例有宫腔镜检查史的患者及158例无宫腔镜手术史的子宫内膜癌患者进行腹水分析,结果如下:
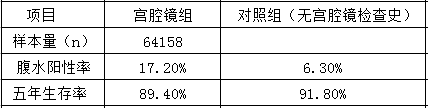
结论:宫腔镜检查可能提高腹水中癌细胞的阳性率,但五年生存率无显著差异。
关于腹水阳性率:1,腹水阳性率目前各实验结论不一致;2,腹水阳性率可能与腹水的取材时机、膨宫介质、膨宫压力、肿瘤的分期分级等多种因素有关;3,扩散至腹腔不等于腹腔内种植转移,但会增加腹腔内转移的风险;4,传统的诊刮术亦有腹腔内播散的风险;5,腹水假阳性可能干扰手术分期。
子宫内膜癌的宫腔镜所见:色泽是不透明的黄白色或灰白色;坏死:白色点状或小斑状;宫颈管内浸润:与宫腔内的病灶有连续关系;隆起,结节状、乳头状、息肉状(卵圆形或球形)、绒毛状突起;血管怒张,不规则的蛇形,时隐时现;溃疡:不整洁、粗糙的外观。
子宫内膜癌的宫腔镜诊断要点:具有中心血管的半透明绒毛状突起群,很可能高分化内膜腺癌;有异型血管,特别是不整的扩张血管;结节状隆起或息肉隆起,质地脆弱;有白点状或斑状的坏死组织。
宫腔镜操作前子宫内膜的预处理
药物预处理:促性腺激素释放激素激动剂(GnRH-a)或孕三烯酮等,使用2~3个月,抑制内膜增生,薄化子宫内膜。机械性预处理:术中负压吸宫,薄化子宫内膜(不孕症及宫腔粘连者慎用)。
目的:1、宫腔背景清晰,易于发现病灶;2、缩短手术时间,减少并发症;3、减少子宫内膜腺体,减少膨宫液吸收;4、增加子宫内膜电切术的效果。
膨宫介质的选择
气体:CO2可进行宫腔染色,需特殊装置。CO2指数为1.00,与其他介质比较,视野相对较大,清晰度高,不如液体膨宫简便。
5%葡萄糖液体:粘稠度较高,视野清晰,取材方便,便宜,使用时器械、手套表明发粘,产生不适感。
生理盐水液体:折射指数为1.37,为等渗液,易于冲去宫内组织碎片和血块,但粘稠度差,易于血液混合,妨碍视线。
Hyskon液体:为高粘稠度膨宫液,是32%的右旋糖酐,70%与10%的葡萄糖的混合液。优点为粘度大,用量少,不易与血液、粘液混合,尤适用于子宫出血病人。缺点为价格昂贵,易形成结晶,清洗困难,并有个别发生过敏者。
宫腔镜手术在子宫内膜癌中的应用
宫腔镜经宫颈管子宫内膜切除术(TCRE),是早期子宫内膜癌并有强烈生育愿望患者治疗的一种选择。宫腔镜下局部切除病灶,减少肿瘤负荷,增强药物治疗,术后辅以高效孕激素3-6个月,复查无复发可尝试妊娠。TCRE不适子宫内膜癌的标准手术,仅适用于早期高分化子宫内膜腺癌患者,手术利弊需向患者说明。
保留子宫的指征,根据2016年NCCN子宫肿瘤指南:1,适用于子宫内膜样腺癌、子宫内膜浆液性癌、透明细胞癌,癌肉瘤和子宫肉瘤不能保留生育功能。2,分段诊刮标本经病理专家核实,病理类型为子宫内膜样腺癌G1级。3,磁共振(MRI)检查(首选)或经阴道超声检查发现病灶局限于子宫内膜。4,影像学检查未发现可疑的转移病灶。
保留生育功能后续治疗
根据2016年NCCN子宫肿瘤指南,可给予高效孕激素或左炔诺孕酮宫内缓释系统。治疗期间每3-6个月分段诊刮或取子宫内膜活检,若子宫内膜癌持续存在6-9个月,则行全子宫+双附件切除+手术分期;若6个月后病变完全缓解,鼓励患者受孕,孕前持续每3-6个月进行内膜取样检查,若患者暂无生育计划,予孕激素维持治疗及定期监测。完成生育后或内膜取样发现疾病进展,需进行全面的子宫内膜癌分期手术。
小结:目前无指南指出宫腔镜在子宫内膜癌诊断中的必要性。宫腔镜能够提高子宫内膜癌诊断的敏感性和特异性。宫腔镜存在肿瘤细胞向盆腔内播散的风险。宫腔镜检查史不明显减低患者五年生存率。宫腔镜手术可保留早期G1级子宫内膜癌患者的生育功能。目前宫腔镜在子宫内膜癌的应用仍有争议,且缺乏高级别证据。
 妇产科在线APP下载
妇产科在线APP下载










 京公网安备 11010202008857号
京公网安备 11010202008857号